第100页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
1. 空运观赏鱼必须密封。为了解决鱼的吸氧问题,可在水中加入过氧化钙$(CaO_2),$其与水反应的化学方程式为$ 2CaO_2 + 2H_2O = 2Ca(OH)_2 + O_2↑。$若要产生 3.2 g 氧气,应向水中投入过氧化钙的质量为(
A.14.4 g
B.7.2 g
C.2 g
D.18.2 g
A
)A.14.4 g
B.7.2 g
C.2 g
D.18.2 g
答案:
A
2. (教材习题变式)在反应$ 2Mg + O_2\xlongequal{点燃}2MgO $中,镁、氧气、氧化镁的质量比为(
A.48∶32∶80
B.24∶32∶40
C.24∶32∶64
D.24∶32∶80
A
)A.48∶32∶80
B.24∶32∶40
C.24∶32∶64
D.24∶32∶80
答案:
A
3. 取$ 20.0 g KMnO_4 $固体制氧气,加热一段时间后,固体质量减少 1.6 g。已分解$ KMnO_4 $的质量占取用$ KMnO_4 $总质量的百分率为(
A.8%
B.39.5%
C.79%
D.92%
C
)A.8%
B.39.5%
C.79%
D.92%
答案:
C
4. 在化学反应$ A + B_2 = AB_2 $中,A 与$ B_2 $反应的质量关系如图所示,现将 8 g A 和$ 5 g B_2 $充分反应,则生成$ AB_2 $的质量是(
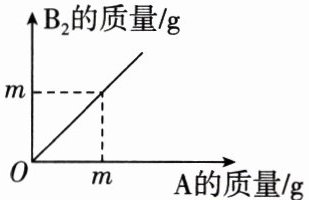
A.10 g
B.13 g
C.16 g
D.18 g
A
)
A.10 g
B.13 g
C.16 g
D.18 g
答案:
A
5. (2024 德阳中考)某火力发电厂为防止燃煤烟气中的 SO_2 污染环境,使用石灰石进行烟气脱硫,发生反应:$2CaCO_3 + 2SO_2 + O_2\xlongequal{高温}2CaSO_4 + 2CO_2,$生成的 CaSO_4 可用作建筑材料的原料。如果将燃煤烟气中的 256 kg SO_2 全部吸收,至少需要 CaCO_3 的质量是多少?
答案:
解:设至少需要CaCO₃的质量是x。
2CaCO₃ + 2SO₂+O₂$\xlongequal{高温}$2CaSO₄+2CO₂
200 128
x 256 kg
$\frac{200}{128}$=$\frac{x}{256\ kg}$ x=400 kg
答:至少需要CaCO₃的质量是400 kg。
2CaCO₃ + 2SO₂+O₂$\xlongequal{高温}$2CaSO₄+2CO₂
200 128
x 256 kg
$\frac{200}{128}$=$\frac{x}{256\ kg}$ x=400 kg
答:至少需要CaCO₃的质量是400 kg。
6. 某化学兴趣小组的同学为测定实验室里一瓶过氧化氢溶液中过氧化氢的质量,进行了相关实验,实验数据记录如下:
|过氧化氢溶液 34 g| + |二氧化锰 2 g|
|完全反应|→|固液残留物 35.2 g|

请计算:
(1)生成氧气
(2)此过氧化氢溶液中过氧化氢的质量。
|过氧化氢溶液 34 g| + |二氧化锰 2 g|
|完全反应|→|固液残留物 35.2 g|

请计算:
(1)生成氧气
0.8
g。(2)此过氧化氢溶液中过氧化氢的质量。
答案:
(1)0.8
(2)解:设过氧化氢溶液中过氧化氢的质量为x。
2H₂O₂$\xlongequal{MnO_2}$2H₂O+O₂↑
68 32
x 0.8 g
$\frac{68}{32}$=$\frac{x}{0.8\ g}$ x=1.7 g
答:此过氧化氢溶液中过氧化氢的质量为1.7 g。
(1)0.8
(2)解:设过氧化氢溶液中过氧化氢的质量为x。
2H₂O₂$\xlongequal{MnO_2}$2H₂O+O₂↑
68 32
x 0.8 g
$\frac{68}{32}$=$\frac{x}{0.8\ g}$ x=1.7 g
答:此过氧化氢溶液中过氧化氢的质量为1.7 g。
查看更多完整答案,请扫码查看


