第53页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
8. 将炭粉和氧化铜粉末的混合物共 22g,在高温条件下反应一段时间后,称得剩余固体的质量为 17.6g,该反应的化学方程式为${C + 2CuO\xlongequal{高温}2Cu + CO_{2}\uparrow}$。请回答下列问题:
(1)该反应生成二氧化碳的质量为
(2)该反应中参与反应的氧化铜的质量为多少?(请写出具体的计算过程)
(1)该反应生成二氧化碳的质量为
4.4
g。(2)该反应中参与反应的氧化铜的质量为多少?(请写出具体的计算过程)
答案:
8.
(1)4.4
(2)解:设参与反应的氧化铜的质量为x。
$C + 2CuO \overset{高温}{=}2Cu + CO₂↑$
160 44
x 4.4 g
$\frac{160}{44} = \frac{x}{4.4 g} x = 16 g$
答:该反应中参与反应的氧化铜的质量为16 g。
(1)4.4
(2)解:设参与反应的氧化铜的质量为x。
$C + 2CuO \overset{高温}{=}2Cu + CO₂↑$
160 44
x 4.4 g
$\frac{160}{44} = \frac{x}{4.4 g} x = 16 g$
答:该反应中参与反应的氧化铜的质量为16 g。
9. 实验室通常用过氧化氢溶液与二氧化锰混合制取氧气,取烧杯向其中加入 18g 过氧化氢溶液和 2g 二氧化锰,随着反应的发生,烧杯内物质质量变化情况如上示意图所示,据此回答下列问题:
(1)反应结束生成氧气的质量为
(2)参加反应的过氧化氢的质量为多少?(写出计算过程)
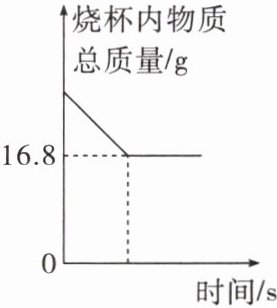
(1)反应结束生成氧气的质量为
3.2
g。(2)参加反应的过氧化氢的质量为多少?(写出计算过程)

答案:
9.
(1)3.2
(2)解:设参加反应的过氧化氢的质量为x。
$2H₂O₂ \overset{MnO₂}{=}2H₂O + O₂↑$
68 32
x 3.2 g
$\frac{68}{32} = \frac{x}{3.2 g} x = 6.8 g$
答:参加反应的过氧化氢的质量为6.8 g。
(1)3.2
(2)解:设参加反应的过氧化氢的质量为x。
$2H₂O₂ \overset{MnO₂}{=}2H₂O + O₂↑$
68 32
x 3.2 g
$\frac{68}{32} = \frac{x}{3.2 g} x = 6.8 g$
答:参加反应的过氧化氢的质量为6.8 g。
10. 科技兴则民族兴,科技强则国家强。中国科学家在国际上首次实现了二氧化碳到淀粉的人工合成,为淀粉工业制造和二氧化碳利用打开了一扇窗。部分人工合成淀粉路线如图:
$\begin{matrix}二氧 & \xrightarrow[一定条件]{氢气} & 甲醇 & \xrightarrow[转化]{再经系列催化} & 淀粉 \\化碳 & & ({CH_{3}OH}) & & □ \\$ $\end{matrix}$
$\end{matrix}$
(1)淀粉${(C_{6}H_{10}O_{5})_{n}}$中碳元素与氢元素的质量比是
(2)已知二氧化碳转化为甲醇反应的化学方程式为${CO_{2} + 3H_{2}\xlongequal{一定条件}CH_{3}OH + H_{2}O}$。则 6.6g ${CO_{2}}$理论上可制备${CH_{3}OH}$的质量是多少?(写出计算过程)
$\begin{matrix}二氧 & \xrightarrow[一定条件]{氢气} & 甲醇 & \xrightarrow[转化]{再经系列催化} & 淀粉 \\化碳 & & ({CH_{3}OH}) & & □ \\$
 $\end{matrix}$
$\end{matrix}$(1)淀粉${(C_{6}H_{10}O_{5})_{n}}$中碳元素与氢元素的质量比是
36 : 5
。(2)已知二氧化碳转化为甲醇反应的化学方程式为${CO_{2} + 3H_{2}\xlongequal{一定条件}CH_{3}OH + H_{2}O}$。则 6.6g ${CO_{2}}$理论上可制备${CH_{3}OH}$的质量是多少?(写出计算过程)
答案:
10.
(1)36 : 5
(2)解:设可制备甲醇的质量为x。
$CO₂ + 3H₂ \overset{一定条件}{=}CH₃OH + H₂O$
44 32
6.6 g x
$\frac{44}{32} = \frac{6.6 g}{x} x = 4.8 g$
答:理论上可制备甲醇的质量为4.8 g。
(1)36 : 5
(2)解:设可制备甲醇的质量为x。
$CO₂ + 3H₂ \overset{一定条件}{=}CH₃OH + H₂O$
44 32
6.6 g x
$\frac{44}{32} = \frac{6.6 g}{x} x = 4.8 g$
答:理论上可制备甲醇的质量为4.8 g。
查看更多完整答案,请扫码查看


