第28页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
1. 现有一瓶溶质质量分数为10%的食盐水,下列关于该食盐水的说法正确的是 (
A.$m_{质}:m_{剂}= 1:10$
B.$m_{质}:m_{液}= 1:10$
C.$m_{质}:m_{液}= 1:11$
D.$m_{剂}:m_{液}= 10:11$
B
)A.$m_{质}:m_{剂}= 1:10$
B.$m_{质}:m_{液}= 1:10$
C.$m_{质}:m_{液}= 1:11$
D.$m_{剂}:m_{液}= 10:11$
答案:
B
2. (2024 武汉)实验室配制一定溶质质量分数的氯化钠溶液,下列操作错误的是 (
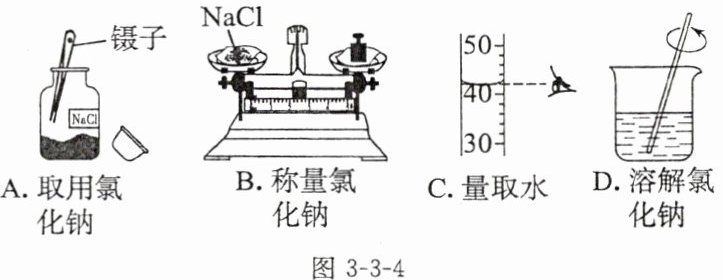
A
)
答案:
A
3. (2024 广西)实验室要配制50 g溶质质量分数为16%的氯化钠溶液,下列做法错误的是 (
A.计算:配制该溶液所需氯化钠固体的质量为8.0 g
B.称量:用托盘天平称量所需的氯化钠固体
C.溶解:将称量好的氯化钠固体倒入量筒中溶解
D.装瓶:将配制好的溶液装入贴好标签的试剂瓶并盖好瓶塞
C
)A.计算:配制该溶液所需氯化钠固体的质量为8.0 g
B.称量:用托盘天平称量所需的氯化钠固体
C.溶解:将称量好的氯化钠固体倒入量筒中溶解
D.装瓶:将配制好的溶液装入贴好标签的试剂瓶并盖好瓶塞
答案:
C
4. 在配制50 g溶质质量分数为6%的氯化钠溶液时,下列实验操作与目的分析均正确的是 (
|选项|实验操作|目的分析|
|A|称取氯化钠时,在两边托盘上各放一张相同的纸张|整洁美观|
|B|称取氯化钠时,将剩余的氯化钠放回原瓶|节约试剂|
|C|量取水时,视线与量筒内液体凹液面的最低处保持水平|准确读数|
|D|溶解氯化钠时,用玻璃棒搅拌|增大氯化钠在水中的最大溶解量|
C
)|选项|实验操作|目的分析|
|A|称取氯化钠时,在两边托盘上各放一张相同的纸张|整洁美观|
|B|称取氯化钠时,将剩余的氯化钠放回原瓶|节约试剂|
|C|量取水时,视线与量筒内液体凹液面的最低处保持水平|准确读数|
|D|溶解氯化钠时,用玻璃棒搅拌|增大氯化钠在水中的最大溶解量|

答案:
C
5. (2023 辽宁改编)用溶质质量分数为98%的浓硫酸配制100 g溶质质量分数为10%的稀硫酸。下列说法正确的是 (
A.需要98%的浓硫酸的质量为10 g,水的质量为90 g
B.用量筒量取浓硫酸时仰视读数,会导致配制的溶液溶质质量分数偏大
C.实验中需要的仪器有:烧杯、相应规格的量筒、胶头滴管、玻璃棒及托盘天平
D.装瓶时有少量液体溅出,会导致配制的溶液溶质质量分数偏小
B
)A.需要98%的浓硫酸的质量为10 g,水的质量为90 g
B.用量筒量取浓硫酸时仰视读数,会导致配制的溶液溶质质量分数偏大
C.实验中需要的仪器有:烧杯、相应规格的量筒、胶头滴管、玻璃棒及托盘天平
D.装瓶时有少量液体溅出,会导致配制的溶液溶质质量分数偏小
答案:
B
6. 将80 g溶质质量分数为20%的浓盐酸稀释成10%的稀盐酸,需加水的质量为 (
A.80 g
B.100 g
C.200 g
D.280 g
A
)A.80 g
B.100 g
C.200 g
D.280 g
答案:
A
7. 对溶质质量分数为25%的食盐溶液,下列操作及解释正确的是 (
A.将25 g食盐全部溶解于100 g水中,得到的溶液
B.再加25 g食盐,溶质质量分数变为原来的2倍
C.将25 g食盐全部溶解在75 g水中形成的溶液
D.将溶液中的水蒸发掉一半,其溶质质量分数变为50%
C
)A.将25 g食盐全部溶解于100 g水中,得到的溶液
B.再加25 g食盐,溶质质量分数变为原来的2倍
C.将25 g食盐全部溶解在75 g水中形成的溶液
D.将溶液中的水蒸发掉一半,其溶质质量分数变为50%
答案:
C
8. 常温下将6 g氯化钠完全溶于54 g水中,将所得溶液均分成6份,请完成下列计算。
(1)第一份溶液中,溶质质量分数为
(2)向第二份溶液中加入0.8 g氯化钠,完全溶解,溶质质量分数为
(3)向第三份溶液中加入10 g水,溶质质量分数为
(4)将第四份溶液蒸发5 g水(无氯化钠析出),溶质质量分数为
(5)向第五份溶液中加入1 g氯化钠,完全溶解,再蒸发1 g水(无氯化钠析出),溶质质量分数为
(6)向第六份溶液中加入1 g氯化钠,若要使溶质质量分数保持不变,则需再加水
(1)第一份溶液中,溶质质量分数为
10%
。(2)向第二份溶液中加入0.8 g氯化钠,完全溶解,溶质质量分数为
16.7%
(精确到0.1%)。(3)向第三份溶液中加入10 g水,溶质质量分数为
5%
。(4)将第四份溶液蒸发5 g水(无氯化钠析出),溶质质量分数为
20%
。(5)向第五份溶液中加入1 g氯化钠,完全溶解,再蒸发1 g水(无氯化钠析出),溶质质量分数为
20%
。(6)向第六份溶液中加入1 g氯化钠,若要使溶质质量分数保持不变,则需再加水
9
g。
答案:
(1)10% (2)16.7% (3)5% (4)20% (5)20% (6)9
查看更多完整答案,请扫码查看


