15. 1.6 g某物质完全燃烧后生成4.4 g $CO_{2}$和3.6 g $H_{2}O$,下列关于该物质的说法:①一定含碳、氢元素;②一定不含氧元素;③可能含氧元素;④一定含氧元素;⑤分子中碳、氢原子的个数比为1∶2;⑥分子中碳、氢原子的个数比为1∶4。其中正确的是(
A.①④⑤
B.①③⑥
C.①②⑤
D.①②⑥
D
)A.①④⑤
B.①③⑥
C.①②⑤
D.①②⑥
答案:
D
16. (6分)我们通常通过化学反应来认识物质的化学性质。氢气具有可燃性,在空气中燃烧的化学方程式为
A. $3Fe+2O_{2}\xlongequal{点燃}Fe_{3}O_{4}$ B. $Fe+2FeCl_{3}= 3FeCl_{2}$
C. $3CO+Fe_{2}O_{3}\xlongequal{高温}2Fe+3CO_{2}$ D. $Fe+CuSO_{4}= FeSO_{4}+Cu$
$2\mathrm{H}_{2}+\mathrm{O}_{2}\xlongequal{点燃}2\mathrm{H}_{2}\mathrm{O}$
,该反应属于基本反应类型中的化合
反应。氢气具有还原性,可以和CuO反应,化学方程式为$H_{2}+CuO\xlongequal{\triangle}Cu+H_{2}O$。我们常从元素化合价变化的角度来认识氧化—还原反应:在化学反应中,只要有元素化合价升高的反应物就具有还原性。上述两个反应中,氢元素的化合价都从0
变成+1
,都能体现氢气具有还原性。从元素化合价的变化特点来分析,在下列四个反应中,能体现金属铁具有还原性的反应有ABD
(填字母)。 A. $3Fe+2O_{2}\xlongequal{点燃}Fe_{3}O_{4}$ B. $Fe+2FeCl_{3}= 3FeCl_{2}$
C. $3CO+Fe_{2}O_{3}\xlongequal{高温}2Fe+3CO_{2}$ D. $Fe+CuSO_{4}= FeSO_{4}+Cu$
答案:
$2\mathrm{H}_{2}+\mathrm{O}_{2}\xlongequal{点燃}2\mathrm{H}_{2}\mathrm{O}$ 化合 0 +1 ABD
|化学方程式|评价|反应类型|
|(1)$H_{2}O_{2}\xlongequal{MnO_{2}}H_{2}\uparrow+O_{2}\uparrow$|
|(2)$P+O_{2}\xlongequal{点燃}P_{2}O_{5}$|
|(3)$H_{2}+CuO\xlongequal{\triangle}Cu+H_{2}O$|
|(4)$Ca(OH)_{2}+CO_{2}\uparrow=CaCO_{3}\downarrow+H_{2}O$|
|(1)$H_{2}O_{2}\xlongequal{MnO_{2}}H_{2}\uparrow+O_{2}\uparrow$|
B
|①
||(2)$P+O_{2}\xlongequal{点燃}P_{2}O_{5}$|
C
|②
||(3)$H_{2}+CuO\xlongequal{\triangle}Cu+H_{2}O$|
A
|③
||(4)$Ca(OH)_{2}+CO_{2}\uparrow=CaCO_{3}\downarrow+H_{2}O$|
D
|③
|
答案:
(1)B ①
(2)C ②
(3)A ③
(4)D ③
(1)B ①
(2)C ②
(3)A ③
(4)D ③
18. (4分)从古至今,化学一直渗透于我们的生产和生活之中。
(1)在高温条件下向金红石(主要成分为$TiO_{2}$)与炭粉的混合物中通入氯气($Cl_{2}$),制得四氯化钛($TiCl_{4}$)和一种可燃性气体(CO),发生反应的化学方程式为
(2)某化学反应前后分子种类变化的微观示意图如图5-C-5,请回答下列问题。
①该反应中生成物丙的化学式为
②该反应中甲、乙两种反应物的分子个数比为
(1)在高温条件下向金红石(主要成分为$TiO_{2}$)与炭粉的混合物中通入氯气($Cl_{2}$),制得四氯化钛($TiCl_{4}$)和一种可燃性气体(CO),发生反应的化学方程式为
$\mathrm{Ti}\mathrm{O}_{2}+2\mathrm{C}+2\mathrm{Cl}_{2}\xlongequal{高温}\mathrm{Ti}\mathrm{Cl}_{4}+2\mathrm{CO}$
。 (2)某化学反应前后分子种类变化的微观示意图如图5-C-5,请回答下列问题。
①该反应中生成物丙的化学式为
$\mathrm{SO}_{2}$
。 ②该反应中甲、乙两种反应物的分子个数比为
$2:3$
。
答案:
(1)$\mathrm{Ti}\mathrm{O}_{2}+2\mathrm{C}+2\mathrm{Cl}_{2}\xlongequal{高温}\mathrm{Ti}\mathrm{Cl}_{4}+2\mathrm{CO}$
(2)①$\mathrm{SO}_{2}$ ②$2:3$
(1)$\mathrm{Ti}\mathrm{O}_{2}+2\mathrm{C}+2\mathrm{Cl}_{2}\xlongequal{高温}\mathrm{Ti}\mathrm{Cl}_{4}+2\mathrm{CO}$
(2)①$\mathrm{SO}_{2}$ ②$2:3$
19. (6分)质量守恒定律是一条重要的规律,请利用该规律的相关知识回答下列问题。
(1)化学反应前后肯定没有发生变化的是
①原子数目 ②分子数目 ③元素种类 ④物质种类 ⑤原子种类 ⑥物质的总质量 ⑦分子种类
(2)镁条在空气中完全燃烧后生成氧化镁(只考虑氧气参加反应,下同),反应的化学方程式为
(3)实验过程中,镁条燃烧时实验现象如图Ⅱ所示,镁条完全燃烧后,称得陶土网上剩余固体的质量反而比反应前镁条的质量轻,其原因可能是
(1)化学反应前后肯定没有发生变化的是
①③⑤⑥
(填序号)。 ①原子数目 ②分子数目 ③元素种类 ④物质种类 ⑤原子种类 ⑥物质的总质量 ⑦分子种类
(2)镁条在空气中完全燃烧后生成氧化镁(只考虑氧气参加反应,下同),反应的化学方程式为
$2\mathrm{Mg}+\mathrm{O}_{2}\xlongequal{点燃}2\mathrm{Mg}\mathrm{O}$
,若固体质量变化情况用图5-C-6Ⅰ表示,则$m_{2}与m_{1}$之差表示参加反应的氧气
的质量。 (3)实验过程中,镁条燃烧时实验现象如图Ⅱ所示,镁条完全燃烧后,称得陶土网上剩余固体的质量反而比反应前镁条的质量轻,其原因可能是
反应生成白烟,部分生成物逸散到空气中,未被称量 (合理即可)
。
答案:
(1)①③⑤⑥
(2)$2\mathrm{Mg}+\mathrm{O}_{2}\xlongequal{点燃}2\mathrm{Mg}\mathrm{O}$ 参加反应的氧气
(3)反应生成白烟,部分生成物逸散到空气中,未被称量 (合理即可)
(1)①③⑤⑥
(2)$2\mathrm{Mg}+\mathrm{O}_{2}\xlongequal{点燃}2\mathrm{Mg}\mathrm{O}$ 参加反应的氧气
(3)反应生成白烟,部分生成物逸散到空气中,未被称量 (合理即可)
20. 定律是对自然现象或关系的描述,通常可用数学方式加以表达。在学习“质量守恒定律”时,小丽查阅到以下材料。
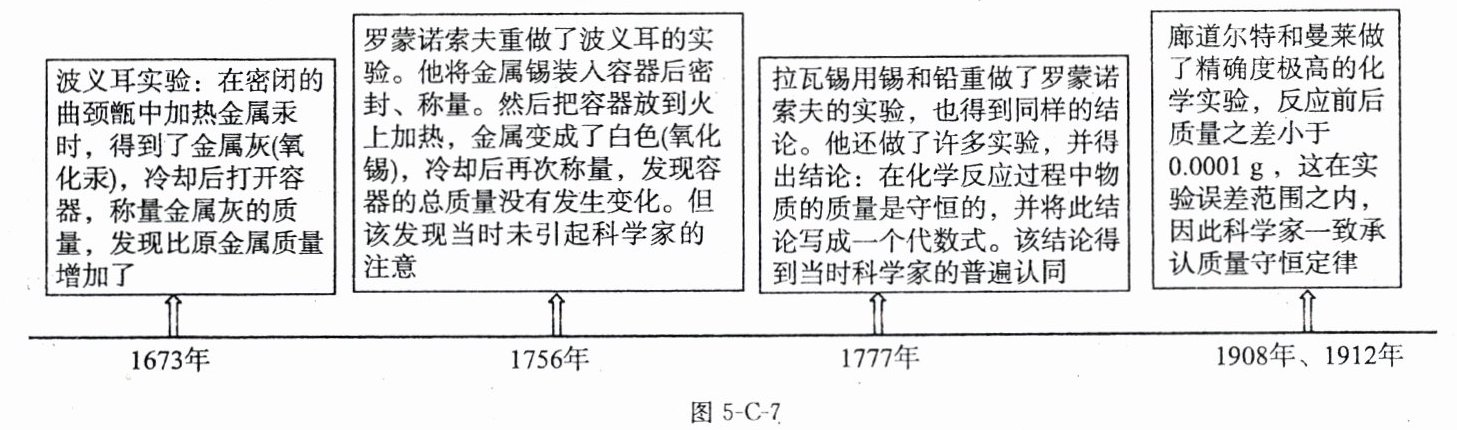
(1)波义耳实验中,金属灰增加的质量是
(2)质量守恒定律的发现过程,带给我们的启示有
A. 要善于总结前人的成果和经验 B. 实验的成功与否,取决于试剂的选择
C. 定量研究的方法是科学研究的重要方法
受上述研究启发,小丽对相关实验进行了深入探究。
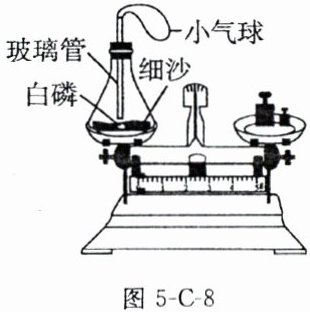
(3)在测定白磷燃烧前后质量的实验中(如图5-C-8),小气球的作用有
(4)小丽认为,蜡烛燃烧后剩余的固体质量比燃烧前少了,因此该反应不符合质量守恒定律。请你设计一个能纠正小丽的简明实验思路:

(1)波义耳实验中,金属灰增加的质量是
参加反应的氧气质量(或氧化汞中氧元素的质量)
。 (2)质量守恒定律的发现过程,带给我们的启示有
AC
(填字母)。 A. 要善于总结前人的成果和经验 B. 实验的成功与否,取决于试剂的选择
C. 定量研究的方法是科学研究的重要方法
受上述研究启发,小丽对相关实验进行了深入探究。
(3)在测定白磷燃烧前后质量的实验中(如图5-C-8),小气球的作用有
形成密闭装置,同时平衡装置内外气压,防止橡皮塞被冲出(合理即可)
;锥形瓶底部铺有一层细沙,其作用是防止锥形瓶因受热不均而炸裂
。 
(4)小丽认为,蜡烛燃烧后剩余的固体质量比燃烧前少了,因此该反应不符合质量守恒定律。请你设计一个能纠正小丽的简明实验思路:
在密闭装置中完成蜡烛燃烧实验,并测量蜡烛燃烧前后整个装置的质量,比较两者的质量大小(合理即可)
。
答案:
(1)参加反应的氧气质量(或氧化汞中氧元素的质量)
(2)AC
(3)形成密闭装置,同时平衡装置内外气压,防止橡皮塞被冲出(合理即可) 防止锥形瓶因受热不均而炸裂
(4)在密闭装置中完成蜡烛燃烧实验,并测量蜡烛燃烧前后整个装置的质量,比较两者的质量大小(合理即可)
(1)参加反应的氧气质量(或氧化汞中氧元素的质量)
(2)AC
(3)形成密闭装置,同时平衡装置内外气压,防止橡皮塞被冲出(合理即可) 防止锥形瓶因受热不均而炸裂
(4)在密闭装置中完成蜡烛燃烧实验,并测量蜡烛燃烧前后整个装置的质量,比较两者的质量大小(合理即可)
查看更多完整答案,请扫码查看


