22. (6分)【证据推理】兴趣小组追寻科学家的足迹,对水进行探究。
[宏观辨识] 根据实验探究水的组成。
(1)水的合成:在密闭容器中将氢气和氧气的混合气体点燃,根据容器内生成的小水珠可知,水是由
(2)水的分解:电解水一段时间后(如图3-C-11),观察到管a和管b中气体体积比约为

[证据推理] 结合实验现象推算水分子中氢、氧原子个数比。
方法一:根据相同条件下气体的体积比等于其分子的个数比,得出电解水的产物中氢、氧分子个数比为
方法二:已知电解水实验中氢气和氧气的体积比和正、负极产生气体的
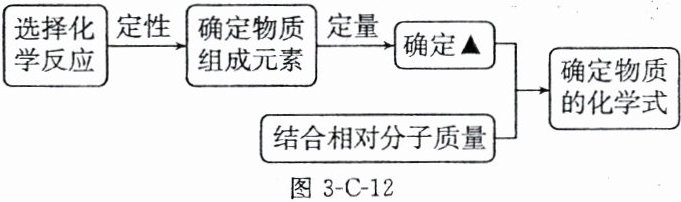
[模型构建] 以分子构成的物质为例,图中“▲”表示的是
[宏观辨识] 根据实验探究水的组成。
(1)水的合成:在密闭容器中将氢气和氧气的混合气体点燃,根据容器内生成的小水珠可知,水是由
氢元素和氧元素
组成的化合物。 (2)水的分解:电解水一段时间后(如图3-C-11),观察到管a和管b中气体体积比约为
2∶1
,经检验管a中的气体是H₂
(填化学式)。 
[证据推理] 结合实验现象推算水分子中氢、氧原子个数比。
方法一:根据相同条件下气体的体积比等于其分子的个数比,得出电解水的产物中氢、氧分子个数比为
2∶1
,进而推算出结果。 方法二:已知电解水实验中氢气和氧气的体积比和正、负极产生气体的
密度
,可计算出水中各元素的质量比,结合氢、氧原子的相对原子质量,可进一步推算出结果。 [模型构建] 以分子构成的物质为例,图中“▲”表示的是
各元素的原子个数比
。
答案:
[宏观辨识](1)氢元素和氧元素 (2)2∶1 H₂ [证据推理]2∶1 密度 [模型构建]各元素的原子个数比
23. 有100 g溶质质量分数为10%的食盐溶液,要使其溶质质量分数变为20%,有以下三种方法,请你进行计算。(写出计算过程)
(1)可加入多少克食盐?
(2)可蒸发多少克水?
(3)将其与溶质质量分数为25%的食盐溶液混合,需要25%的食盐溶液多少克?
(1)可加入多少克食盐?
(2)可蒸发多少克水?
(3)将其与溶质质量分数为25%的食盐溶液混合,需要25%的食盐溶液多少克?
答案:
解:
(1)设可加入食盐的质量为x。$\frac{100\ g×10\%+x}{100\ g+x}×100\%=20\%$ $x=12.5\ g$
(2)设可蒸发水的质量为y。$100\ g×10\%=(100\ g-y)×20\%$ $y=50\ g$
(3)设需要25%的食盐溶液的质量为z。$100\ g×10\%+z×25\%=(100\ g+z)×20\%$ $z=200\ g$ 答:
(1)可加入12.5 g食盐;
(2)可蒸发50 g水;
(3)需要25%的食盐溶液200 g。
(1)设可加入食盐的质量为x。$\frac{100\ g×10\%+x}{100\ g+x}×100\%=20\%$ $x=12.5\ g$
(2)设可蒸发水的质量为y。$100\ g×10\%=(100\ g-y)×20\%$ $y=50\ g$
(3)设需要25%的食盐溶液的质量为z。$100\ g×10\%+z×25\%=(100\ g+z)×20\%$ $z=200\ g$ 答:
(1)可加入12.5 g食盐;
(2)可蒸发50 g水;
(3)需要25%的食盐溶液200 g。
查看更多完整答案,请扫码查看


