第20页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
3. (2023·鄂州)下列物质中,属于纯净物的是 (
A.水泥砂浆
B.液态氧
C.洁净的空气
D.汽水
B
)A.水泥砂浆
B.液态氧
C.洁净的空气
D.汽水
答案:
B
4. 测定空气组成实验是化学史上的经典实验,汞用作反应试剂有很多优点。下列关于该实验的说法错误的是 (
A.汞在常温下呈液态,在该实验中既可以隔绝外界空气,还可以通过连通器直接用于测量反应器(曲颈甑)内空间体积的变化
B.汞和氧气反应的速率非常缓慢,便于实验者观察实验现象
C.汞的沸点为$356.6^{\circ}C$,在加热时源源不断汽化的汞可以将空气中的氧气完全耗尽
D.反应生成的氧化汞在这个温度下呈固态,且不溶于汞。又因为密度小于液态汞,所以浮在汞的液面上,很容易分离
B
)A.汞在常温下呈液态,在该实验中既可以隔绝外界空气,还可以通过连通器直接用于测量反应器(曲颈甑)内空间体积的变化
B.汞和氧气反应的速率非常缓慢,便于实验者观察实验现象
C.汞的沸点为$356.6^{\circ}C$,在加热时源源不断汽化的汞可以将空气中的氧气完全耗尽
D.反应生成的氧化汞在这个温度下呈固态,且不溶于汞。又因为密度小于液态汞,所以浮在汞的液面上,很容易分离
答案:
B
5. 某同学设计了测定空气中氧气含量的实验。
(一)利用图1装置进行实验
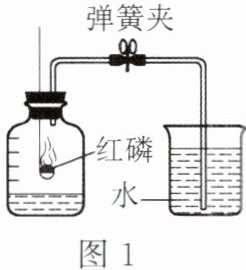
该同学的实验步骤如下:
①将图中集气瓶中水面上方空间分为5等份,并做好标记;
②在带橡胶塞和导管的燃烧匙内装入足量的红磷,将乳胶管上的弹簧夹夹紧,在酒精灯上点燃红磷,立即伸入集气瓶内,并塞紧橡胶塞;
③充分反应后,待集气瓶冷却至室温,打开弹簧夹。
(1)该实验中红磷须足量或者过量,目的是
(2)红磷燃烧的文字表达式为
(3)根据步骤③中打开弹簧夹后观察到的现象可得出空气中氧气约占空气体积的
(4)若实验时没有用弹簧夹夹紧乳胶管,在红磷燃烧时,会观察到烧杯中导管口有气泡冒出,产生这一现象的原因是
(二)为了帮助同学们更好地理解测定空气中氧气含量的实验原理,老师利用传感器技术定时测定了实验过程中实验装置(如图2所示)内的气体压强、温度和氧气浓度的变化趋势(如图3所示)。
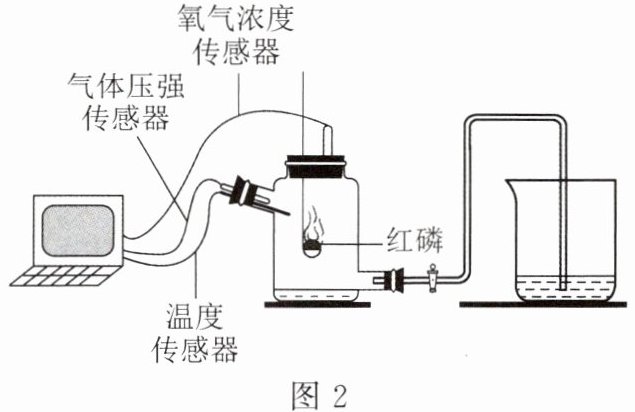
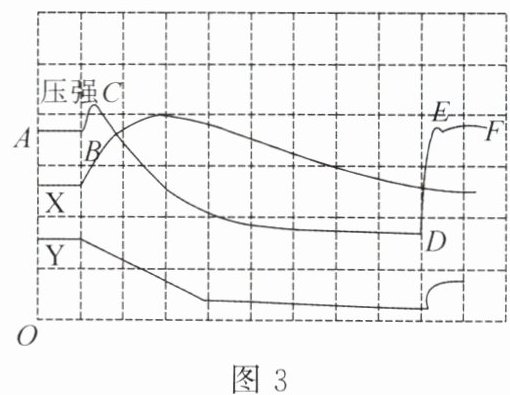
(5)表示温度变化的是曲线
(6)根据图3中压强曲线可知,CD段压强减小的原因是
(7)根据图3可知,红磷燃烧
(一)利用图1装置进行实验

该同学的实验步骤如下:
①将图中集气瓶中水面上方空间分为5等份,并做好标记;
②在带橡胶塞和导管的燃烧匙内装入足量的红磷,将乳胶管上的弹簧夹夹紧,在酒精灯上点燃红磷,立即伸入集气瓶内,并塞紧橡胶塞;
③充分反应后,待集气瓶冷却至室温,打开弹簧夹。
(1)该实验中红磷须足量或者过量,目的是
将集气瓶内空气中的氧气消耗完全
。(2)红磷燃烧的文字表达式为
红磷+氧气$\xrightarrow{\text{点燃}}$五氧化二磷
,步骤②中集气瓶内观察到的现象是红磷燃烧,发光放热,产生大量白烟
。(3)根据步骤③中打开弹簧夹后观察到的现象可得出空气中氧气约占空气体积的
$\frac{1}{5}$
。(4)若实验时没有用弹簧夹夹紧乳胶管,在红磷燃烧时,会观察到烧杯中导管口有气泡冒出,产生这一现象的原因是
红磷燃烧放出热量,瓶内气体受热膨胀,压强增大,使气体从导管口逸出
,会导致最终测得的氧气含量偏大
(选填“偏大”或“偏小”)。(二)为了帮助同学们更好地理解测定空气中氧气含量的实验原理,老师利用传感器技术定时测定了实验过程中实验装置(如图2所示)内的气体压强、温度和氧气浓度的变化趋势(如图3所示)。


(5)表示温度变化的是曲线
X
(选填“X”或“Y”)。(6)根据图3中压强曲线可知,CD段压强减小的原因是
氧气被消耗和装置内的温度降低
。(7)根据图3可知,红磷燃烧
不能
(选填“能”或“不能”)将瓶内空气中的氧气完全消耗。
答案:
(1)将集气瓶内空气中的氧气消耗完全 (2)红磷+氧气$\xrightarrow{\text{点燃}}$五氧化二磷 红磷燃烧,发光放热,产生大量白烟 (3)$\frac{1}{5}$ (4)红磷燃烧放出热量,瓶内气体受热膨胀,压强增大,使气体从导管口逸出 偏大 (5)X (6)氧气被消耗和装置内的温度降低 (7)不能
查看更多完整答案,请扫码查看


