2025年暑假Happy假日八年级化学人教版五四制
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假Happy假日八年级化学人教版五四制 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第77页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
22. 为测定某盐酸的溶质质量分数,取200g样品于烧杯中,将50g碳酸钠溶液分为5等份,分5次加入盛有样品的烧杯中。测出每次反应后溶液的总质量,实验数据如下表所示。(提示:①盐酸的溶质为氯化氢;②反应的化学方程式为$2HCl + Na_{2}CO_{3} = 2NaCl + H_{2}O + CO_{2} \uparrow$)
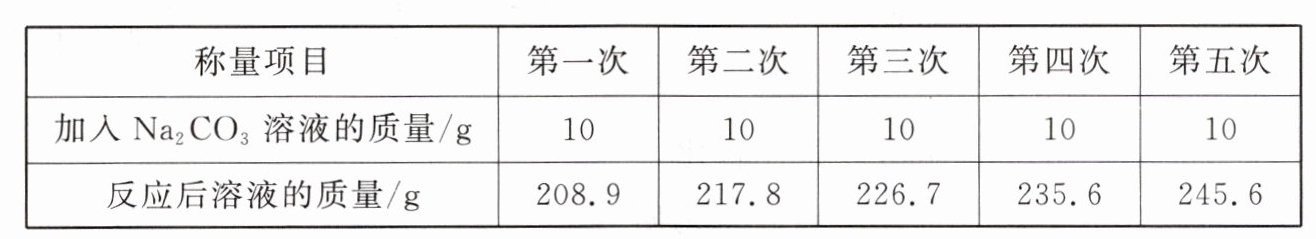
请根据实验数据计算200g盐酸中氯化氢的质量。(写出计算过程)
解:根据质量守恒定律,第一次加入10g碳酸钠溶液时,生成二氧化碳的质量为200g + 10g - 209.56g = 0.44g;
第二次加入10g碳酸钠溶液时,生成二氧化碳的质量为(209.56g + 10g) - 219.12g = 0.44g;
第三次加入10g碳酸钠溶液时,生成二氧化碳的质量为(219.12g + 10g) - 228.68g = 0.44g;
第四次加入10g碳酸钠溶液时,生成二氧化碳的质量为(228.68g + 10g) - 238.24g = 0.44g;
第五次加入10g碳酸钠溶液时,生成二氧化碳的质量为(238.24g + 10g) - 248.24g = 0g,说明第四次加入碳酸钠溶液后盐酸已完全反应。
则总共生成二氧化碳的质量为0.44g×4 = 1.76g。
设200g盐酸中氯化氢的质量为x。
$2HCl + Na_{2}CO_{3} = 2NaCl + H_{2}O + CO_{2} \uparrow$
73 44
x 1.76g
$\frac{73}{44}=\frac{x}{1.76g}$
$x=\frac{73×1.76g}{44}=$
答:200g盐酸中氯化氢的质量为

请根据实验数据计算200g盐酸中氯化氢的质量。(写出计算过程)
解:根据质量守恒定律,第一次加入10g碳酸钠溶液时,生成二氧化碳的质量为200g + 10g - 209.56g = 0.44g;
第二次加入10g碳酸钠溶液时,生成二氧化碳的质量为(209.56g + 10g) - 219.12g = 0.44g;
第三次加入10g碳酸钠溶液时,生成二氧化碳的质量为(219.12g + 10g) - 228.68g = 0.44g;
第四次加入10g碳酸钠溶液时,生成二氧化碳的质量为(228.68g + 10g) - 238.24g = 0.44g;
第五次加入10g碳酸钠溶液时,生成二氧化碳的质量为(238.24g + 10g) - 248.24g = 0g,说明第四次加入碳酸钠溶液后盐酸已完全反应。
则总共生成二氧化碳的质量为0.44g×4 = 1.76g。
设200g盐酸中氯化氢的质量为x。
$2HCl + Na_{2}CO_{3} = 2NaCl + H_{2}O + CO_{2} \uparrow$
73 44
x 1.76g
$\frac{73}{44}=\frac{x}{1.76g}$
$x=\frac{73×1.76g}{44}=$
2.92g
。答:200g盐酸中氯化氢的质量为
2.92g
。
答案:
【解析】:
根据质量守恒定律,第一次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$200g + 10g - 209.56g = 0.44g$;
第二次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(209.56g + 10g) - 219.12g = 0.44g$;
第三次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(219.12g + 10g) - 228.68g = 0.44g$;
第四次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(228.68g + 10g) - 238.24g = 0.44g$;
第五次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(238.24g + 10g) - 248.24g = 0g$,说明第四次加入碳酸钠溶液后盐酸已完全反应。
则总共生成二氧化碳的质量为$0.44g\times4 = 1.76g$。
设$200g$盐酸中氯化氢的质量为$x$。
$2HCl + Na_{2}CO_{3} = 2NaCl + H_{2}O + CO_{2} \uparrow$
$73$ $44$
$x$ $1.76g$
$\frac{73}{44}=\frac{x}{1.76g}$
$x=\frac{73\times1.76g}{44}=2.92g$。
【答案】:$2.92g$
根据质量守恒定律,第一次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$200g + 10g - 209.56g = 0.44g$;
第二次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(209.56g + 10g) - 219.12g = 0.44g$;
第三次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(219.12g + 10g) - 228.68g = 0.44g$;
第四次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(228.68g + 10g) - 238.24g = 0.44g$;
第五次加入$10g$碳酸钠溶液时,生成二氧化碳的质量为$(238.24g + 10g) - 248.24g = 0g$,说明第四次加入碳酸钠溶液后盐酸已完全反应。
则总共生成二氧化碳的质量为$0.44g\times4 = 1.76g$。
设$200g$盐酸中氯化氢的质量为$x$。
$2HCl + Na_{2}CO_{3} = 2NaCl + H_{2}O + CO_{2} \uparrow$
$73$ $44$
$x$ $1.76g$
$\frac{73}{44}=\frac{x}{1.76g}$
$x=\frac{73\times1.76g}{44}=2.92g$。
【答案】:$2.92g$
查看更多完整答案,请扫码查看


