2025年暑假Happy假日八年级化学人教版五四制
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假Happy假日八年级化学人教版五四制 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第105页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
21. 某化学小组围绕燃烧的主题开展了相关活动,请你参与完成。
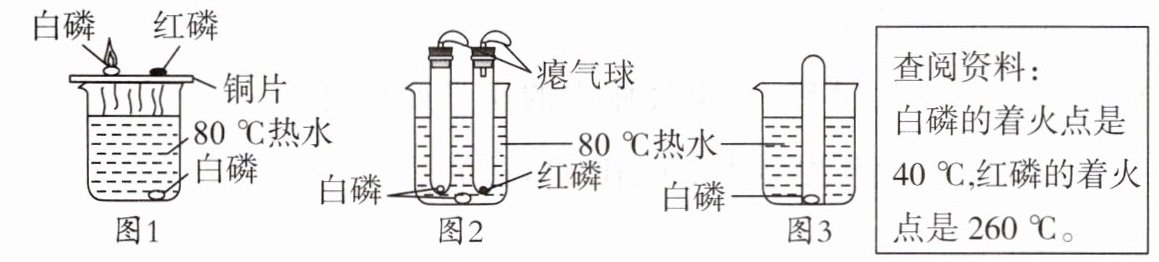
【知识回忆】可燃物燃烧的必备条件是
【交流讨论】
(1)改进后的装置(图2)与图1相比,其优点是
(2)将装有空气的大试管口朝下垂直插入水中,使试管罩住白磷(如图3所示),结果观察到了“水火相容”的奇观,则大试管内出现的现象是

【知识回忆】可燃物燃烧的必备条件是
与氧气(或空气)接触
和温度达到可燃物的着火点
。【交流讨论】
(1)改进后的装置(图2)与图1相比,其优点是
减少污染(环保)
。欲使图2中的红磷燃烧,可将试管从水中取出并擦干
后再对试管加热。(2)将装有空气的大试管口朝下垂直插入水中,使试管罩住白磷(如图3所示),结果观察到了“水火相容”的奇观,则大试管内出现的现象是
白磷燃烧,产生白烟,试管内液面上升
。
答案:
【解析】:
- 知识回忆:根据燃烧条件分析。
- 交流讨论(1):对比图1和图2装置特点,考虑环保和实验操作;从试管有水影响加热角度分析。
- 交流讨论(2):依据白磷燃烧现象和消耗氧气使气压变化分析。
- 实验1:根据实验目的和生石灰与水反应放热分析。
- 白磷燃烧:根据反应原理写方程式。
- 氧气体积分数:按提供数据计算。
- 压强变化:分析白磷燃烧过程中温度和氧气消耗对压强影响;从水的作用(降温、吸收产物、液封等)分析集气瓶装水目的。
【答案】:
- 与氧气(或空气)接触;温度达到可燃物的着火点
- (1)减少污染(环保);擦干
- (2)白磷燃烧,产生白烟,试管内液面上升
- (1)向烧杯中加入适量的水;${CaO + H_{2}O = Ca(OH)_{2}}$
- (2)${4P + 5O_{2}\xlongequal {点燃} 2P_{2}O_{5}}$
- (3)$\frac{60mL}{350mL - 50mL}×100\% = 20\%$
- (4)先变大,再变小,又恢复至常压;吸收白烟,同时防止集气瓶内空气因瓶内温度升高、压强增大而逸散到瓶外
- 知识回忆:根据燃烧条件分析。
- 交流讨论(1):对比图1和图2装置特点,考虑环保和实验操作;从试管有水影响加热角度分析。
- 交流讨论(2):依据白磷燃烧现象和消耗氧气使气压变化分析。
- 实验1:根据实验目的和生石灰与水反应放热分析。
- 白磷燃烧:根据反应原理写方程式。
- 氧气体积分数:按提供数据计算。
- 压强变化:分析白磷燃烧过程中温度和氧气消耗对压强影响;从水的作用(降温、吸收产物、液封等)分析集气瓶装水目的。
【答案】:
- 与氧气(或空气)接触;温度达到可燃物的着火点
- (1)减少污染(环保);擦干
- (2)白磷燃烧,产生白烟,试管内液面上升
- (1)向烧杯中加入适量的水;${CaO + H_{2}O = Ca(OH)_{2}}$
- (2)${4P + 5O_{2}\xlongequal {点燃} 2P_{2}O_{5}}$
- (3)$\frac{60mL}{350mL - 50mL}×100\% = 20\%$
- (4)先变大,再变小,又恢复至常压;吸收白烟,同时防止集气瓶内空气因瓶内温度升高、压强增大而逸散到瓶外
22. 小明同学设计以下实验来探究可燃物燃烧的条件和测定空气中氧气的含量(已知:白磷的着火点是40℃,红磷的着火点是260℃)。
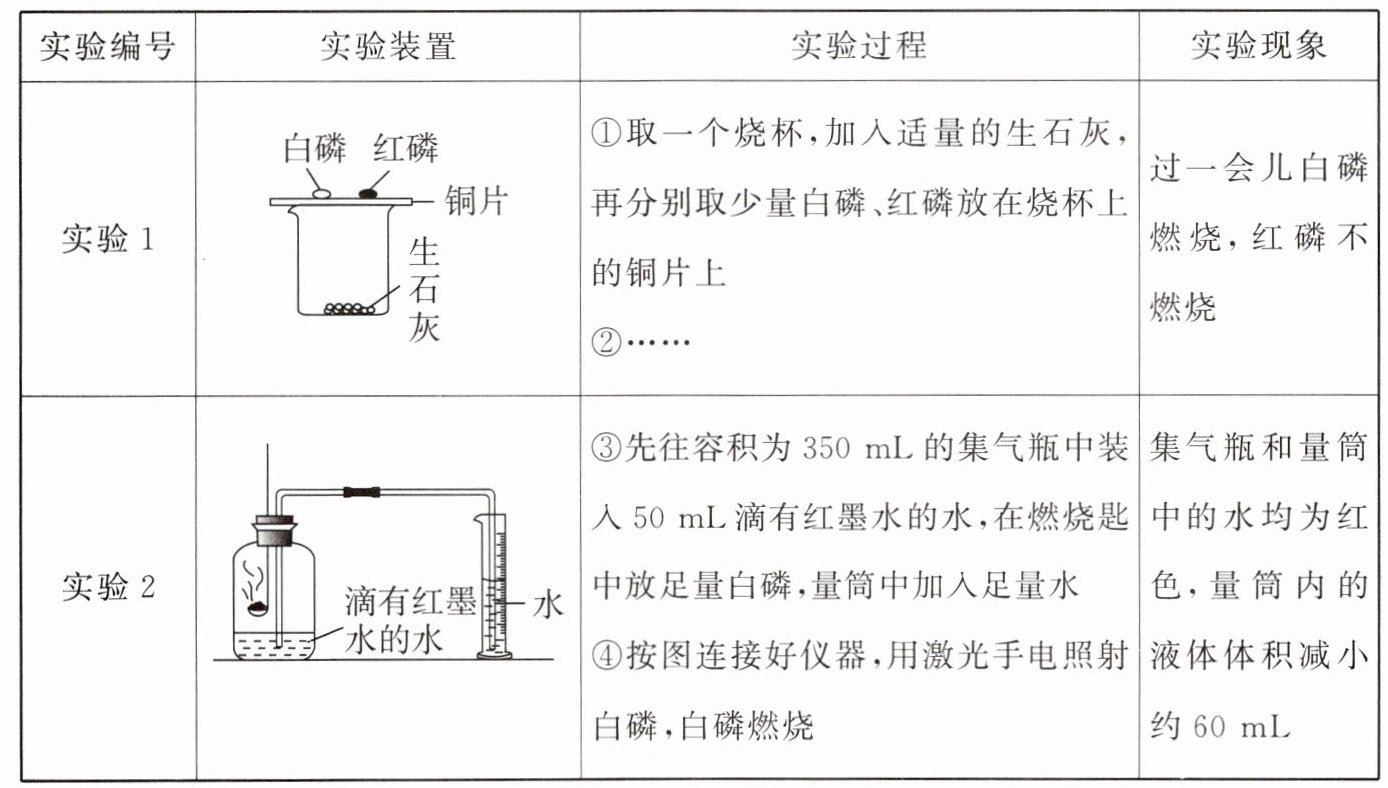
(1)补充实验过程②:
(2)白磷燃烧的化学方程式为
(3)根据实验2的结果,计算空气中氧气的体积分数:
(4)在整个实验2的过程中,集气瓶内的压强变化是

(1)补充实验过程②:
向烧杯中加入适量的水
,烧杯中发生反应的化学方程式为CaO + H₂O=Ca(OH)₂
。(2)白磷燃烧的化学方程式为
4P + 5O₂$\stackrel{点燃}{=\!=\!=}$2P₂O₅
。(3)根据实验2的结果,计算空气中氧气的体积分数:
$\frac{60mL}{350mL - 50mL}×100\% = 20\%$
(写出算式和结果)。(4)在整个实验2的过程中,集气瓶内的压强变化是
先增大后减小
,集气瓶中预先装入50mL水,目的是吸收白磷燃烧生成的五氧化二磷,防止污染空气,同时降低温度,吸收热量
。
答案:
【解析】:
(1) 要探究可燃物燃烧的条件,根据实验现象过一会儿白磷燃烧,红磷不燃烧,说明要提供热量使温度达到白磷的着火点,所以补充的实验过程②为:向烧杯中加入适量的水。生石灰是氧化钙,与水反应生成氢氧化钙,化学方程式为$CaO + H_{2}O=Ca(OH)_{2}$,该反应放出大量的热,使温度达到白磷的着火点。
(2) 白磷燃烧生成五氧化二磷,化学方程式为$4P + 5O_{2}\stackrel{点燃}{=\!=\!=}2P_{2}O_{5}$。
(3) 集气瓶的容积为$350mL$,其中预先装入$50mL$水,则空气的体积为$350mL - 50mL = 300mL$,量筒内的液体体积减小约$60mL$,说明消耗氧气的体积约为$60mL$,则空气中氧气的体积分数为$\frac{60mL}{350mL - 50mL}\times100\%=\frac{60mL}{300mL}\times100\% = 20\%$。
(4) 白磷燃烧放出大量的热,使集气瓶内温度升高,压强增大;随着反应的进行,氧气被消耗,集气瓶内压强逐渐减小,所以集气瓶内的压强变化是先增大后减小。集气瓶中预先装入$50mL$水,目的是吸收白磷燃烧生成的五氧化二磷,防止污染空气,同时还能降低温度,吸收热量。
【答案】:
(1) 向烧杯中加入适量的水;$CaO + H_{2}O=Ca(OH)_{2}$
(2) $4P + 5O_{2}\stackrel{点燃}{=\!=\!=}2P_{2}O_{5}$
(3) $\frac{60mL}{350mL - 50mL}\times100\% = 20\%$
(4) 先增大后减小;吸收白磷燃烧生成的五氧化二磷,防止污染空气,同时降低温度,吸收热量
(1) 要探究可燃物燃烧的条件,根据实验现象过一会儿白磷燃烧,红磷不燃烧,说明要提供热量使温度达到白磷的着火点,所以补充的实验过程②为:向烧杯中加入适量的水。生石灰是氧化钙,与水反应生成氢氧化钙,化学方程式为$CaO + H_{2}O=Ca(OH)_{2}$,该反应放出大量的热,使温度达到白磷的着火点。
(2) 白磷燃烧生成五氧化二磷,化学方程式为$4P + 5O_{2}\stackrel{点燃}{=\!=\!=}2P_{2}O_{5}$。
(3) 集气瓶的容积为$350mL$,其中预先装入$50mL$水,则空气的体积为$350mL - 50mL = 300mL$,量筒内的液体体积减小约$60mL$,说明消耗氧气的体积约为$60mL$,则空气中氧气的体积分数为$\frac{60mL}{350mL - 50mL}\times100\%=\frac{60mL}{300mL}\times100\% = 20\%$。
(4) 白磷燃烧放出大量的热,使集气瓶内温度升高,压强增大;随着反应的进行,氧气被消耗,集气瓶内压强逐渐减小,所以集气瓶内的压强变化是先增大后减小。集气瓶中预先装入$50mL$水,目的是吸收白磷燃烧生成的五氧化二磷,防止污染空气,同时还能降低温度,吸收热量。
【答案】:
(1) 向烧杯中加入适量的水;$CaO + H_{2}O=Ca(OH)_{2}$
(2) $4P + 5O_{2}\stackrel{点燃}{=\!=\!=}2P_{2}O_{5}$
(3) $\frac{60mL}{350mL - 50mL}\times100\% = 20\%$
(4) 先增大后减小;吸收白磷燃烧生成的五氧化二磷,防止污染空气,同时降低温度,吸收热量
查看更多完整答案,请扫码查看


