2025年暑假Happy假日八年级化学人教版五四制
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假Happy假日八年级化学人教版五四制 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第10页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
11. 高铁酸钾($K_{2}FeO_{4}$)常用于废水处理,可通过下列反应制得:$2FeS{O}_{4}+6N{a}_{2}{O}_{2}\xlongequal{\;\;}2N{a}_{2}Fe{O}_{4}+2N{a}_{2}S{O}_{4}+2X+{O}_{2}\uparrow$;$N{a}_{2}Fe{O}_{4}+2KOH\xlongequal{\;\;}{K}_{2}Fe{O}_{4}+2NaOH$。根据质量守恒定律可推测X是 (
A. $SO_{2}$
B. $SO_{3}$
C. $Na_{2}O$
D. $Fe_{2}(SO_{4})_{3}$
C
)A. $SO_{2}$
B. $SO_{3}$
C. $Na_{2}O$
D. $Fe_{2}(SO_{4})_{3}$
答案:
C
12. 我国古代将炉甘石($ZnCO_{3}$)、赤铜和木炭粉混合后加热到约$800^{\circ }C$,有如下反应发生:①$ZnC{O}_{3}\overset{高温}{\xlongequal{\;\;}}ZnO+C{O}_{2}\uparrow$②$C+2ZnO\overset{高温}{\xlongequal{\;\;}}2Zn+X\uparrow$。
下列有关说法错误的是 (
A. X的化学式为$CO_{2}$
B. 反应前后锌元素的质量不变
C. ②反应中$ZnO$发生了还原反应
D. ②反应前后锌元素化合价升高
下列有关说法错误的是 (
D
)A. X的化学式为$CO_{2}$
B. 反应前后锌元素的质量不变
C. ②反应中$ZnO$发生了还原反应
D. ②反应前后锌元素化合价升高
答案:
D
13. 随着人类对能源的需求量日益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注。我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
(1)可燃冰主要含甲烷水合物,甲烷($CH_{4}$)完全燃烧的化学方程式为
(2)氢气不便于储存,可将其转化为固态氢化物(如氢化钠等)。氢化钠($NaH$)与水反应生成氢氧化钠和氢气,该反应的化学方程式为
(1)可燃冰主要含甲烷水合物,甲烷($CH_{4}$)完全燃烧的化学方程式为
$CH_{4}+2O_{2}\stackrel{点燃}{=\!=\!=}CO_{2}+2H_{2}O$
。(2)氢气不便于储存,可将其转化为固态氢化物(如氢化钠等)。氢化钠($NaH$)与水反应生成氢氧化钠和氢气,该反应的化学方程式为
$NaH + H_{2}O = NaOH + H_{2}\uparrow$
。
答案:
【解析】:
(1)甲烷($CH_{4}$)完全燃烧生成二氧化碳和水,化学方程式为$CH_{4}+2O_{2}\stackrel{点燃}{=\!=\!=}CO_{2}+2H_{2}O$。
(2)氢化钠($NaH$)与水反应生成氢氧化钠和氢气,化学方程式为$NaH + H_{2}O = NaOH + H_{2}\uparrow$。
【答案】:
(1)$CH_{4}+2O_{2}\stackrel{点燃}{=\!=\!=}CO_{2}+2H_{2}O$;
(2)$NaH + H_{2}O = NaOH + H_{2}\uparrow$
(1)甲烷($CH_{4}$)完全燃烧生成二氧化碳和水,化学方程式为$CH_{4}+2O_{2}\stackrel{点燃}{=\!=\!=}CO_{2}+2H_{2}O$。
(2)氢化钠($NaH$)与水反应生成氢氧化钠和氢气,化学方程式为$NaH + H_{2}O = NaOH + H_{2}\uparrow$。
【答案】:
(1)$CH_{4}+2O_{2}\stackrel{点燃}{=\!=\!=}CO_{2}+2H_{2}O$;
(2)$NaH + H_{2}O = NaOH + H_{2}\uparrow$
14. 氟及其化合物常被用于原子弹制造、航天工业等领域。氟气($F_{2}$)的化学性质极其活泼,水能在氟气中燃烧,燃烧产物之一是氧气。

(1)图1是水与氟气反应的微观示意图。图1方框内应填图2中的
(2)分析微观示意图可知,化学反应中发生变化的粒子是

(1)图1是水与氟气反应的微观示意图。图1方框内应填图2中的
B
。写出该反应的化学方程式:2H₂O + 2F₂=4HF + O₂
。(2)分析微观示意图可知,化学反应中发生变化的粒子是
分子
,未发生变化的粒子是原子
。
答案:
【解析】:
(1)根据质量守恒定律,化学反应前后原子的种类和数目不变。反应前有$2$个$H$、$2$个$O$、$2$个$F$,反应后已知有$2$个$H$、$2$个$F$,还缺少$2$个$O$,所以方框内应填$B$($1$个氧分子)。化学方程式为$2H_{2}O + 2F_{2}=4HF + O_{2}$。
(2)从微观示意图可以看出,化学反应中发生变化的粒子是分子(水分子和氟分子发生了变化),未发生变化的粒子是原子(氢原子、氧原子、氟原子种类和数目不变)。
【答案】:
(1)$B$;$\boldsymbol{2H_{2}O + 2F_{2}=4HF + O_{2}}$
(2)分子;原子
(1)根据质量守恒定律,化学反应前后原子的种类和数目不变。反应前有$2$个$H$、$2$个$O$、$2$个$F$,反应后已知有$2$个$H$、$2$个$F$,还缺少$2$个$O$,所以方框内应填$B$($1$个氧分子)。化学方程式为$2H_{2}O + 2F_{2}=4HF + O_{2}$。
(2)从微观示意图可以看出,化学反应中发生变化的粒子是分子(水分子和氟分子发生了变化),未发生变化的粒子是原子(氢原子、氧原子、氟原子种类和数目不变)。
【答案】:
(1)$B$;$\boldsymbol{2H_{2}O + 2F_{2}=4HF + O_{2}}$
(2)分子;原子
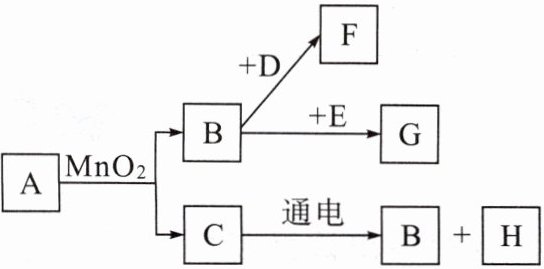
15. A、B、C、D、E、F、G是初中常见的7种物质,它们的转化关系如图。
已知A、C是无色液体,B、G、H是无色气体,E在纯净的B中燃烧产生蓝紫色火焰,D在纯净的B中燃烧火星四射。
(1)请写出下列化学反应的化学方程式:
①$B+D\to F$
②$A\to B+C$
(2)D、E在纯净的B中燃烧都要加少量的水。其中E在纯净的B中燃烧要加少量的水,其目的是
已知A、C是无色液体,B、G、H是无色气体,E在纯净的B中燃烧产生蓝紫色火焰,D在纯净的B中燃烧火星四射。
(1)请写出下列化学反应的化学方程式:
①$B+D\to F$
$3Fe + 2O_{2}\stackrel{点燃}{=\!=\!=}Fe_{3}O_{4}$
。②$A\to B+C$
$2H_{2}O_{2}\stackrel{MnO_{2}}{=\!=\!=}2H_{2}O + O_{2}\uparrow$
,该反应的基本类型是分解反应
。(2)D、E在纯净的B中燃烧都要加少量的水。其中E在纯净的B中燃烧要加少量的水,其目的是
吸收二氧化硫,防止污染空气
。
答案:
【解析】:
- ①根据已知条件,$B$是氧气$(O_{2})$,$D$是铁$(Fe)$,铁在氧气中燃烧生成四氧化三铁$(Fe_{3}O_{4})$,化学方程式为$3Fe + 2O_{2}\stackrel{点燃}{=\!=\!=}Fe_{3}O_{4}$。
- ②$A$是过氧化氢$(H_{2}O_{2})$,在二氧化锰催化作用下分解生成水$(H_{2}O)$和氧气$(O_{2})$,化学方程式为$2H_{2}O_{2}\stackrel{MnO_{2}}{=\!=\!=}2H_{2}O + O_{2}\uparrow$,该反应是一种物质生成两种物质,基本类型是分解反应。
- $E$是硫$(S)$,硫在氧气中燃烧生成二氧化硫$(SO_{2})$,加少量水目的是吸收二氧化硫,防止污染空气。
【答案】:
- ①$3Fe + 2O_{2}\stackrel{点燃}{=\!=\!=}Fe_{3}O_{4}$
- ②$2H_{2}O_{2}\stackrel{MnO_{2}}{=\!=\!=}2H_{2}O + O_{2}\uparrow$;分解反应
- 吸收二氧化硫,防止污染空气
- ①根据已知条件,$B$是氧气$(O_{2})$,$D$是铁$(Fe)$,铁在氧气中燃烧生成四氧化三铁$(Fe_{3}O_{4})$,化学方程式为$3Fe + 2O_{2}\stackrel{点燃}{=\!=\!=}Fe_{3}O_{4}$。
- ②$A$是过氧化氢$(H_{2}O_{2})$,在二氧化锰催化作用下分解生成水$(H_{2}O)$和氧气$(O_{2})$,化学方程式为$2H_{2}O_{2}\stackrel{MnO_{2}}{=\!=\!=}2H_{2}O + O_{2}\uparrow$,该反应是一种物质生成两种物质,基本类型是分解反应。
- $E$是硫$(S)$,硫在氧气中燃烧生成二氧化硫$(SO_{2})$,加少量水目的是吸收二氧化硫,防止污染空气。
【答案】:
- ①$3Fe + 2O_{2}\stackrel{点燃}{=\!=\!=}Fe_{3}O_{4}$
- ②$2H_{2}O_{2}\stackrel{MnO_{2}}{=\!=\!=}2H_{2}O + O_{2}\uparrow$;分解反应
- 吸收二氧化硫,防止污染空气
查看更多完整答案,请扫码查看


