第56页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
实验活动8 常见酸、碱的化学性质
实验报告
【实验目的】
1. 加深对酸和碱的主要性质的认识。
2. 通过实验解释生活中的一些现象。
【实验用品】
1. 器材:白色点滴板、试管、镊子、蒸发皿、坩埚钳、玻璃棒、药匙、酒精灯、铁架台(带铁圈)、胶头滴管、火柴等。
2. 试剂:稀盐酸、稀硫酸、氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。
【实验步骤】

1. 酸、碱与指示剂的作用
(1) 现象

(2) 结论
① 酸能使石蕊溶液变成____色,使酚酞溶液____。
② 碱能使石蕊溶液变成____色,使酚酞溶液变成____色。
2. 铁锈、铁钉和稀盐酸的反应

(1) ① 现象:生锈铁钉与稀盐酸反应时,铁锈慢慢____,溶液由____色慢慢变成____色。
② 发生反应的化学方程式为____。
(2) ① 现象:光亮铁钉与稀盐酸反应时,铁钉表面产生____,溶液颜色变成____色。将铁钉取出、洗净,发现铁钉质量____。
② 发生反应的化学方程式为____。
3. 硫酸铜溶液和氢氧化钠溶液反应
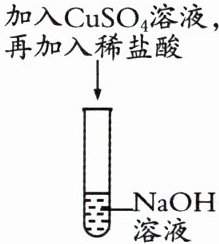
(1) 现象:将硫酸铜溶液加入氢氧化钠溶液中,有____产生,再向试管中加入稀盐酸,____。
(2) 发生反应的化学方程式:
① ____。
② ____。
4. 氢氧化钠和稀盐酸反应

(1) 现象:溶液颜色先变成____色再变成____色。蒸发皿中____。
(2) 发生反应的化学方程式为____。
5. 氢氧化钙和稀盐酸的反应

(1) 向氢氧化钙粉末中滴加水,振荡后液体浑浊,说明氢氧化钙____。
(2) 向氢氧化钙溶液中滴加酚酞溶液,溶液颜色的变化是____。
(3) 向含酚酞的氢氧化钙溶液中滴加稀盐酸,溶液颜色的变化是____。发生反应的化学方程式为____。
【交流反思】
1. 使用白色点滴板进行实验的优点是什么?
2. 将铁钉放入试管时应如何操作?
3. 中和反应的指示剂一般选择酚酞溶液,不选用紫色石蕊溶液,为什么?
4. 为什么氢氧化钠溶液和氢氧化钙溶液都能使无色的酚酞溶液变红?
5. 如何证明中和反应的发生?
实验报告
【实验目的】
1. 加深对酸和碱的主要性质的认识。
2. 通过实验解释生活中的一些现象。
【实验用品】
1. 器材:白色点滴板、试管、镊子、蒸发皿、坩埚钳、玻璃棒、药匙、酒精灯、铁架台(带铁圈)、胶头滴管、火柴等。
2. 试剂:稀盐酸、稀硫酸、氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。
【实验步骤】

1. 酸、碱与指示剂的作用
(1) 现象

(2) 结论
① 酸能使石蕊溶液变成____色,使酚酞溶液____。
② 碱能使石蕊溶液变成____色,使酚酞溶液变成____色。
2. 铁锈、铁钉和稀盐酸的反应

(1) ① 现象:生锈铁钉与稀盐酸反应时,铁锈慢慢____,溶液由____色慢慢变成____色。
② 发生反应的化学方程式为____。
(2) ① 现象:光亮铁钉与稀盐酸反应时,铁钉表面产生____,溶液颜色变成____色。将铁钉取出、洗净,发现铁钉质量____。
② 发生反应的化学方程式为____。
3. 硫酸铜溶液和氢氧化钠溶液反应

(1) 现象:将硫酸铜溶液加入氢氧化钠溶液中,有____产生,再向试管中加入稀盐酸,____。
(2) 发生反应的化学方程式:
① ____。
② ____。
4. 氢氧化钠和稀盐酸反应

(1) 现象:溶液颜色先变成____色再变成____色。蒸发皿中____。
(2) 发生反应的化学方程式为____。
5. 氢氧化钙和稀盐酸的反应

(1) 向氢氧化钙粉末中滴加水,振荡后液体浑浊,说明氢氧化钙____。
(2) 向氢氧化钙溶液中滴加酚酞溶液,溶液颜色的变化是____。
(3) 向含酚酞的氢氧化钙溶液中滴加稀盐酸,溶液颜色的变化是____。发生反应的化学方程式为____。
【交流反思】
1. 使用白色点滴板进行实验的优点是什么?
2. 将铁钉放入试管时应如何操作?
3. 中和反应的指示剂一般选择酚酞溶液,不选用紫色石蕊溶液,为什么?
4. 为什么氢氧化钠溶液和氢氧化钙溶液都能使无色的酚酞溶液变红?
5. 如何证明中和反应的发生?
答案:
(1)红 不变色 红 不变色 蓝 红 蓝 红
(2)①红 不变色 ②蓝 红
@@
(1)①消失 无 黄 ②$\mathrm{Fe}_{2}\mathrm{O}_{3}+6\mathrm{HCl}\xlongequal{\;\;}2\mathrm{FeCl}_{3}+3\mathrm{H}_{2}\mathrm{O}$
(2)①气泡 浅绿 变小 ②$\mathrm{Fe}+2\mathrm{HCl}\xlongequal{\;\;}\mathrm{FeCl}_{2}+\mathrm{H}_{2}\uparrow$
@@
(1)蓝色沉淀 蓝色沉淀逐渐溶解
(2)①$2\mathrm{NaOH}+\mathrm{CuSO}_{4}\xlongequal{\;\;}\mathrm{Cu}(\mathrm{OH})_{2}\downarrow+\mathrm{Na}_{2}\mathrm{SO}_{4}$②$\mathrm{Cu}(\mathrm{OH})_{2}+2\mathrm{HCl}\xlongequal{\;\;}\mathrm{CuCl}_{2}+2\mathrm{H}_{2}\mathrm{O}$
@@
(1)红 无 有白色固体析出
(2)$\mathrm{NaOH}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}$
@@
(1)微溶于水
(2)变红
(3)红色逐渐消失$\mathrm{Ca}(\mathrm{OH})_{2}+2\mathrm{HCl}\xlongequal{\;\;}\mathrm{CaCl}_{2}+2\mathrm{H}_{2}\mathrm{O}$
@@节约试剂,可减少对环境的污染,可同时完成多个实验,便于对比实验现象等。
@@先将试管横放,把铁钉放在试管口,然后将试管慢慢竖起。
@@紫色石蕊溶液在碱性溶液中呈蓝色,在中性溶液中呈紫色,蓝色与紫色之间没有明显的界线,不易判断反应终点。
@@因为它们解离出的阴离子都是氢氧根离子。
@@使用酸碱指示剂或pH试纸证明溶液的酸碱性发生了改变。
(1)红 不变色 红 不变色 蓝 红 蓝 红
(2)①红 不变色 ②蓝 红
@@
(1)①消失 无 黄 ②$\mathrm{Fe}_{2}\mathrm{O}_{3}+6\mathrm{HCl}\xlongequal{\;\;}2\mathrm{FeCl}_{3}+3\mathrm{H}_{2}\mathrm{O}$
(2)①气泡 浅绿 变小 ②$\mathrm{Fe}+2\mathrm{HCl}\xlongequal{\;\;}\mathrm{FeCl}_{2}+\mathrm{H}_{2}\uparrow$
@@
(1)蓝色沉淀 蓝色沉淀逐渐溶解
(2)①$2\mathrm{NaOH}+\mathrm{CuSO}_{4}\xlongequal{\;\;}\mathrm{Cu}(\mathrm{OH})_{2}\downarrow+\mathrm{Na}_{2}\mathrm{SO}_{4}$②$\mathrm{Cu}(\mathrm{OH})_{2}+2\mathrm{HCl}\xlongequal{\;\;}\mathrm{CuCl}_{2}+2\mathrm{H}_{2}\mathrm{O}$
@@
(1)红 无 有白色固体析出
(2)$\mathrm{NaOH}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}$
@@
(1)微溶于水
(2)变红
(3)红色逐渐消失$\mathrm{Ca}(\mathrm{OH})_{2}+2\mathrm{HCl}\xlongequal{\;\;}\mathrm{CaCl}_{2}+2\mathrm{H}_{2}\mathrm{O}$
@@节约试剂,可减少对环境的污染,可同时完成多个实验,便于对比实验现象等。
@@先将试管横放,把铁钉放在试管口,然后将试管慢慢竖起。
@@紫色石蕊溶液在碱性溶液中呈蓝色,在中性溶液中呈紫色,蓝色与紫色之间没有明显的界线,不易判断反应终点。
@@因为它们解离出的阴离子都是氢氧根离子。
@@使用酸碱指示剂或pH试纸证明溶液的酸碱性发生了改变。
查看更多完整答案,请扫码查看


