第5页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
教材原型 四支试管中分别盛有相同质量分数的稀盐酸,将镁、锌、铁和铜四种金属分别同时放入其中(如图所示)。

(1)上述实验中能观察到有气泡生成的是__________(填名称,下同),其剧烈程度由强到弱的顺序是__________,不能观察到有气泡生成的是________。
(2)有关化学方程式为________________、________________、________________。
探究 小兵对“锌与稀硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与稀硫酸反应的快慢受哪些因素影响呢?
【猜想与假设】a. 可能与稀硫酸的浓度有关;b. 可能与锌的形状有关。
【设计并实验】小兵用不同浓度的稀硫酸和不同形状的锌进行如下实验:

(1)用如图所示的装置收集并测量氢气的体积,其中量筒的作用是______________________________,氢气应从____(填“a”或“b”)管通入。

【收集证据】(2)要比较不同浓度的稀硫酸对反应快慢的影响,应选择的实验编号是__________。
【得出结论】(3)结论是稀硫酸的浓度越________,反应速率越快。
【拓展延伸】(4)下表是小兵第①组实验的详细数据。
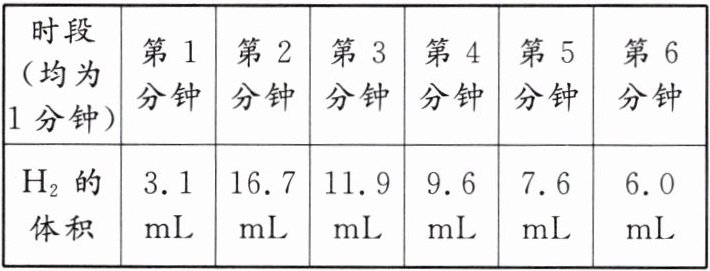
请描述锌与稀硫酸反应的快慢的变化并解释原因:______________________________。
(5)锌与稀硫酸反应的快慢可能还受哪些因素影响?设计实验验证。
影响因素:__________。
简述实验验证的方法:______________________________。

(1)上述实验中能观察到有气泡生成的是__________(填名称,下同),其剧烈程度由强到弱的顺序是__________,不能观察到有气泡生成的是________。
(2)有关化学方程式为________________、________________、________________。
探究 小兵对“锌与稀硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与稀硫酸反应的快慢受哪些因素影响呢?
【猜想与假设】a. 可能与稀硫酸的浓度有关;b. 可能与锌的形状有关。
【设计并实验】小兵用不同浓度的稀硫酸和不同形状的锌进行如下实验:

(1)用如图所示的装置收集并测量氢气的体积,其中量筒的作用是______________________________,氢气应从____(填“a”或“b”)管通入。

【收集证据】(2)要比较不同浓度的稀硫酸对反应快慢的影响,应选择的实验编号是__________。
【得出结论】(3)结论是稀硫酸的浓度越________,反应速率越快。
【拓展延伸】(4)下表是小兵第①组实验的详细数据。

请描述锌与稀硫酸反应的快慢的变化并解释原因:______________________________。
(5)锌与稀硫酸反应的快慢可能还受哪些因素影响?设计实验验证。
影响因素:__________。
简述实验验证的方法:______________________________。
答案:
教材原型
(1)镁、锌、铁 镁、锌、铁 铜
(2)$Mg + 2HCl = MgCl_{2} + H_{2}\uparrow$ $Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$ $Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
探究
(1)根据进入量筒中水的体积判断生成氢气的体积 a
(2)①③(或②④)
(3)大
(4)由慢到快然后逐渐减慢,该反应放热,故开始时反应速率加快,随着反应进行,硫酸被消耗,稀硫酸浓度变小,反应速率减慢
(5)温度 取质量相等的锌粒分别放入两支试管中,然后分别加入体积和浓度相同的稀硫酸,一支试管放在室温下,一支试管放在热水中水浴加热,测量收集等体积的氢气所需要的时间(合理即可)
(1)镁、锌、铁 镁、锌、铁 铜
(2)$Mg + 2HCl = MgCl_{2} + H_{2}\uparrow$ $Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$ $Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
探究
(1)根据进入量筒中水的体积判断生成氢气的体积 a
(2)①③(或②④)
(3)大
(4)由慢到快然后逐渐减慢,该反应放热,故开始时反应速率加快,随着反应进行,硫酸被消耗,稀硫酸浓度变小,反应速率减慢
(5)温度 取质量相等的锌粒分别放入两支试管中,然后分别加入体积和浓度相同的稀硫酸,一支试管放在室温下,一支试管放在热水中水浴加热,测量收集等体积的氢气所需要的时间(合理即可)
查看更多完整答案,请扫码查看


