第43页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
教材原型 利用以下装置对酸的化学性质进行探究。
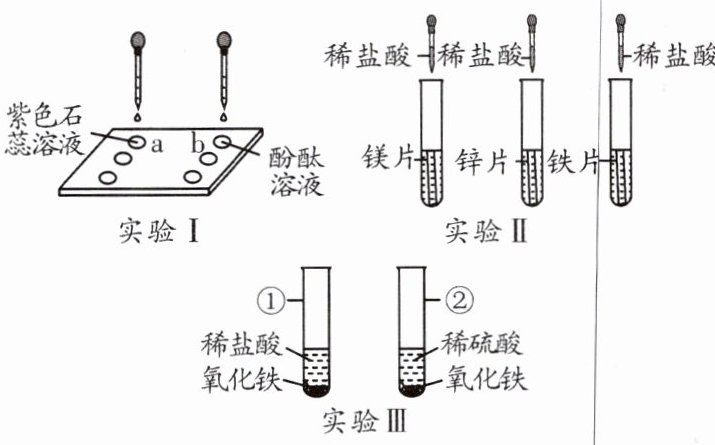
(1)实验Ⅰ中,在点滴板的 a、b 穴中滴入酸溶液后,溶液变红的是____(填“a”或“b”)。使用点滴板的优点之一是____。
(2)实验Ⅱ中,分别写出三个试管中发生反应的化学方程式:____、____、____。
(3)实验Ⅲ中,在试管①、②中均可观察到的现象是____、____。试管②中发生反应的化学方程式是____。
(4)以上的三个实验分别体现了酸的哪些化学性质:____、____、____。

(1)实验Ⅰ中,在点滴板的 a、b 穴中滴入酸溶液后,溶液变红的是____(填“a”或“b”)。使用点滴板的优点之一是____。
(2)实验Ⅱ中,分别写出三个试管中发生反应的化学方程式:____、____、____。
(3)实验Ⅲ中,在试管①、②中均可观察到的现象是____、____。试管②中发生反应的化学方程式是____。
(4)以上的三个实验分别体现了酸的哪些化学性质:____、____、____。
答案:
(1)a 节约试剂(方便观察反应现象等,合理即可)
(2)$Mg + 2HCl = MgCl_{2} + H_{2}\uparrow$ $Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$ $Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
(3)红棕色固体逐渐消失 溶液逐渐变成黄色 $Fe_{2}O_{3} + 3H_{2}SO_{4} = Fe_{2}(SO_{4})_{3} + 3H_{2}O$
(4)与指示剂反应 与活泼金属反应 与某些金属氧化物反应
(1)a 节约试剂(方便观察反应现象等,合理即可)
(2)$Mg + 2HCl = MgCl_{2} + H_{2}\uparrow$ $Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$ $Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
(3)红棕色固体逐渐消失 溶液逐渐变成黄色 $Fe_{2}O_{3} + 3H_{2}SO_{4} = Fe_{2}(SO_{4})_{3} + 3H_{2}O$
(4)与指示剂反应 与活泼金属反应 与某些金属氧化物反应
探究 1 下列关于镁条与稀盐酸反应的实验叙述正确的是 ( )
A. 先用 50mL 量筒量取 3mL 稀盐酸于试管中再加入镁条
B. 用温度计测得镁条与稀盐酸反应后溶液的温度为 51.23℃
C. 点燃镁条与稀盐酸反应得到的气体,产生淡蓝色火焰,该气体是氢气
D. 实验结束后将试管内的物质倒入下水道,并将试管洗刷干净
A. 先用 50mL 量筒量取 3mL 稀盐酸于试管中再加入镁条
B. 用温度计测得镁条与稀盐酸反应后溶液的温度为 51.23℃
C. 点燃镁条与稀盐酸反应得到的气体,产生淡蓝色火焰,该气体是氢气
D. 实验结束后将试管内的物质倒入下水道,并将试管洗刷干净
答案:
探究1 C
探究 2 某同学为探究盐酸的化学性质,做了如下实验:
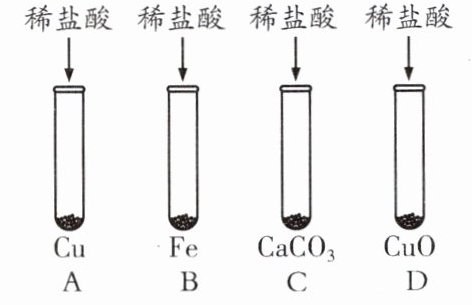
(1)ABCD 中无明显现象的是哪一组____(填字母,下同),有蓝色溶液产生的是____。
(2)B 中可以看到的现象是产生气泡,溶液由无色变成浅绿色,写出反应的化学方程式:____。
(3)C 中,发生反应的化学方程式为____,为了验证生成的气体,将气体通入试剂 X 中,试剂 X 的名称是____。

(1)ABCD 中无明显现象的是哪一组____(填字母,下同),有蓝色溶液产生的是____。
(2)B 中可以看到的现象是产生气泡,溶液由无色变成浅绿色,写出反应的化学方程式:____。
(3)C 中,发生反应的化学方程式为____,为了验证生成的气体,将气体通入试剂 X 中,试剂 X 的名称是____。
答案:
(1)A D
(2)$Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
(3)$CaCO_{3} + 2HCl = CaCl_{2} + H_{2}O + CO_{2}\uparrow$ 澄清石灰水
(1)A D
(2)$Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
(3)$CaCO_{3} + 2HCl = CaCl_{2} + H_{2}O + CO_{2}\uparrow$ 澄清石灰水
探究 3 小江和小亮在实验室中用锌粒和过量的稀硫酸制取氢气,实验后发现容器中的固体全部溶解,对所得溶液中含有的溶质,他们进行了如下探究。
【作出猜想】①溶质只有硫酸锌;
②溶质有硫酸锌和____(填化学式)。
【查阅资料】硫酸锌溶液酸性极弱(不能与活泼金属反应)。
【设计并进行实验】
(1)若要验证猜想①是否正确,能不能选用无色酚酞溶液作为试剂?____(填“能”或“不能”),理由是____。
(2)小江选用一种金属单质进行实验,观察到了明显的现象,从而肯定了猜想②是正确的,写出发生反应的化学方程式:____。
(3)小亮用生锈的铁钉也完成了对猜想②的证明,他观察到的实验现象为____。
【作出猜想】①溶质只有硫酸锌;
②溶质有硫酸锌和____(填化学式)。
【查阅资料】硫酸锌溶液酸性极弱(不能与活泼金属反应)。
【设计并进行实验】
(1)若要验证猜想①是否正确,能不能选用无色酚酞溶液作为试剂?____(填“能”或“不能”),理由是____。
(2)小江选用一种金属单质进行实验,观察到了明显的现象,从而肯定了猜想②是正确的,写出发生反应的化学方程式:____。
(3)小亮用生锈的铁钉也完成了对猜想②的证明,他观察到的实验现象为____。
答案:
探究3 [作出猜想]$H_{2}SO_{4}$
@@[设计并进行实验]
(1)不能 酚酞溶液在酸性溶液和中性溶液中均不变色
(2)$Fe + H_{2}SO_{4} = FeSO_{4} + H_{2}\uparrow$(合理即可)
(3)铁锈消失,溶液变为黄色
@@[设计并进行实验]
(1)不能 酚酞溶液在酸性溶液和中性溶液中均不变色
(2)$Fe + H_{2}SO_{4} = FeSO_{4} + H_{2}\uparrow$(合理即可)
(3)铁锈消失,溶液变为黄色
查看更多完整答案,请扫码查看


