第82页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
3. 中和反应的应用
(1)改良酸性或碱性的土壤:常用__________来改良酸性土壤。
(2)废水处理:如用熟石灰来处理含硫酸的废水,化学方程式为____________________。
(3)医药应用:常用含$Al(OH)_{3}$和$Mg(OH)_{2}$的药物来中和胃酸,化学方程式分别为
①____________________。
②____________________。
(1)改良酸性或碱性的土壤:常用__________来改良酸性土壤。
(2)废水处理:如用熟石灰来处理含硫酸的废水,化学方程式为____________________。
(3)医药应用:常用含$Al(OH)_{3}$和$Mg(OH)_{2}$的药物来中和胃酸,化学方程式分别为
①____________________。
②____________________。
答案:
(1)熟石灰 (2)Ca(OH)₂ + H₂SO₄ = CaSO₄ + 2H₂O
(3)①Al(OH)₃ + 3HCl = AlCl₃ + 3H₂O ②Mg(OH)₂ + 2HCl = MgCl₂ + 2H₂O
三、复分解反应
1. 复分解反应:参加反应的两种化合物____________________生成另外两种__________的反应。
2. 通式:AB + CD → AD + CB。
3. 特征:两交换,价不变。反应时两种化合物要互相__________,反应过程中各元素______不变。
1. 复分解反应:参加反应的两种化合物____________________生成另外两种__________的反应。
2. 通式:AB + CD → AD + CB。
3. 特征:两交换,价不变。反应时两种化合物要互相__________,反应过程中各元素______不变。
答案:
互相交换成分,化合物
@@交换成分,化合价
@@交换成分,化合价
【例1】酸具有共同的性质,是因为 ( )
A. 都能使石蕊溶液变红
B. 都能解离出氢离子
C. 都能跟碱反应生成盐和水
D. 都含有氧元素
解析:能使石蕊溶液变红是酸的共性但不是具有共性的原因,故A错误;酸在解离时都会生成氢离子,所以酸的共性的实质是氢离子的性质,所以能解离出氢离子是酸具有共性的原因,故B正确;能跟碱反应生成盐和水是酸的共性不是酸具有共性的原因,故C错误;酸可分为含氧酸与无氧酸,所以不是所有的酸都含有氧元素,也不是酸具有共同性质的原因,故D错误。
答案:B
A. 都能使石蕊溶液变红
B. 都能解离出氢离子
C. 都能跟碱反应生成盐和水
D. 都含有氧元素
解析:能使石蕊溶液变红是酸的共性但不是具有共性的原因,故A错误;酸在解离时都会生成氢离子,所以酸的共性的实质是氢离子的性质,所以能解离出氢离子是酸具有共性的原因,故B正确;能跟碱反应生成盐和水是酸的共性不是酸具有共性的原因,故C错误;酸可分为含氧酸与无氧酸,所以不是所有的酸都含有氧元素,也不是酸具有共同性质的原因,故D错误。
答案:B
答案:
B
【例2】(2023包头)常温下向一定量的稀盐酸中逐滴加入氢氧化钠溶液至过量,测得水的质量、氯化钠的质量随氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是 ( )
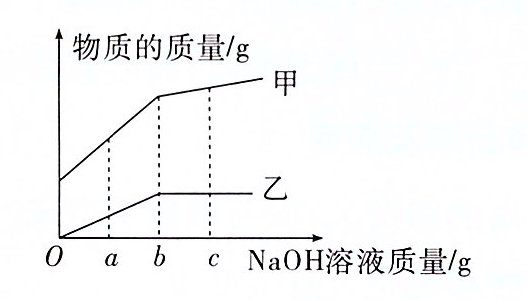
A. 乙表示的物质为氯化钠
B. 加入b g NaOH溶液时,恰好完全反应
C. 加入c g NaOH溶液时,所得溶液中的阴离子为$Cl^{-}$
D. NaOH溶液由a g递增到b g,所得溶液的酸性逐渐减弱
解析:由于稀盐酸中含有水,因此未开始反应时水的质量不为零;盐酸和氢氧化钠反应生成氯化钠和水,氯化钠的质量由0逐渐增大,至完全反应时质量不再改变。由此可知甲表示水的质量,乙表示氯化钠的质量,A正确;加入b g氢氧化钠时,氯化钠质量达到最大,说明此时滴入的氢氧化钠和盐酸恰好完全反应,B正确;加入c g氢氧化钠时,氢氧化钠过量,此时溶液中的溶质为氢氧化钠和氯化钠,其中的阴离子为$OH^{-}$和$Cl^{-}$,C不正确;氢氧化钠溶液由a g递增到b g,溶液中的盐酸不断被中和而减少,则溶液的酸性逐渐减弱,D正确。
答案:C

A. 乙表示的物质为氯化钠
B. 加入b g NaOH溶液时,恰好完全反应
C. 加入c g NaOH溶液时,所得溶液中的阴离子为$Cl^{-}$
D. NaOH溶液由a g递增到b g,所得溶液的酸性逐渐减弱
解析:由于稀盐酸中含有水,因此未开始反应时水的质量不为零;盐酸和氢氧化钠反应生成氯化钠和水,氯化钠的质量由0逐渐增大,至完全反应时质量不再改变。由此可知甲表示水的质量,乙表示氯化钠的质量,A正确;加入b g氢氧化钠时,氯化钠质量达到最大,说明此时滴入的氢氧化钠和盐酸恰好完全反应,B正确;加入c g氢氧化钠时,氢氧化钠过量,此时溶液中的溶质为氢氧化钠和氯化钠,其中的阴离子为$OH^{-}$和$Cl^{-}$,C不正确;氢氧化钠溶液由a g递增到b g,溶液中的盐酸不断被中和而减少,则溶液的酸性逐渐减弱,D正确。
答案:C
答案:
C
查看更多完整答案,请扫码查看


