第79页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
- 第213页
- 第214页
- 第215页
- 第216页
- 第217页
- 第218页
- 第219页
- 第220页
- 第221页
- 第222页
- 第223页
- 第224页
- 第225页
- 第226页
- 第227页
- 第228页
- 第229页
- 第230页
- 第231页
- 第232页
- 第233页
- 第234页
- 第235页
- 第236页
- 第237页
- 第238页
- 第239页
- 第240页
- 第241页
- 第242页
- 第243页
- 第244页
- 第245页
- 第246页
- 第247页
- 第248页
- 第249页
- 第250页
- 第251页
- 第252页
- 第253页
- 第254页
- 第255页
- 第256页
- 第257页
- 第258页
- 第259页
- 第260页
- 第261页
- 第262页
- 第263页
2.[2021·全国甲卷,26(1)]碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
I₂的一种制备方法如图所示:

①加入Fe粉进行转化反应的离子方程式为______________________________,生成的沉淀与硝酸反应,生成________________后可循环使用。
②通入Cl₂的过程中,若氧化产物只有一种,反应的化学方程式为__________________________;若反应物用量比$\frac{n(Cl_{2})}{n(FeI_{2})}=1.5$时,氧化产物为____________;当$\frac{n(Cl_{2})}{n(FeI_{2})}>1.5$后,单质碘的收率会降低,原因是______________________________。
I₂的一种制备方法如图所示:

①加入Fe粉进行转化反应的离子方程式为______________________________,生成的沉淀与硝酸反应,生成________________后可循环使用。
②通入Cl₂的过程中,若氧化产物只有一种,反应的化学方程式为__________________________;若反应物用量比$\frac{n(Cl_{2})}{n(FeI_{2})}=1.5$时,氧化产物为____________;当$\frac{n(Cl_{2})}{n(FeI_{2})}>1.5$后,单质碘的收率会降低,原因是______________________________。
答案:
①$2AgI + Fe = 2Ag + Fe^{2+} + 2I^{-}$ $AgNO_{3}$
②$FeI_{2} + Cl_{2} = I_{2} + FeCl_{2}$ $I_{2}$、$FeCl_{3}$ $I_{2}$被过量的$Cl_{2}$进一步氧化
解析 ①由流程图可知悬浊液中含$AgI$,$AgI$可与$Fe$反应生成$FeI_{2}$和$Ag$,$FeI_{2}$易溶于水,在离子方程式中能拆,故加入$Fe$粉进行转化反应的离子方程式为$2AgI + Fe = 2Ag + Fe^{2+} + 2I^{-}$,生成的银能与硝酸反应生成硝酸银参与循环。②通入$Cl_{2}$的过程中,因$I^{-}$还原性强于$Fe^{2+}$,$Cl_{2}$先氧化还原性强的$I^{-}$,若氧化产物只有一种,则该氧化产物只能是$I_{2}$,故反应的化学方程式为$FeI_{2} + Cl_{2} = I_{2} + FeCl_{2}$;若反应物用量比$\frac{n(Cl_{2})}{n(FeI_{2})}=1.5$时,先氧化完全部$I^{-}$再氧化$Fe^{2+}$,恰好将全部$I^{-}$和$Fe^{2+}$氧化,故氧化产物为$I_{2}$、$FeCl_{3}$;当$\frac{n(Cl_{2})}{n(FeI_{2})}>1.5$即$Cl_{2}$过量,多余的氯气会与生成的单质碘以及水继续发生氧化还原反应,单质碘的收率会降低。
②$FeI_{2} + Cl_{2} = I_{2} + FeCl_{2}$ $I_{2}$、$FeCl_{3}$ $I_{2}$被过量的$Cl_{2}$进一步氧化
解析 ①由流程图可知悬浊液中含$AgI$,$AgI$可与$Fe$反应生成$FeI_{2}$和$Ag$,$FeI_{2}$易溶于水,在离子方程式中能拆,故加入$Fe$粉进行转化反应的离子方程式为$2AgI + Fe = 2Ag + Fe^{2+} + 2I^{-}$,生成的银能与硝酸反应生成硝酸银参与循环。②通入$Cl_{2}$的过程中,因$I^{-}$还原性强于$Fe^{2+}$,$Cl_{2}$先氧化还原性强的$I^{-}$,若氧化产物只有一种,则该氧化产物只能是$I_{2}$,故反应的化学方程式为$FeI_{2} + Cl_{2} = I_{2} + FeCl_{2}$;若反应物用量比$\frac{n(Cl_{2})}{n(FeI_{2})}=1.5$时,先氧化完全部$I^{-}$再氧化$Fe^{2+}$,恰好将全部$I^{-}$和$Fe^{2+}$氧化,故氧化产物为$I_{2}$、$FeCl_{3}$;当$\frac{n(Cl_{2})}{n(FeI_{2})}>1.5$即$Cl_{2}$过量,多余的氯气会与生成的单质碘以及水继续发生氧化还原反应,单质碘的收率会降低。
3.[2018·全国卷Ⅲ,27(1)(2)]KIO₃是一种重要的无机化合物,可作为食盐中的补碘剂。
(1)KIO₃的化学名称是__________。
(2)利用“KClO₃氧化法”制备KIO₃工艺流程如下图所示:

“酸化反应”所得产物有KH(IO₃)₂、Cl₂和KCl。“逐Cl₂”采用的方法是______________________。“滤液”中的溶质主要是____________。“调pH”中发生反应的化学方程式为__________________。
(1)KIO₃的化学名称是__________。
(2)利用“KClO₃氧化法”制备KIO₃工艺流程如下图所示:

“酸化反应”所得产物有KH(IO₃)₂、Cl₂和KCl。“逐Cl₂”采用的方法是______________________。“滤液”中的溶质主要是____________。“调pH”中发生反应的化学方程式为__________________。
答案:
(1)碘酸钾
(2)加热 $KCl$ $KH(IO_{3})_{2} + KOH = 2KIO_{3}+H_{2}O$
(1)碘酸钾
(2)加热 $KCl$ $KH(IO_{3})_{2} + KOH = 2KIO_{3}+H_{2}O$
1. 硫元素的存在形态


答案:
硫化物 硫酸盐
[思考](1)硫有$S_2$、$S_4$、$S_6$、$S_8$等多种单质,它们的关系是什么?加热时,$S_8$转化为$S_6$、$S_4$、$S_2$属于什么变化?
______________________________
(2)硫单质难溶于水,易溶于$CS_2$,其原因是什么?
______________________________
______________________________
(2)硫单质难溶于水,易溶于$CS_2$,其原因是什么?
______________________________
答案:
$S_{2}$、$S_{4}$、$S_{6}$、$S_{8}$属于同一元素的不同种单质,它们互为同素异形体,$S_{8}$转化为$S_{6}$、$S_{4}$、$S_{2}$属于化学变化。
@@硫单质、$CS_{2}$均属于非极性分子,而$H_{2}O$属于极性分子,根据“相似相溶”规律,非极性分子易溶于非极性分子形成的溶剂中。
@@硫单质、$CS_{2}$均属于非极性分子,而$H_{2}O$属于极性分子,根据“相似相溶”规律,非极性分子易溶于非极性分子形成的溶剂中。
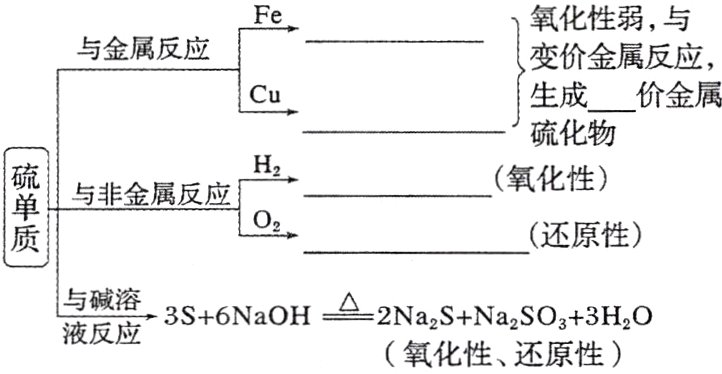
3. 从化合价的角度认识硫单质的化学性质
$\overset{-2}{S}\xleftarrow{氧化性}\overset{0}{S}\xrightarrow{还原性}\overset{+4}{S}$
$\overset{-2}{S}\xleftarrow{氧化性}\overset{0}{S}\xrightarrow{还原性}\overset{+4}{S}$

答案:
$Fe + S\xlongequal{\triangle}FeS$ $2Cu + S\xlongequal{\triangle}Cu_{2}S$ 低 $H_{2} + S\xlongequal{\triangle}H_{2}S$ $S + O_{2}\xlongequal{点燃}SO_{2}$
易错辨析
1. 硫在空气中燃烧的产物是$SO_2$,在纯氧中燃烧的产物是$SO_3$ ( )
2. 硫与铁粉和铜粉分别反应,都可生成二价金属硫化物 ( )
1. 硫在空气中燃烧的产物是$SO_2$,在纯氧中燃烧的产物是$SO_3$ ( )
2. 硫与铁粉和铜粉分别反应,都可生成二价金属硫化物 ( )
答案:
×
@@×
@@×
查看更多完整答案,请扫码查看


