第47页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
- 第213页
- 第214页
- 第215页
- 第216页
- 第217页
- 第218页
- 第219页
- 第220页
- 第221页
- 第222页
- 第223页
- 第224页
- 第225页
- 第226页
- 第227页
- 第228页
- 第229页
- 第230页
- 第231页
- 第232页
- 第233页
- 第234页
- 第235页
- 第236页
- 第237页
- 第238页
- 第239页
- 第240页
- 第241页
- 第242页
- 第243页
- 第244页
- 第245页
- 第246页
- 第247页
- 第248页
- 第249页
- 第250页
- 第251页
- 第252页
- 第253页
- 第254页
- 第255页
- 第256页
- 第257页
- 第258页
- 第259页
- 第260页
- 第261页
- 第262页
- 第263页
3. 制备金属单质
(1)钠是强还原剂,用Na来制取钛(Ti)、锆(Zr)、铌(Nb)等稀有金属。金属铌可用金属钠还原K₂NbF₇制取,写出热还原法制备铌的化学方程式:______________________________。
(2)下列关于钠制取金属钛的方案错误的是________(填字母)。
A. 工业上用钠单质与TiCl₄溶液反应制取钛单质
B. 金属钠与熔融的TiCl₄反应可制备金属钛
(1)钠是强还原剂,用Na来制取钛(Ti)、锆(Zr)、铌(Nb)等稀有金属。金属铌可用金属钠还原K₂NbF₇制取,写出热还原法制备铌的化学方程式:______________________________。
(2)下列关于钠制取金属钛的方案错误的是________(填字母)。
A. 工业上用钠单质与TiCl₄溶液反应制取钛单质
B. 金属钠与熔融的TiCl₄反应可制备金属钛
答案:
(1)$K_{2}NbF_{7} + 5Na = Nb + 5NaF + 2KF$
(2)A
(1)$K_{2}NbF_{7} + 5Na = Nb + 5NaF + 2KF$
(2)A
4. (2021·福建1月适应性考试,10)钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化示意图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是 ( )
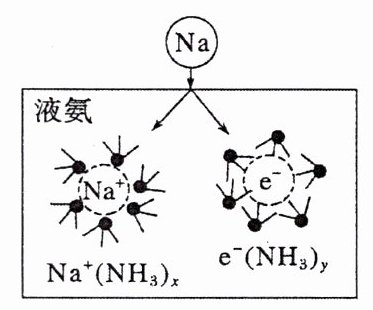
A. 钠的密度比液氨大
B. 溶液的导电性增强
C. 0.1 mol钠投入液氨 中生成0.01 mol H₂时,Na共失去0.02 mol电子
D. 钠和液氨可以发生的反应为2NH₃ + 2Na == 2NaNH₂ + H₂↑

A. 钠的密度比液氨大
B. 溶液的导电性增强
C. 0.1 mol钠投入液氨 中生成0.01 mol H₂时,Na共失去0.02 mol电子
D. 钠和液氨可以发生的反应为2NH₃ + 2Na == 2NaNH₂ + H₂↑
答案:
C [钠沉入液氨中说明钠的密度比液氨大,A正确;液氨中没有能导电的离子,而钠投入液氨中生成蓝色的溶剂合电子,能导电,说明溶液的导电性增强,B正确;钠投入液氨中先生成络合物,再反应得到$H_{2}$,故$0.1mol$钠反应失去$0.1mol$电子,C错误;反应中钠失去电子,只能是氢元素得到电子,所以钠和液氨可以发生的反应为$2NH_{3} + 2Na = 2NaNH_{2} + H_{2}\uparrow$,D正确。]
整合 必备知识
1. 氧化钠和过氧化钠
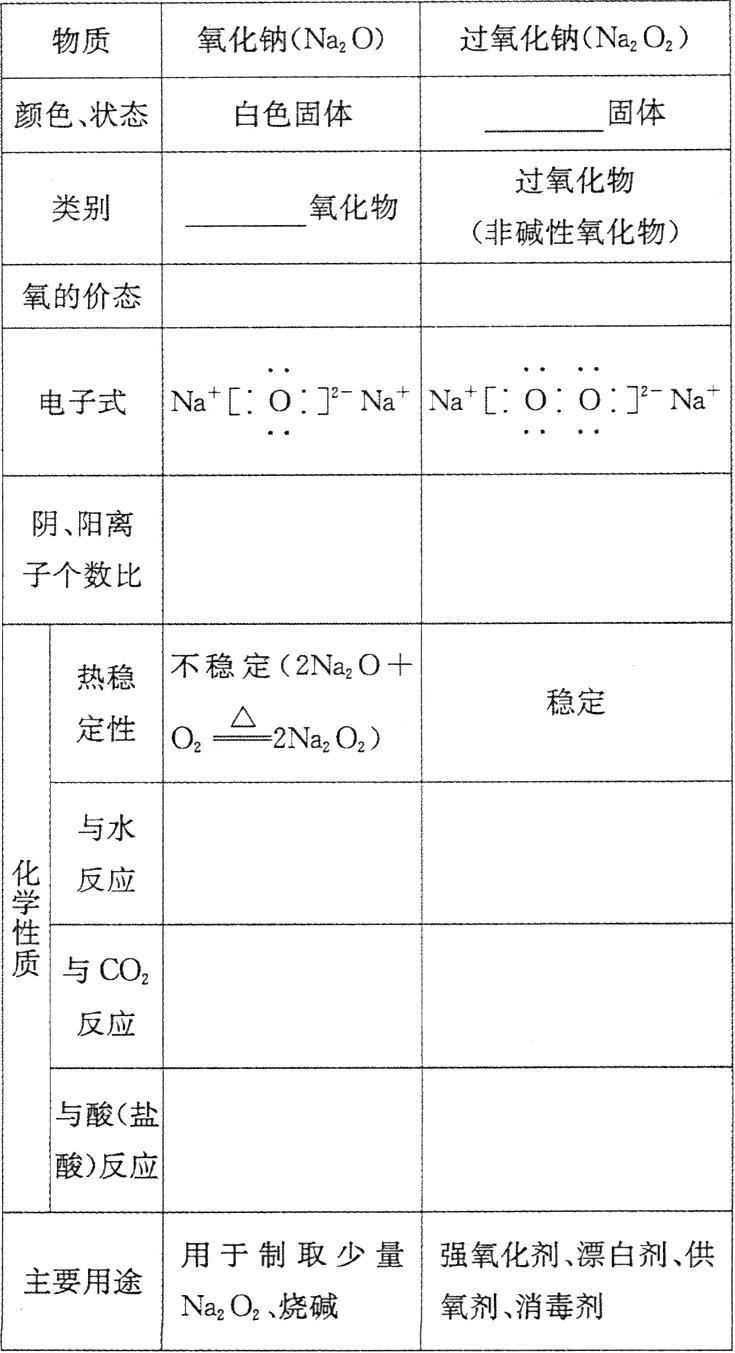
1. 氧化钠和过氧化钠

答案:
淡黄色 碱性 -2 -1 1 : 2 1 : 2 $Na_{2}O + H_{2}O = 2NaOH$ $2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow$ $Na_{2}O + CO_{2} = Na_{2}CO_{3}$ $2Na_{2}O_{2} + 2CO_{2} = 2Na_{2}CO_{3} + O_{2}$ $Na_{2}O + 2HCl = 2NaCl + H_{2}O$ $2Na_{2}O_{2} + 4HCl = 4NaCl + 2H_{2}O + O_{2}\uparrow$
2. Na₂O₂的强氧化性与还原性
从元素化合价角度分析Na₂O₂的性质
$O_{2}\xleftarrow[表现还原性]{失去电子,化合价升高}Na_{2}O_{2}\xrightarrow[表现氧化性]{得到电子,化合价降低}O^{-2}$(1)Na₂O₂表现强氧化性
$Na_{2}O_{2}+SO_{2}\xlongequal{\;\;}$ ______________;
$Na_{2}O_{2}+Na_{2}SO_{3}+H_{2}O\xlongequal{\;\;}$ ________________;
$Na_{2}O_{2}+H_{2}S\xlongequal{\;\;}$ ____________________;
$Na_{2}O_{2}+$品红溶液→品红溶液褪色;
$Na_{2}O_{2}+$酚酞溶液→溶液先变红后褪色。
(2)Na₂O₂表现还原性
当遇KMnO₄等强氧化剂时,Na₂O₂被氧化,其氧化产物为O₂。
(3)Na₂O₂既表现氧化性又表现还原性
遇CO₂、H₂O、H⁺则发生自身的氧化还原反应。
从元素化合价角度分析Na₂O₂的性质
$O_{2}\xleftarrow[表现还原性]{失去电子,化合价升高}Na_{2}O_{2}\xrightarrow[表现氧化性]{得到电子,化合价降低}O^{-2}$(1)Na₂O₂表现强氧化性
$Na_{2}O_{2}+SO_{2}\xlongequal{\;\;}$ ______________;
$Na_{2}O_{2}+Na_{2}SO_{3}+H_{2}O\xlongequal{\;\;}$ ________________;
$Na_{2}O_{2}+H_{2}S\xlongequal{\;\;}$ ____________________;
$Na_{2}O_{2}+$品红溶液→品红溶液褪色;
$Na_{2}O_{2}+$酚酞溶液→溶液先变红后褪色。
(2)Na₂O₂表现还原性
当遇KMnO₄等强氧化剂时,Na₂O₂被氧化,其氧化产物为O₂。
(3)Na₂O₂既表现氧化性又表现还原性
遇CO₂、H₂O、H⁺则发生自身的氧化还原反应。
答案:
$Na_{2}SO_{4}$ $Na_{2}SO_{4} + 2NaOH$ $S\downarrow + 2NaOH$
□ 易错辨析
1. 氧化钠、过氧化钠均为离子化合物 ( )
2. 1 mol Na₂O₂固体中含离子总数为4Nₐ ( )
3. H₂O₂和Na₂O₂都属于过氧化物,含有的化学键完全相同 ( )
4. Na₂O₂投入滴加酚酞的水中,溶液先变红后褪色,并产生大量无色气泡 ( )
5. Na₂O由两种单质直接反应生成 ( )
1. 氧化钠、过氧化钠均为离子化合物 ( )
2. 1 mol Na₂O₂固体中含离子总数为4Nₐ ( )
3. H₂O₂和Na₂O₂都属于过氧化物,含有的化学键完全相同 ( )
4. Na₂O₂投入滴加酚酞的水中,溶液先变红后褪色,并产生大量无色气泡 ( )
5. Na₂O由两种单质直接反应生成 ( )
答案:
√
@@×
@@×
@@√
@@√
@@×
@@×
@@√
@@√
1. (1)用单线桥分析Na₂O₂与水的反应中电子转移的方向和数目:____________________________
______________________________;其中氧化剂是______________,还原剂是________________,氧化产物是______________,还原产物是________。
(2)Na₂O₂与CO₂反应生成0.1 mol氧气时,转移的电子数为________。
______________________________;其中氧化剂是______________,还原剂是________________,氧化产物是______________,还原产物是________。
(2)Na₂O₂与CO₂反应生成0.1 mol氧气时,转移的电子数为________。
答案:
(1)$2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow$ $Na_{2}O_{2}$ $Na_{2}O_{2}$ $O_{2}$ $NaOH$
(2)$0.2N_{A}$(或$1.204×10^{23}$)
(1)$2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow$ $Na_{2}O_{2}$ $Na_{2}O_{2}$ $O_{2}$ $NaOH$
(2)$0.2N_{A}$(或$1.204×10^{23}$)
查看更多完整答案,请扫码查看


