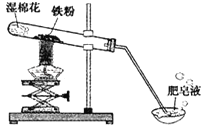
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是 .
(2)探究生成的气体是什么?
反应中有肥皂泡飘到空中时,用燃着的木条靠近肥皂泡,有听到爆鸣声.说明生成的气体是 .
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是 .
【实验探究】根据猜想与假设,设计实验方案加以检验.
实验操作 | 实验现象及结论 |
取适量黑色固体,加入足量的 | 有气泡产生 |
【实验结论】剩余固体是Fe与Fe3O4.
【反思与交流】该黑色固体不可能是Fe2O3,理由是 .
参考答案:
【答案】(1)提供水蒸气;(2)氢气;(3)【猜想与假设】Fe3O4;
【实验探究】
实验操作 | 实验现象及结论 |
稀盐酸 |
【反思与交流】Fe2O3红棕色粉末且不能被磁铁吸引
【解析】
(1)根据图和“高温下,铁与水蒸气能反应”,可知试管尾部放一团湿棉花的目的是提供水蒸气.
(2)用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体具有可燃性、密度小于空气,再根据反应物为“铁与水蒸气”,则是氢气.
【猜想与假设】能被磁铁吸引的只有Fe与Fe3O4,则猜想一Fe与Fe3O4;又不可能只有Fe没有其他反应产物,猜想二是Fe3O4;验证猜想一与猜想二,关键是否含有Fe.
【实验探究】根据铁与稀盐酸反应产生气体,进行设计实验:
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸 | 有气泡产生 |
【实验结论】剩余固体是Fe与Fe3O4..
【反思与交流】该黑色固体不可能是Fe2O3,理由是 Fe2O3红棕色粉末且不能被磁铁吸引.
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是某种加碘食盐包装标签上的部分内容.请用化学用语表示下列带点部分:

(1)该食盐的主要成分是氯化钠 ;
(2)食用该食盐可补充钙元素 ;
(3)碘原子的结构示意图为
 ,碘原子在化学反应中易形成碘离子 .
,碘原子在化学反应中易形成碘离子 . -
科目: 来源: 题型:
查看答案和解析>>【题目】下表除杂质所选试剂正确的是
选项
物质
所含杂质
除去杂质的方法
A
CaO
CaCO3
加入稀盐酸至不再产生气泡
B
CO2气体
HCl气体
通入NaOH溶液
C
CO2气体
CO气体
通过灼热的CuO
D
NaCl溶液
Na2CO3
加入稀硫酸至不再产生气泡
-
科目: 来源: 题型:
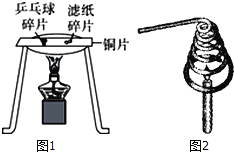
查看答案和解析>>【题目】某兴趣小组围绕“燃烧条件”这一主题开展如下探究活动,请你参与.
【实验内容】
①用棉花分别蘸酒精和水,放在酒精灯上加热片刻,观察现象.
②取一小块乒乓球碎片和滤纸碎片,分别用坩埚钳夹住,放在酒精灯火焰上加热,观察两种物质都能燃烧.
③从乒乓球和滤纸上各剪下一小片(同样大小),如图1所示分开放在一片薄铜片的两侧,加热铜片的中部,观察现象.
【分析讨论】
(1)进行实验①时,如果在酒精灯上加热时间较长,两个棉花球都会燃烧起来. 其中蘸水的棉花球燃烧的原因是 ;
(2)进行实验②的目的是为了证明 ,实验③看到的现象是 ,这两个实验的对比说明,燃烧的条件之一是 .
【反思与应用】
(3)毕业联欢会上,小明表演了一个小魔术:将一根粗铜丝绕成线圈,罩在蜡烛火焰上(如图2所示),观察到火焰缓缓熄灭,他再将铜圈加热后罩在蜡烛火焰上,观察到蜡烛照常燃烧,请你分析原因是: .
-
科目: 来源: 题型:
查看答案和解析>>【题目】2016年3月联合国秘书长潘基文任命游戏“愤怒的小鸟”为绿色荣誉大使,以鼓励年轻人应对气候变化及环境污染采取积极的行动。以下哪些行为是不提倡的( )
A.出行多选择自行车和公交车
B.大量使用塑料袋方便购物
C.植树造林,增加城市绿地面积
D.对垃圾分类,回收利用
-
科目: 来源: 题型:
查看答案和解析>>【题目】硝酸铵可发生如下反应:2NH4NO3═2N2↑+O2↑+4X,则 X的化学式是( )
A.H2 B.H2O C.H2O2 D.HNO3
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的鉴别方法错误的是
A.用水鉴别氢氧化钠和硝酸铵固体
B.用带火星的小木条验证空气和氧气
C.用小木条鉴别浓硫酸和稀硫酸
D.用燃着的小木条鉴别二氧化碳和氮气
相关试题

