【题目】草酸亚铁晶体(FeC2O4·2H2O)受热的方程式为:FeC2O4·2H2O![]() FeO +CO↑+CO2↑+2H2O,通过如下装置验证该反应得到的气体产物,说法正确的是
FeO +CO↑+CO2↑+2H2O,通过如下装置验证该反应得到的气体产物,说法正确的是
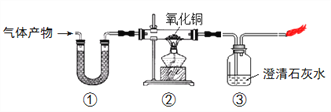
A. ①中固体为胆矾,可验证气体产物中的水蒸气
B. ②中固体由黑色变红色,可验证气体产物中有一氧化碳
C. ③中石灰水变浑浊,可验证气体产物中有一氧化碳
D. ③中石灰水变浑浊,可验证气体产物中有二氧化碳
参考答案:
【答案】B
【解析】根据所学知识和题中信息知,草酸亚铁晶体(FeC2O4·2H2O)受热的方程式为:
FeC2O4·2H2O![]() FeO +CO↑+CO2↑+2H2O。A、 ①中固体为无水硫酸铜,无水硫酸铜遇水变为蓝色,可验证气体产物中的水蒸气,故A错误;B、②中固体由黑色变红色,可验证气体产物中有一氧化碳,一氧化碳具有还原性,可以把氧化铜还原为铜,铜为红色,故B正确;C、 ③中石灰水变浑浊,不可验证气体产物中有一氧化碳,故C错误;D、③中石灰水变浑浊,不可验证气体产物中有二氧化碳,一氧化碳通过氧化铜被氧化为二氧化碳,故D错误。
FeO +CO↑+CO2↑+2H2O。A、 ①中固体为无水硫酸铜,无水硫酸铜遇水变为蓝色,可验证气体产物中的水蒸气,故A错误;B、②中固体由黑色变红色,可验证气体产物中有一氧化碳,一氧化碳具有还原性,可以把氧化铜还原为铜,铜为红色,故B正确;C、 ③中石灰水变浑浊,不可验证气体产物中有一氧化碳,故C错误;D、③中石灰水变浑浊,不可验证气体产物中有二氧化碳,一氧化碳通过氧化铜被氧化为二氧化碳,故D错误。
点睛∶无水硫酸铜遇水变为蓝色。一氧化碳具有还原性,二氧化碳可使石灰水变浑浊。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表是氯化钠和硝酸钾在不同温度下的溶解度。(假设硝酸钾与氯化钠同时溶解在水中各自的溶解度不变,实验过程中水分损失忽略不计)。
温度(℃)
0
20
40
60
80
100
溶解度(g/100g水)
KNO3
13.3
31.6
64.0
110.0
169.0
246.0
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
①由表可知,20℃时,氯化钠的溶解度是________。影响硝酸钾溶解度的因素是_________。
②在80℃的100g水中溶解NaCl和KNO3,进行以下实验:
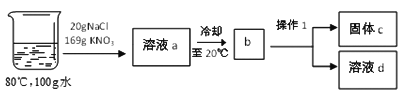
Ⅰ.操作1的名称是_________。
Ⅱ.溶液a冷却至b的过程中出现的现象是__________。溶液d中所含的溶质是_________。
Ⅲ.对整个实验过程分析正确的是_________。
A.无法判断a、d溶液中氯化钠溶液的状态 B.固体c是纯净物
C.溶液a中硝酸钾的质量分数为
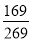 D.硝酸钾溶液始终处于饱和状态
D.硝酸钾溶液始终处于饱和状态 -
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制备二氧化碳的实验装置如下图所示。
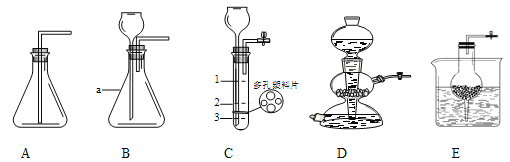
①写出仪器名称:a_______,D的装置的名称是________。此时D装置的开关处于_________状态(选填“开”或“关”)。E与D装置制取气体具有相同的优点是_________。
②观察A~E装置,____________装置(选填编号)进行实验时,集气瓶中不能收集得到二氧化碳,原因是_______________。
③用C装置制取CO2,反应时装置内盐酸液面应位于_____________处(选填“1、2或3”)为宜,理由是_______________。
④测定其大理石中碳酸钙的质量分数。在15g大理石中分5次共加入50.0g稀盐酸(假设杂质不与盐酸反应,忽略盐酸的挥发),部分数据如下表。
容器中盐酸的质量
10
20
40
50
气体质量m/g
1.1
2.2
m
4.4
根据实验数据回答下列问题:
Ⅰ. 当盐酸滴入40g时,对应的气体质量m是________g。
Ⅱ. 大理石中碳酸钙的质量分数是_______。(根据化学方程式列式计算,结果精确到0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某气体可能含有CO2 、 CO一种或二种。为探究其成分进行以下实验。
[实验步骤]
步骤一:打开K,缓缓通入干燥的氮气一段时间,关闭K。
步骤二:通入待测气体,同时打开K,点燃酒精灯,进行实验。
[实验结论] 该气体是CO、CO2混合物。
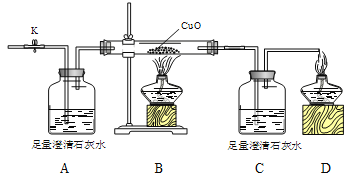
回答问题:
①写出B中玻璃管内发生反应的化学方程式______________。
②实验过程中,根据_______________实验现象可以判断该气体的成分。
③对该实验的分析正确的是___________(选填编号)
Ⅰ.步骤一的目的是为了把容器中空气反应完
Ⅱ.C中增加的质量与B中固体减少的质量相等
Ⅲ.省略C装置对检验的结果没有影响
Ⅳ.反应结束后继续通气体的目的是防止生成的铜与空气中氧气反应
V.实验结束应先灭B处的酒精灯
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表是氢氧化钙和氢氧化钠的溶解度数据。请回答下列问题:
温度/℃
0
20
40
60
80
100
溶解度
(g/100gH2O)
氢氧化钙
0.19
0.17
0.14
0.12
0.09
0.08
氢氧化钠
31
91
111
129
313
336
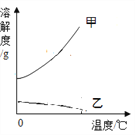
① 氢氧化钠溶解度曲线是____(选填“甲”或“乙”)
② 把接近饱和的氢氧化钙溶液变成饱和溶液的方法是______。
③ 20 ℃时,10 g水中溶解______克氢氧化钠恰好饱和。
④ 20 ℃时,分别在100克水中加入m克氢氧化钠和氢氧化钙固体,可得到质量分数相同的两种溶液,则m的取值范围是______。
⑤ 60 ℃时,氢氧化钠的饱和溶液中含少量氢氧化钙,把其降温,结晶后过滤,对滤渣、滤液成分分析正确的是______。
Ⅰ.滤渣中只有氢氧化钠
Ⅱ.滤渣中一定有氢氧化钠,可能有氢氧化钙
Ⅲ.滤液中一定有氢氧化钙,可能有氢氧化钠
Ⅳ.滤液中一定有氢氧化钠和氢氧化钙
⑥ 氢氧化钙溶液和氢氧化钠溶液都是无色溶液,都能与二氧化碳发生反应。氢氧化钠与二氧化碳反应的方程式为: 2NaOH + CO2
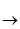 Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为______________。
Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为______________。根据以上信息,你认为____(选填“能”或“不能”)用二氧化碳来鉴别这两种溶液。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列装置回答问题:
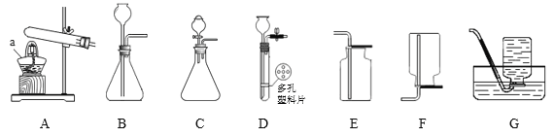
① 写出标号仪器名称:a ______________.
② 用氯酸钾在装置A中制氧气,若试管口有水珠出现,此现象是______(选填“物理”或“化学”)变化引起的。
③ 用粉末状碳酸钙与稀盐酸反应制二氧化碳,可使反应平稳进行的发生装置是_________,写出该反应的化学方程式_______________。收集二氧化碳和氧气都可用E装置的原因是_______________。
④ 探究催化剂的种类对过氧化氢分解速率的影响,实验数据如下表。(其他影响实验的因素均相同)
编号
过氧化氢溶液质量/克
催化剂质量/克
待测数据/秒
实验1
100.0
MnO2 0.2
t1
实验2
100.0
CuO X
t2
Ⅰ.表中X的数值应是______。
Ⅱ.表中的待测数据指测量收集相同体积氧气所需时间,若t1____(选填“>”、“<”或“=”)t2,则MnO2的催化效果优于CuO。或者还可以测量__________,也能达到实验目的。
Ⅲ.测得实验1中完全反应后生成氧气1.6克,求过氧化氢溶液的溶质质量分数是__________。(根据化学方程式计算)
-
科目: 来源: 题型:
查看答案和解析>>【题目】如下图装置进行木炭、一氧化碳与氧化铜反应的实验,请回答。

(1)图1实验的名称是木炭 __________(选填“氧化”或“还原”)氧化铜。A中反应的化学方程式是________。实验结束时,先拔去单孔塞,马上停止加热,试管内可能看到的现象是______ 。
(2)图2实验中,先通一会儿一氧化碳后,C处加热反应开始,此时E处_______(选填“有”或“没有”)火焰。实验结束时先停止C处加热,待___时停止通一氧化碳,目的是____。
相关试题

