【题目】在今年化学实验操作考试“探究纯碱的性质”中,同学们做了如图所示的四组实验,并将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中。考试结束后,某兴趣小组发现大烧杯底部有沉淀,上层溶液呈红色。为了探究上层溶液的成分,进行了以下实验。

【提出问题】大烧杯中的上层溶液中除了含有水和酚酞外,还含有哪些离子?(假设难溶物质、水和酚酞均不会解离出离子)
【猜想假设】小明认为上层溶液中一定含有Na+、CO![]() 、H+、Cl-、Ba2+、Ca2+、OH-七种离子,你认为上层溶液中含有的离子最多可能有几种,它们分别是__________________(填离子符号)。
、H+、Cl-、Ba2+、Ca2+、OH-七种离子,你认为上层溶液中含有的离子最多可能有几种,它们分别是__________________(填离子符号)。
【分析讨论】(1)小红认为上层溶液中一定不含有H+,因为上层溶液呈红色。请你分析上层溶液中不含有H+的另外一个理由___________________________________________。
(2)小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一定不含有CO![]() 。小红认为他的结论不正确,原因是________________。
。小红认为他的结论不正确,原因是________________。
【设计实验】为进一步确定上层溶液中是否含有CO![]() ,请你和小红一起参与下列探究:
,请你和小红一起参与下列探究:
实验操作 | 实验现象 | 实验结论 |
取大烧杯中上层溶液少许于一支试管中,滴加过量的BaCl2溶液,静置 | ①_____________________ ②试管中的上层溶液仍是红色 | ①大烧杯中上层溶液中一定含有CO ②同时还能得出大烧杯中的上层溶液中一定含有的离子是________(填离子符号) |
【实验结论】大烧杯中的上层溶液中一定含有的离子是____________________(填离子符号)。
参考答案:
【答案】 Na+、Cl-、Ba2+、Ca2+、OH- 大烧杯底部有碳酸盐沉淀,氢离子不能与之共存 溶液中可能含有氢氧化钡和氢氧化钙,加入的盐酸会先与这些碱发生反应,因而看不到气体生成 有白色沉淀生成 OH- OH-、Na+、CO![]() 、Cl-
、Cl-
【解析】【猜想假设】将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中,上层溶液呈红色,说明溶液呈碱性,故一定含有氢氧根离子,不含有氢离子;大烧杯底部有沉淀,Ba2+、Ca2+与CO32-反应能产生碳酸钡、碳酸钙沉淀,上层溶液中Ba2+、Ca2+与CO32-不能共存,故上层溶液中含有的离子最多可能有5中,它们分别是Na+、Cl-、Ba2+、Ca2+、OH--;【分析讨论】(1)小红认为上层溶液中一定不含有H+,因为上层溶液呈红色.上层溶液中不含有H+的另外一个理由氢离子和氢氧根离子不能共存;(2)小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一定不含有CO32-.小红认为他的结论不正确,原因是:酸碱优先反应,如果所加盐酸过少,被碱全部消耗,没与CO32-反应;【设计实验】与氯化钡反应生成白色沉淀的是碳酸根离子和硫酸根离子,取大烧杯中上层溶液少许于一支试管中,滴加过量的BaCl2溶液,静置,①有白色沉淀生成,说明大烧杯中上层溶液中一定含有CO32-;②试管中的上层溶液仍是红色,说明溶液呈碱性,同时还能得出大烧杯中的上层溶液中一定含有离子是OH-;【实验结论】大烧杯中的上层溶液中一定含有的离子是CO32-、OH-。
-
科目: 来源: 题型:
查看答案和解析>>【题目】经过一年的学习,大家已知道日常生活中的一些变化,不是物理变化,就是化学变化。其中下列各组变化中,全部都属于化学变化的是
A.酒精挥发、酒精燃烧 B.动物的呼吸作用、水分蒸发
C.剩饭变馊、铁锅生锈 D.木头做成家具、棉花纺线织成布
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质的性质决定其保存方法.氢氧化钠固体必须密封保存的主要原因是
A.白色固体
B.有腐蚀性
C.易吸收水分
D.能与空气中的二氧化碳反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】氨碱法制纯碱的工业流程如下:

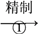
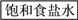
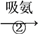



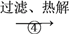
(1)最终所得纯碱主要成分的化学式是________,它属于________(填“酸”“碱”或“盐”),该产品易溶于水,溶液显________性。
(2)由步骤③所得的碳酸氢钠在生产和生活中有许多重要用途,在医疗上,它是治疗________过多的药剂之一。
(3)试写出步骤④中发生反应的化学方程式________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某碳酸钠样品中混有少量氯化钠,根据如图所示信息计算该样品中碳酸钠的质量分数。(计算结果精确到0.1%)(反应的化学方程式:CaCl2+Na2CO3===CaCO3↓+2NaCl)
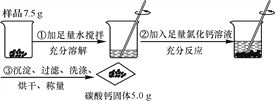
-
科目: 来源: 题型:
查看答案和解析>>【题目】把质量相同的浓盐酸和浓硫酸,分别敞口置于天平的左右盘上,一段时间后指针
A. 指向左边 B. 指向右边 C. 仍然平衡 D. 无法判断
-
科目: 来源: 题型:
查看答案和解析>>【题目】氢氧化钠溶液和二氧化碳反应没有明显现象,为验证CO2与NaOH能够发生反应,某同学按右图组装实验装置,并进行实验。
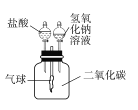
(1)有时药品滴加顺序会影响实验现象。如果观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是________(填序号)
A.先加入盐酸,再加入氢氧化钠溶液 B.先加入氢氧化钠溶液,再加入盐酸
(2)请解释气球“先膨胀”的原因:______________。
(3)写出气球“后变瘪”的化学方程式________________。
相关试题

