
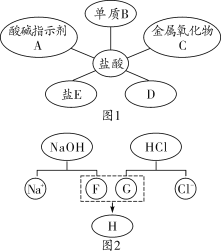
【题目】盐酸是实验室常用的试剂,也是重要的化工原料,茜茜同学归纳出盐酸的五条化学性质(如图1所示,连线表示相互反应);林林同学为表示反应实质绘制了图2。
请根据图示回答下列问题。
(1)如图1所示。①若将紫色石蕊溶液滴加到盐酸中,溶液变_____色。
②B不可能是_____(填序号)。
a、Mg b、Fe c、Ag d、Zn
③若C为铁锈的主要成分,C与盐酸反应的化学方程式是_____。
④D所表示的物质类别是_____。
⑤若E为碳酸钠,D与E反应的化学方程式是_____。
(2)如图2所示。该图描述了氢氧化钠溶液与盐酸反应的微观实质。在图2中,F、G、H处应填入微粒的化学符号依次为_____,写出该反应的化学方程式_____。
(3)向稀盐酸中分别逐渐加入下列物质,溶液pH几乎不发生变化的是_____(填序号)。
A AgNO3固体
B 浓盐酸
C Ca(OH)2固体
D H2O
【答案】红 c Fe2O3+6HCl=2FeCl3+3H2O 碱 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH(合理即可) OH-、H+、H2O HCl+NaOH=NaCl+H2O A
【解析】
(1)①若将紫色石蕊溶液滴加到盐酸中,盐酸会使紫色石蕊溶液变成红色;②只有在金属活动性顺序中排在氢前的金属才能与酸发生反应,银排在氢后,所以不能与酸反应,因此B不可能是银;③铁锈的主要成分为氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;④酸还能与碱发生反应,所以D为碱;⑤若E为碳酸钠,D可为氢氧化钙、氢氧化钡等,反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH等。(2)氢氧化钠与盐酸反应的实质是氢氧根离子和氢离子结合生成水分子,所以F、G、H处分别为OH-、H+、H2O;该反应是氢氧化钠与盐酸反应生成氯化钠和水,反应的化学方程式为HCl+NaOH=NaCl+H2O。(3)硝酸银与稀盐酸反应生成氯化银沉淀和硝酸,氢离子数目没有改变,溶液pH几乎不变,A正确;加入浓盐酸会使酸性增强,溶液pH变小,B错误;氢氧化钙会中和稀盐酸中的氢离子,使溶液pH变大,C错误;水会稀释稀盐酸,使溶液的pH变大,D错误。


科目:初中化学 来源: 题型:
【题目】下列实验设计能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
A | 除去铁制品表面的铁锈 | 将铁制品长时间浸泡在稀盐酸中 |
B | 检验某溶液中是否含有 | 滴加氯化钡溶液 |
C | 区分盐酸、氯化钾、氯化钙三种溶液 | 滴加碳酸钠溶液 |
D | 分离氯化钠和氯化镁晶体 | 溶解,加入适量氢氧化钠溶液,过滤,蒸发结晶 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为验证“酸的化学通性”,某班同学在实验室进行如下实验。请分析并回答相关问题:
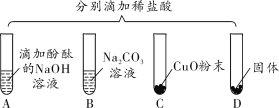
(1)写出能证明A中反应发生的现象_____。
(2)写出上述实验中酸与金属氧化物反应的化学方程式_____。
(3)要全面验证酸的化学通性,D试管中能与酸反应的固体单质是_____(写一种即可)。
(4)实验完成后,将全部废液倒入废液缸内,测得pH=2,则废液中所含溶质最多有_____种(溶质不计指示剂与气体)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2017石家庄质检二模)某研究性学习小组欲测定生铁中的含碳量,采用的方法如下:取生铁样品5.8 g,把50 g稀硫酸分5次加入到生铁样品中,实验过程中的数据见下表(假设生铁样品中只含铁和碳)。请计算:
加入硫酸的次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
稀硫酸质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | 4.4 | 3.0 | 1.6 | 0.2 | 0.2 |
(1)5.8 g生铁中含碳的质量为________g。
(2)所用稀硫酸中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下,向加有酚酞试液的氢氧化钠溶液中滴加稀盐酸如图1所示,并不断搅拌。烧杯中溶液温度变化如图2所示。
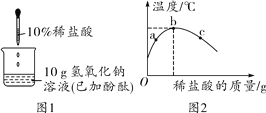
关于该实验有如下说法:
①a点时,溶液中所含溶质为HCl和NaCl
②从b→c,溶液的pH逐渐变大 ③c点时,溶液为无色 ④取c点溶液,加入锌粒有气泡产生,说明原氢氧化钠溶液中含有碳酸钠 ⑤该实验说明氢氧化钠和盐酸反应放热。以上说法正确的是( )
A. ①② B. ①⑤ C. ③④ D. ③⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2018深圳改编)某Ca(OH)2样品已变质,且只有CaCO3一种杂质,取10 g该样品,将样品放入到足量的盐酸中,所得数据如下表:
时间/s | t0 | t1 | t2 | t3 |
烧杯中剩余物质的质量/g | 280 | 278.9 | 277.8 | 277.8 |
求:(1)生成二氧化碳的质量为_____g。
(2)该样品中Ca(OH)2的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室有一瓶氢氧化钠溶液,瓶上标签内容如图所示,某同学向盛有20 g盐酸和氯化镁组成的混合溶液中慢慢滴加该氢氧化钠溶液并振荡,当加入20 g氢氧化钠溶液时才开始产生沉淀,直到60 g时不再产生沉淀。

(1)开始不产生沉淀的原因是_____。
(2)计算原混合溶液中氯化镁的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(有关反应条件的探究) (2018唐山路北区二模)唐山市实验加试有一个题是金属的性质,验证铁与盐酸、硫酸铜溶液的反应。实验练习期间废液缸中过滤网上的铁钉生锈很快,为什么这里的铁钉更容易生锈呢?
(观察与思考)
(1)铁生锈的条件是_________。
(2)走进实验室,空气中弥漫着盐酸的刺激性气味,这因为盐酸具有________。
(3)废液缸中过滤网上的铁钉都或多或少的沾有盐酸或硫酸铜溶液。
(作出猜想)是不是盐酸或硫酸铜溶液能促进铁生锈呢?
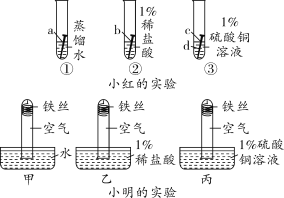
(设计实验)小红和小明分别设计如图所示的实验,并于一段时间后进行观察。
(进行实验)
小红的实验:按如图所示进行实验。
铁钉上c比d点生锈多,原因是d点的铁钉_________________。
铁钉上b和c点均比a点生锈多,得出的结论是_________。
小明的实验:他使试管中的铁丝分别沾上相应的水槽中的液体,然后进行图中所示的实验。
丙比乙试管中液面上升更高,可能的原因是(用化学方程式表示)_____________。
小明得出了硫酸铜溶液能促进铁生锈的结论,他观察到的实验现象是_____________。
(得出结论)经过反复讨论得出结论:稀盐酸和硫酸铜都能促进铁生锈。
(实验反思)
(1)实验加试练习过后,需要把用后的铁钉冲洗、晾干保存,可以防止其过快生锈。
(2)实验加试练习期间,即使是放在烧杯中的新铁钉也容易生锈,原因是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】几种物质的溶解度如下表所示,根据表中信息回答下列问题:
温度/℃ 溶解度/g | 0 | 20 | 40 | 60 | 80 | 100 |
Li2CO3 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
NaCl | 35.7 | 36 | 36.6 | 37.3 | 38.4 | 39.8 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 245 |
(1)溶解度随温度升高而减小的是_______ 。(填化学式)
(2)硝酸钾固体中混有少量氯化钠固体,欲分离该混合物获得更纯的硝酸钾, 可在较高温度时制成饱溶液,然后_______。
(3)配制 20℃时氯化钠的饱和溶液 68g,需水_______ g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com