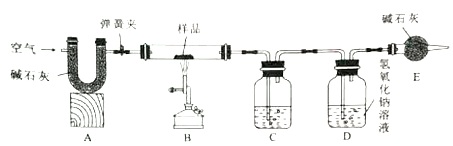
【题目】热水瓶用久后,瓶胆内壁常附着意层水垢,其成份是碳酸钙、氢氧化镁及少量水。实验室现有一瓶水垢样品,为沉淀其中各成份的质量分数,某化学兴趣小组的同学利用下图所示装置进行实验(该装置气密性良好.A、C、D中所装药品足量)。已知:碱石灰是氧化钙和氢氧化钠的混合物:加热条件下,氢氧化镁易分解,反应的化学方程式为:Mg(OH)2![]() MgO+H2O↑。
MgO+H2O↑。
部分实验步骤如下:
I.将质量为m的样品装入装置B的玻璃管中,按图连接好装置,关闭弹赞夹,给样品加热;
II.待样品完全反应,先打开弹赞夹通入空气,再熄灭酒精喷灯,直到玻璃管冷却:
III.实验完毕,测得装置C、D中的液体质以分别增加了m1、m2;
IV.根据实验所测数据计算该样品中碳胶钙、氢氧化镁和水的质量分数。
请回答下列问题:
(1)装置C中所装药品为___________。
(2)装置D中发生反应的化学方程式为___________。
(3)该水垢样品中碳酸钙的质量分数的表达式为___________。
(4)实验反思:实验步骤不变,若没有装置A,会导致氢氧化镁的测定结果_____(填“偏大”“偏小”或“无法判断”)。
参考答案:
【答案】(1)浓硫酸(2)CO2+2NaOH=Na2CO3+H2O(3)![]() 或其它合理答案
或其它合理答案
(4)偏小
【解析】根据题中信息知,(1)装置C中所装药品为浓硫酸。(2)装置D中发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O。(3)该水垢样品中碳酸钙的质量分数的表达式为![]() ×100%。(4)实验反思:实验步骤不变,若没有装置A,会导致氢氧化镁的测定结果偏小。
×100%。(4)实验反思:实验步骤不变,若没有装置A,会导致氢氧化镁的测定结果偏小。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某校实验室有一无色澄清溶液,其中除了硝酸钠以外,可能还含有氢氧化钠、碳酸钠、硫酸钠、硝酸钡中的一种或几种。
实验活动一“探究该废液的组成。
去一定量的无色溶液,进行如下图所示实验。
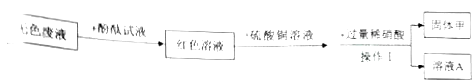
请回答下列问题:
(1)原无色废液呈______(填“酸性”“碱性”或“中性”)操作l的名称为_______。
(2)生成固体甲的化学方程式为_____________。
(3)原无色澄清废液中一定没有(写名称或化学式均可,下同)_____________。
实验活动二:处理废液得到较纯净的硝酸钠溶液。
将溶液A和原无色废液充分混合,无明显现象。接下来进行如下图所示实验。
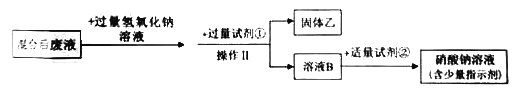
(4)混合后废液中一定含有的溶质是(指示剂除外)______,试剂①是_____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质X与Ca(OH)2水溶液发生反应的化学方程式为:X+Ca(OH)2=Y+Cu(OH)2↓,下列说法正确的是
A.X可能是酸 B.X和Y的相对分子质量之差为24
C.X可能是单质,也可能是化合物 D.Y只可能是CaCl2
-
科目: 来源: 题型:
查看答案和解析>>【题目】R是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示.某化学兴趣小组的同学进行了如图2所示实验。
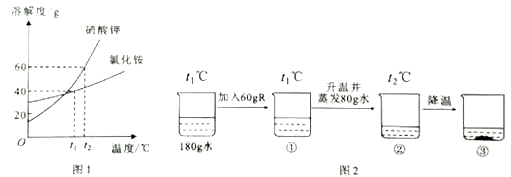
(1)t1℃时,氯化铵的济解度为______g。
(2)①的溶液中溶质质量分数为____________。
(3)根据以上信息可推出R是________(写名称或化学式均可)。
(4)关于图2中烧杯内的物质,以下几种说法正确的有_________。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使③中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的化学式书写正确的是
A.碳酸钠NaCO3 B.氢氧化钠Na(OH)2
C.氧化铁O3Fe2 D.硫酸铝Al2(SO4)3
-
科目: 来源: 题型:
查看答案和解析>>【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是

A.图中a点所示溶液中,含有的溶质是NaCl和Na0H
B.由a点到b点的pH变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列金属中,活动性最强的是
A. Mg B. Cu C. Al D. Ag
相关试题

