【题目】(9分)空气、水、金属等是重要的资源。
(1)工业上常把煤块粉碎后使其充分燃烧,其原理是 。
家中堆放杂物的纸箱着火时,可用水浇灭,其原理是 。
(2)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。
①根据铜锈的主要成分中含有氢元素,可以判断出铜生锈需要空气中的 ;根据铜锈的主要成分中含有碳元素,可以判断出铜生锈需要空气中的 。
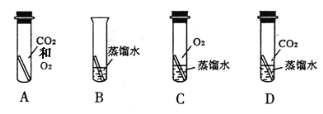
②某化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的氧气?”下图所示实验中(试管内的“![]() ”均为铜片),只需完成实验 和 即可达到探究目的(填字母)。
”均为铜片),只需完成实验 和 即可达到探究目的(填字母)。
(3)铝是世界上年产量第二的金属。
①用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,观察到熔化的铝被一层膜兜着并不滴落,产生该现象的原因是 。
②铝和氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2X 2NaAlO2+3H2↑,其中X的化学式为 。足量的稀盐酸与氢氧化钠溶液分别和等质量的铝粉充分反应,产生氢气的质量分别为m1、m2,下列有关m1、m2大小关系的说法正确的是 (填字母)。
A.m1>m2 B.m1<m2 C.m1=m2 D.无法比较
参考答案:
【答案】(1)增大燃料与空气的接触面 水可以吸收可燃物燃烧释放出的大量热,使可燃物的温度降到其着火点以下
(2)①H2O CO2 ②B D
(3)①表面氧化铝的熔点高于铝的熔点 ②H2O C
【解析】
试题分析:(1)工业上常把煤块粉碎后使其充分燃烧,其原理是:增大燃料与空气的接触面;根据灭火的原理:(1)消除可燃物(2)隔绝氧气(或空气)(3)降温到着火点以下;家中堆放杂物的纸箱着火时,可用水浇灭,其原理是:水可以吸收可燃物燃烧释放出的大量热,使可燃物的温度降到其着火点以下
(2)①根据铜锈的主要成分中含有氢元素,结合质量守恒定律,可以判断出铜生锈需要空气中的H2O;根据铜锈的主要成分中含有碳元素,可以判断出铜生锈需要空气中的CO2
②化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的氧气,就要注意控制变量,设计对比实验,故只需完成实验B和D即可达到探究目的,因为这两个实验的变量就是一个有氧气,两一个没有氧气
(3)①用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,观察到熔化的铝被一层膜兜着并不滴落,产生该现象的原因是:表面氧化铝的熔点高于铝的熔点
②根据质量守恒定律的微观解释:在化学反应前后,原子的种类、数目都不变,结合化学反应:2Al+2NaOH+2X 2NaAlO2+3H2↑,可以推出X化学式为H2O;根据化学反应方程式:2Al+2NaOH+2H2O 2NaAlO2+3H2↑中Al与H2的质量关系为9:1,而根据铝和稀盐酸反应的方程式:2Al +6HCl ===2AlCl3+ 3H2↑中Al与H2的质量关系也为9:1,故等质量的铝粉产生氢气的质量分别为m1=m2 ,故选C
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法正确的是
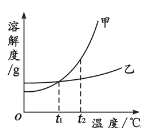
A.甲的溶解度大于乙的溶解度
B.分别将t1℃时的甲、乙的饱和溶液升温至t2℃,溶质的质量分数均增大
C.要从含有少量甲的乙溶液中得到较多的乙晶体,通常可采用降温结晶的方法
D.t2℃时,等质量的甲、乙的饱和溶液中,甲溶液中溶剂的质量更小
-
科目: 来源: 题型:
查看答案和解析>>【题目】(6分)下图中A~J是初中化学常见的物质,虚线圈中的两物质类别相同。A的浓溶液可用作干燥剂,D俗称火碱;A与G发生复分解反应生成F与H,F的水溶液呈蓝色;A与J发生置换反应生成I与E, E中金属元素的质量分数为20%。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
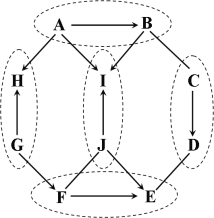
(1)写出化学式:A ,H 。
(2)写出化学方程式:
J 转化为I的反应 ,
E与D的反应 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分) 写出下列生活中熟悉的物质的化学式:
(1)人们生活中最重要的氧化物是_____;
(2)人体中胃酸的主要成分是_____;
(3)农业上用来中和酸性土壤的碱是__ _;
(4)司机驾车前饮用的饮料中不能含有_______
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)海洋是人类宝贵的自然资源,从海水中可以得到粗盐。
(1)称取5.0g粗盐,逐渐加入10mL水中,边加边用玻璃棒搅拌,一直加到粗盐不再溶解为止。还需要进行的实验步骤依次为:①称量剩余粗盐、② 、③ 、④称量精盐、⑤计算产率。
(2)下图是某工厂利用粗盐水生产纯碱的工艺流程图。
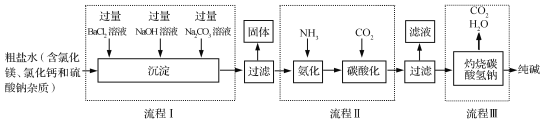
①下列说法正确的是 (填字母)。
A.流程Ⅰ中加入溶液的顺序不能改变
B.流程Ⅰ将粗盐水中的SO42-、 Mg2+、Ca2+转化为沉淀
C.流程Ⅰ后过滤得到三种沉淀
D.流程Ⅲ中发生的是分解反应
②流程II中发生的主要反应为NH3+CO2+H2O NH4HCO3 ,
NH4HCO3+NaCl NaHCO3↓+NH4Cl 。
20℃时,向100g水中加入11.7g NaCl和15.8g NH4HCO3,充分反应后,理论上从溶液中析出晶体的质量为 g(20℃时,NaHCO3的溶解度为9.7g, NH4Cl的溶解度为37.2g)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(3分)请完成下列物质归类。
(1)常见化石燃料:煤、天然气、
(2)常见集气方法:向上排空气、向下排空气、
(3)常见 :生石灰、浓硫酸、烧碱
-
科目: 来源: 题型:
查看答案和解析>>【题目】硬铝的组成金属有铝、镁、铜、锰等。已知:锰丝放入稀硫酸中,有气泡产生;锰丝放入硫酸铝溶液中,表面没有金属析出。下列有关金属的活动性强弱判断错误的是
A.Mn > Cu B.Al > Mn C.Mg > Al D.Mn > Mg
相关试题

