【题目】请用化学用语表示:
5个钾原子_____;4个铵根离子______;氦气_____;氧化铝中铝元素的化合价为+3价_____。
参考答案:
【答案】5K;4NH4+;He;![]()
【解析】
根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,因此5个钾原子表示为:5K;根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其元素符号前加上相应的数字;因此4个铵根离子表示为:4NH4+;氦是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氦气的化学式就是表示氦元素的元素符号,因此氦气表示为:He;根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此氧化铝中铝元素的化合价为+3价表示为:![]() 。
。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)用化学符号表示:
①地壳中含量最多的金属元素________,②硅原子________,③氮分子_________,
④亚铁离子______,⑤铵根_______,⑥标出过氧化氢中氧元素的化合价________。
(2)在实验室配制50g 5%氯化钠溶液后,请回答下列问题:
①配制过程的步骤是:计算、称取、量取、溶解、______。
②用已调节平衡的托盘天平称取氯化钠时,发现指针偏左,接下来的操作是______。
A.添加氯化钠 B.减少氯化钠 C.调节平衡螺母 D.添加砝码
③在量取水的体积时,若仰视读数,则会导致氯化钠溶液的溶质质量分数____(填“<”或“>”)5%。
④在溶解步骤中需要的仪器有________、_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A元素和B元素形成化合物的化学式为AxBy , 已知A、B两元素的相对原子质量之比为27:16.上述化合物中A、B两元素的质量比9:8,则x:y=________若B的相对原子质量为8,则化合物AxBy的相对分子质量为________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形。下表为元素周期表的部分元素的相关信息,利用下表回答相关问题
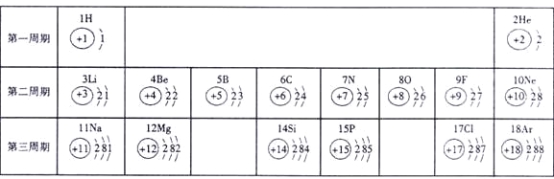
(1)请画出16号元素原子结构示意图 化学反应中该原子比较容易
(填“得到”或“失去”)电子变成离子;
(2)
 表示的是 (填离子符号);
表示的是 (填离子符号);(3)上表中最活泼的金属元素与地壳中含量最多的元素组成的化合物是
(填化学式,任意填写一种);
(4)上表中第二、三周期元素最外层电子数的变化规律是___ _。
-
科目: 来源: 题型:
查看答案和解析>>【题目】随着经济的发展,能源与环境成为人们日益关注的问题.
(1)煤、天然气和石油常称为化石燃料.其中天然气的主要成分为________(填名称).
(2)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体.为控制二氧化碳的排放量,要充分利用和开发太阳能、核能及________(填1种即可)等新能源.
(3)甲烷和水反应也可以制水煤气,其反应的微观示意图如下所示:
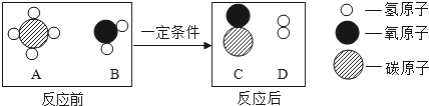
①该反应的化学方程式是________.
②下列对该反应的叙述正确的是 ________(填序号).
a.反应前后分子个数不变
b.该反应中含氢元素的化合物有2种
c.反应前后各元素的化合价均不变
d.若有24g的A完全参加反应,则生成D的质量为9g.
-
科目: 来源: 题型:
查看答案和解析>>【题目】2017年5月18日,中国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。可燃冰是在高压低温环境条件下,水分子笼中装有甲烷分子而成的“冰块”,可直接点燃。己知某种可燃冰的化学式为:CH4·8H2O。请回答:
(1)这种可燃冰中含有______种元素:原子个数比:C:H:O=________;
(2)这种可燃冰中甲烷的质量分数为________%;936g(约1升)该可燃冰常温下可释放出____升甲烷(常温下甲烷密度为0.72g/L)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是
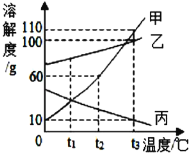
A. t1℃时,甲的溶解度等于丙的溶解度
B. t2℃时,100 g 甲的饱和溶液中含有 60 g 甲物质
C. 若甲中含有少量的乙,则提纯甲的方法是蒸发结晶
D. t1℃时,将甲、乙、丙三种物质的饱和溶液同时升温到 t3℃,不考虑水分蒸发,所得溶液中溶质的质量分数最大的是乙
相关试题

