【题目】化学课外小组的同学想要用一氧化碳气体(含有少量杂质二氧化碳和水蒸气)测定样品中氧化铁的质量分数,装置如图所示,回答下列问题:
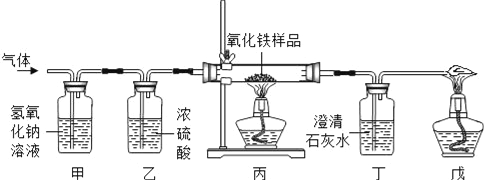
(1)乙装置的作用是____________.
(2)丙装置中反应的化学方程式是__________________.
(3)丁装置中的现象是_______________.
(4)戊装置的作用是_______________.
(5)要生产1000t含杂质3%的生铁,需要含Fe2O390%的铁矿石______t(保留整数).
参考答案:
【答案】 吸收水蒸气 3CO+Fe2O3![]() 2Fe+3CO2 石灰水变浑浊 处理尾气 1540t
2Fe+3CO2 石灰水变浑浊 处理尾气 1540t
【解析】本题考查了二氧化碳和水蒸气的清除方法和根据化学方程式的计算,在进行计算时,代入的数据一定要是参加反应和生成的纯物质的质量,对不纯物质的质量要处理后才能代入计算。。
(1)浓硫酸能吸收气体中的水分,故乙装置的作用是:吸收水蒸气;
(2)一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,化学方程式是:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(3)生成的二氧化碳能使澄清石灰水变浑浊,故丁装置中的现象是:石灰水变浑浊;
(4)一氧化碳有毒,不能直接排放到空气中,需进行尾气处理,故戊装置的作用是处理尾气;
(5)需要含Fe2O390%的铁矿石质量为x
3CO+Fe2O3![]() 2Fe+3CO2,
2Fe+3CO2,
160 112
90%×x 1000t×(1﹣3%)
![]() =
=![]()
x=1540t
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类社会的发展离不开金属材料,用你学到的化学知识分析下列问题.
(1)物质的性质决定物质的用途.由于铜具有良好的______性,所以铜常用于制作导线.
(2)常见的三种金属被发现和使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟下列______(填序号)关系最大.
①地壳中金属元素的含量;②金属的熔点;③金属的活动性
(3)铝在空气中表现良好的抗腐蚀性能,用化学方程式表示其原因______.
(4)有铜和氧化铜的混合物10g,通入氢气加热至完全反应,冷却后称量剩余固体的质量为8.4g.
①写出氧化铜与氢气反应的化学方程式______________________.
②该混合物中氧化铜的质量为______g.
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列变化中,属于物理变化的是 ( )
A. 米饭变馊 B. 湿衣服晾干 C. 火药爆炸 D. 铁锅生锈
-
科目: 来源: 题型:
查看答案和解析>>【题目】某固体混合物A中可能含硫酸钠、碳酸钠、硝酸钡、氯化铵等物质中的若干种.按如图所示进行实验,出现的现象如图所述(实验过程中所有发生的反应都恰好完全反应).
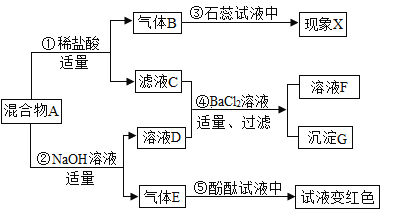
根据实验过程和发生的现象做出判断,填写以下空白:
(1)现象X是______,气体E的化学式为______.
(2)固体混合物A中,肯定存在的物质是______(写化学式).
(3)写出步骤①中发生反应的化学方程式______________________.
(4)仅根据上述实验现象,还不能确定混合物A的组成.为确定混合物A的成分,可用沉淀G再进行实验.方法是取沉淀G少许,向其中加入足量稀硝酸,若沉淀全部溶解,则固体混合物A中不含_____________(化学式).
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学家在合成超导材料时,偶然制得了在自然界中尚未发现的紫色合成物质BaCuSi2O6,它由______种元素组成,一个分子中有______个原子。写出与该物质相同价态硅元素的氧化物的化学式________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列做法有利于保护环境的是
A. 工厂废气直接排放 B. 废旧电池回收处理
C. 生活污水任意排放 D. 随意丢弃塑料袋
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列对水的叙述正确的是
A. 水的三态变化,能实现水的自身净化和水资源的重新分配
B. 水的三态变化,是由于水分子的体积改变
C. 过滤和吸附能除去水中所有的杂质
D. 水是由氢气和氧气组成
相关试题

