【题目】图中A—G是初中化学常见的物质,且分别是由H、C、O、Na、S、Cu中的一种或几种元素组成。A、C为单质;B、D、E由两种元素组成,其中E中两种元素质量比为1:8;F、G、H由三种元素组成,H可用于含铅蓄电池中。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
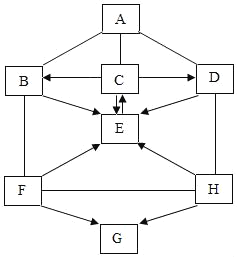
(1)写出化学式:E____________。
(2)写出B物质的一种用途:____________。
(3)写出H和D反应的化学方程式_____________。
(4)写出E→C反应的化学方程式_____________。
参考答案:
【答案】 H2O 灭火(化工原料、气体肥料等合理即可) CuO + H2SO4 = CuSO4 + H2O 2H2O通电2H2↑ + O2↑
【解析】A—G是初中化学常见的物质,且分别是由H、C、O、Na、S、Cu中的一种或几种元素组成。H由三种元素组成,H可用于含铅蓄电池中,H应为硫酸,E由两种元素组成,其中E中两种元素质量比为1:8,E应为水;D由两种元素组成,并且可以与H硫酸反应,可知D应为氧化铜,C为单质,C可以生成E水和D氧化铜;
C应为氧气;F由三种元素组成,可以与H硫酸反应,可知F应为氢氧化钠,F和H都可以得到G,G应为硫酸钠,B由两种元素组成,可以与F氢氧化钠反应,B应为二氧化碳,A同时可以与ACD反应,A为碳。
(1)E为水,化学式为:H2O;
(2)B为二氧化碳,可以用于灭火、化工原料、气体肥料等;
(3)H为硫酸、D是氧化铜,反应的化学方程式CuO + H2SO4=CuSO4 + H2O;
(4)E为水,C为氧气,电解水可以得到氧气,化学方程式为:2H2O ![]() 2H2↑ + O2↑。
2H2↑ + O2↑。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关氧气的叙述,正确的是
A、红磷在氧气中燃烧时产生大量白雾
B、在任何情况下,氧气都是无色气体
C、硫在氧气中燃烧,发出微弱的淡蓝色火焰
D、铁生锈是缓慢氧化
-
科目: 来源: 题型:
查看答案和解析>>【题目】某学生用量筒量取液体,将量筒平放且面对刻度平视测量。初次视线与量筒内凹液面的最低处保持水平,读数为30mL,倒出部分液体后,仰视凹液面的最低处,读数为5mL,则该学生实际倒出液体的体积是
A.大于25mL B.小于25mL C.等于25mL D.无法确定
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表是氯化钠、硝酸钾在不同温度时的溶解度。据此判断:下列说法不正确的是
温度/℃
10
20
30
40
50
60
溶解度/g
氯化钠
35.8
36.0
36.3
36.6
37.0
37.3
硝酸钾
20.9
31.6
45.8
63.9
85.5
110
A. 氯化钠和硝酸钾的溶解度曲线在20℃~30℃温度范围内会相交
B. 在20℃时, 向68g饱和氯化钠溶液中加入32g水,此时溶液中溶质的质量分数为18%
C. 从含有少量氯化钠的饱和硝酸钾溶液中得到较多的硝酸钾晶体,可采用冷却热饱和溶液使其结晶的方法
D. 分别将20℃时一定质量的饱和氯化钠溶液、饱和硝酸钾溶液升温至40℃,此时硝酸钾溶液中溶质的质量分数大于氯化钠溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】合理利用资源和保护环境是我们关注的问题。请回答:
(1)化石燃料是一类重要能源,它包括煤、石油和__________。
(2)煤作为燃料给我么们带来了益处,但对环境也造成了不良影响。
①下列关于酸雨的叙述正确的是__________(填序号)
A. 腐蚀大理石雕像 B. 是由二氧化碳和二氧化硫引起的
C. 酸化土壤 D. 对海洋生物没有影响
②使燃料充分燃烧,通常除了考虑燃烧时要有足够的空气,还要考虑___________;
(3)为减少污染,城市公共交通正大力推广使用压缩天然气或液化石油气为动力。某种清洁燃料的主要成份是A,一定质量的A物质在B物质中充分燃烧,如下表所示)。
物 质
A
B
C
D

分子示意图
?


反应前质量/g
44
?
0
0
反应后质量/g
0
0
132
72
①在上述反应中提供氧、具有氧化性的物质为______________。(写化学式)
②A物质中各元素的质量比为________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】完成下列基础化学实验。
Ⅰ.根据下列实验装置图,回答有关问题:
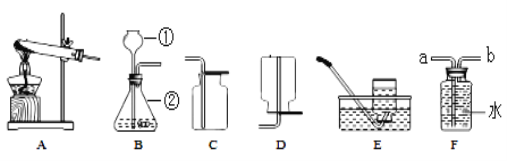
(1)写出装置图中标号仪器的名称:①_____________,②___________。
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为________________________,可选用的发生装置是______。如用E装置收集氧气,当集气瓶中的水排完之后,_______________,缓慢的移出水槽,正放在桌子上。
(3)实验室用大理石和稀盐酸制取二氧化碳时的化学方程式为_______________。
(4)选用F收集氢气时,氢气应从__________(填“a”或“b”)端进入。
Ⅱ.如何证明盐酸与碱发生了化学反应?某化学兴趣小组做了如下两个实验。
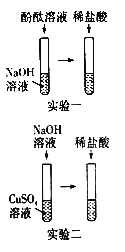
实验一:向NaOH溶液中滴入几滴酚酞溶液,振荡,继续加入稀盐酸,观察到__________________,可证明盐酸与氢氧化钠能发生反应。
实验二:向CuSO4溶液中滴入NaOH溶液,观察到的反应现象为___________;继续滴加稀盐酸,看到_____________(反应现象),也证明了盐酸与碱能发生反应。
实验结束后,小组同学对实验一中试管内的无色溶液成分展开了讨论。
【提出问题】实验一结束后,试管内的溶液的溶质除酚酞外还有什么?
【猜想假设】猜想一:NaCl和HCl 猜想二:NaCl
【实验设计】若要证明猜想一成立,下列试剂中不能达到实验目的的是_________。
A.紫色石蕊溶液 B.Cu C.AgNO3 D.Na2CO3
【讨论交流】小莹同学认为滴入NaOH溶液,也能证明猜想一成立,你认为小莹同学的方案是否可行并说明理由____________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有关物质组成及化学规律的发现对化学的发展做出了重要贡献。
(1)法国化学家拉瓦锡为化学学科的发展做出了巨大贡献,下列有关发现与他有密切关系的是_____。
A. 空气的组成 B. 质量守恒定律 C. 水的组成 D. 酸碱指示剂
(2)在密闭容器内加入下列两种物质,并称量加入前后的总质量(含密闭容器),能验证质量守恒定律的是_____________(填标号)。
A. 蔗糖和水 B. 氯化钠溶液和硝酸钾溶液 C. 氯化钡溶液和稀硫酸
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。
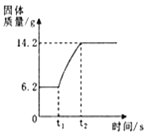
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是___________。
②该反应的化学方程式为________________。
③参加反应的氧气质量为___________g。
(4)某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。
查阅资料可知Mg、Mg3N2能发生如下反应:
①2Mg+O2 △ 2MgO; ②3Mg+N2 △ Mg3N2; ③2Mg+CO2 △ 2MgO+C
④Mg+H2O △ MgO+H2↑ ⑤Mg3N2+6H2O 3Mg(OH)2↓+2NH3↑
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。回答下列问题:
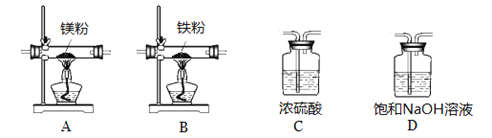
①连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是______(填装置序号)。D装置中发生反应的化学方程式为___________。
②通气后,如果同时点燃A、B装置的酒精灯,对实验结果有何影响?_________。
③设计一个实验,验证产物是否含氮化镁:
实验操作和实验现象
实验结论
________________________
产物中含有氮化镁
④思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N的质量,请给出合理的解释_______________。
相关试题

