【题目】兴趣小组某同学在做铜与硝酸银溶液反应的实验,当观察到铜丝表面有银白色固体出现时,发现试管内溶液未显蓝色,与所学知识不符。组内同学即展开讨论,认为溶液未显蓝色是因为铜离子的浓度太小,于是对铜离子浓度太小的原因进行了如下猜想:
猜想一:硝酸银溶液浓度不够大。
猜想二:铜丝中含有比铜活泼的金属
猜想三:_____________________
(实验验证)
(1)验证猜想一:你的方案是____________________。
(2)验证猜想二:取上述相同的铜丝,选择一种酸或盐溶液在相同条件下进行实验,观察实验现象,得出结论。
请你在矩形内画出实验装置图,并标出所选物质。
 _____________
_____________
(3)验证猜想三:进一步实验______________
参考答案:
【答案】 略 略 略 略
【解析】铜与硝酸银溶液反应的时间太短,或反应速率太慢,都可能导致反应一定时间后,溶液中的铜离子浓度太低;【实验验证】(1)根据控制变量的原则,验证猜想一:方案是其它条件不变,用浓度更大的AgNO3溶液,重复实验,观察实验现象,得出结论;(2) 金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。验证猜想二:取上述相同的铜丝,分别和硫酸或硫酸铜溶液在相同条件下进行实验,观察实验现象,如果有气泡产生或硫酸铜的溶液颜色变浅或变色,可证明铜丝中有比铜活泼的金属,反之,没有; 实验装置如图: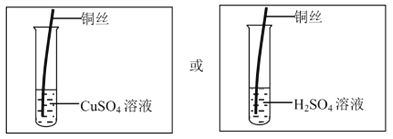
-
科目: 来源: 题型:
查看答案和解析>>【题目】向20g,铜锌合金中不断加入一定溶质质量分数的稀盐酸,加入稀盐酸的质量与固体质量的关系如图所示。请计算:
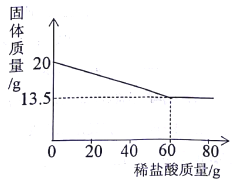
(l)合金中锌的质量分数为____。
(2)所用稀盐酸的溶质质量分数为_____________。(计算结果保留一位小数)
-
科目: 来源: 题型:
查看答案和解析>>【题目】硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是
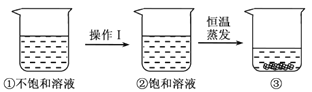
A. 操作I一定是降温 B. 操作I一定是加溶质
C. ①与③的溶质质量一定相等 D. ②与③的溶质质量分数一定相等
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学反应的实质是构成物质分子的原子重新进行组合,形成新分子的过程。如图是在密团容器中某化学反应过程的微观示意图。据图回答:
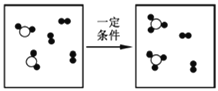
(1)参加反应的“
 ”与“
”与“ ”的分子个数比为_________。
”的分子个数比为_________。(2)该反应的基本反应类型是________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】最近,国外研究人员发明了一种在锌原子周围聚合咪唑钠(C2H3N2Na)和苯并咪唑(C7H6N2)两种有机物的新型玻璃,与硅原子周围聚合各种无机物的传统玻璃相比,其有更好的透光性和延展性。
(1)硅元素与锌元素之间最根本的区别是______________不同。
(2)新型玻璃具有更好的延展性,这属于物质的_______(选填“物理”或“化学”)性质。
(3)请列式计算咪唑钠(C2H3N2Na)中碳元素的质量分数______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】大理石是含杂质的碳酸钙,因具有美丽花纹面被广泛用于建筑物外墙、内壁的贴面和地面铺设。某同学想测出大理石样品中碳酸钙的含量,进行了如下实验和分析。
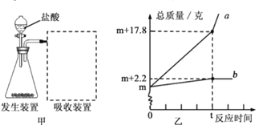
(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(杂质不参加反应),产生的气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是_______________。
(2)反应前,测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为m克,实验后,根据实验数据绘了图乙,曲线a、b分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线b分析计算出大理石样品中碳酸钙的质量______________。
(3)请综合分析曲线a、b,计算出实验中所用盐酸的溶质质量分数为___________。(结果精确到0.1%)
(4)计算后,该同学对上述实验进行了反思。他认为分液漏斗中选用的盐酸浓度偏大,会对实验结果造成较大影响,其原因是______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列反应中属于复分解反应的是
A. 2Mg+ O2
 2MgO B. Cu+2AgNO3=Cu(NO3)2+2Ag
2MgO B. Cu+2AgNO3=Cu(NO3)2+2AgC. CuCl2
 Cu+Cl2↑ D. 2NaOH+H2SO4=Na2SO4+2H2O
Cu+Cl2↑ D. 2NaOH+H2SO4=Na2SO4+2H2O
相关试题

