【题目】(8分)工业上生产电路板及处理废液的工艺流程如下:
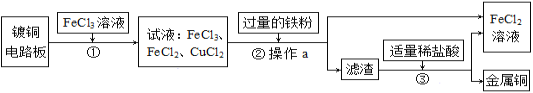
(1)操作a是 。
(2)步骤②加入过量铁粉,除能与废液中的FeCl3反应外,还可发生反应的化学方程式为 。
(3)步骤③加入稀盐酸,充分搅拌,当观察到 现象时,说明滤渣只剩铜。步骤③发生的化学方程式为 。
(4)步骤②③所得FeCl2可与一种单质发生化合反应,生成可循环使用的FeCl3。请写出该反应的化学方程式 。
参考答案:
【答案】(1)过滤(2)Fe + CuCl2 == Cu + FeCl2
(3)没有气泡冒出 Fe + 2HCl == FeCl2 + H2↑。
(4)2FeCl2+ Cl2==2FeCl3
【解析】
试题分析:操作a能够得到固体所以是过滤;步骤②加入过量铁粉,除能与废液中的FeCl3反应外,还可发生反应的化学方程式为Fe + CuCl2 == Cu + FeCl2;步骤③加入稀盐酸,充分搅拌,当观察到没有气泡冒出说明滤渣只剩铜;步骤③发生的化学方程式为Fe + 2HCl == FeCl2 + H2↑;步骤②③所得FeCl2可与一种单质发生化合反应,生成可循环使用的FeCl3。该反应的化学方程式2FeCl2+ Cl2==2FeCl3。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(13分)请根据所提供的试剂按要求填空:
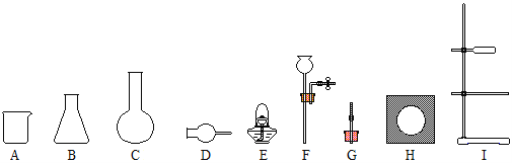
(1)仪器名称:B ,E ,H 。
(2)制取蒸馏水的发生装置需用到C、I外,还有上图中的 ,实验中必须在C中加入碎瓷片,目的是 。
(3)用上图中的A和 可组成“随时控制反应发生和停止”的气体发生装置,本装置可用于实验室制 或 气体。
(4)B和F组成的发生装置可用于实验室制CO2,写出反应的化学方程式 。检查本装置气密性的操作:在导管末端夹紧止水夹, ,静置,若 ,则气密性良好。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学在一定温度下进行硝酸钾的溶解实验,实验数据如下表:
实验序号
实验1
实验2
实验3
实验4
水的质量(g)
100
100
100
100
加入硝酸钾的质量(g)
80
100
120
140
溶液质量(g)
180
200
210
210
根据上述实验数据,下列叙述正确的是( )
A.实验1所得溶液的溶质质量分数为80%
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,硝酸钾饱和溶液的溶质质量分数为52.4%
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制取和收集氧气有如下的操作:①点燃酒精灯,给试管加热 ②熄灭酒精灯 ③检查装置气密性④将氯酸钾与二氧化锰混合均匀装入试管,塞紧试管塞,固定于铁架台上⑤收集氧气 ⑥将导管从水槽中取出。其正确的操作程序是
A.③④①⑤⑥② B.③④①⑤②⑥ C.④①③⑥②⑤ D.④①⑤②⑥③
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)新药左旋氧氟沙星(C18H20FN3O4)可用于治疗敏感菌引起的呼吸道感染,其说明书中部分内容如下图。

(1)左旋氧氟沙星由 种元素组成,属于 (填“有机物”或“无机物”)。
(2)左旋氧氟沙星中氧元素的质量分数是 (精确到0.1%)。
(3)成人呼吸道感染患者,一个疗程最少应服用左旋氧氟沙星 g。
(4)从保存方法看,左旋氧氟沙星可能具有 的化学性质。
-
科目: 来源: 题型:
查看答案和解析>>【题目】图是某同学配制一定质量、溶质质量分数为0.9%的生理盐水的全过程:
(1)请找出图中的错误:

①________________;②________________;③________________.
(2)如果配制的生理盐水中NaCl的质量分数小于0.9%,则可能造成误差的原因有(至少举出三点):①________;②________;③________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化合物化学式为R(H2PO4)2,当P元素显+5价时,元素R在该化合物中化合价为
A.+1价 B.+2价 C.+3价 D.+4价
相关试题

