现有A~E仪器装置图:
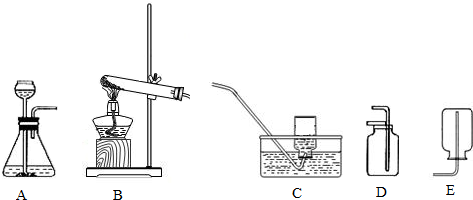
(1)在实验室里,装置A一般用于制取反应物状态为 、反应条件为 的气体;装置B一般用于制取反应物状态为 、反应条件为 _的气体.
(2)实验室常用氯化铵(NH4Cl)晶体和熟石灰(Ca(OH)2)粉末混合加热来制取氨气,同时生成氯化钙和水.①写出上述制取氨气反应的化学方程式: ;
②实验时应该选取上述(填写字母) 作为制取氨气的发生装置. ③根据下表提供的数据分析,实验时收集氨气应选用上述(填写字母)装置 而不用装置 ,其原因是 .

(1)在实验室里,装置A一般用于制取反应物状态为
(2)实验室常用氯化铵(NH4Cl)晶体和熟石灰(Ca(OH)2)粉末混合加热来制取氨气,同时生成氯化钙和水.①写出上述制取氨气反应的化学方程式:
②实验时应该选取上述(填写字母)
| 空气 | 氧气 | 氢气 | 氨气 | 二氧化碳 | |
| 密度(克•升-1) | 1.29 | 1.43 | 0.09 | 0.77 | 1.98 |
| 溶解度(克) | 0.031 | 0.018 | 680 | 0.88 |
分析:实验室制取气体的发生装置选择的依据为反应物的状态和反应的条件,收集装置的选择依据气体本身的密度、溶解性等物理性质.化学方程式的书写主要做好以下几个方面:反应物、生成物、反应条件、化学式的书写、配平、沉淀气体的标注等.
解答:解:(1)实验室制取气体的发生装置选择的依据为反应物的状态和反应的条件,初中阶段主要的两种气体的发生装置为“固液混合不加热”型、“给固体加热”型;
(2)实验室制取氨气反应物为氯化铵(NH4Cl)晶体和熟石灰(Ca(OH)2)粉末,反应条件为加热,因此选择的发生装置为给固体加热”型;生成氨气、氯化钙和水,
因此反应原理为NH4Cl+Ca(OH)2
NH3↑+CaCl2+H2O;根据表中提供的数据可知氨气极易溶于水,不能用排水法收集,密度小于空气密度的,也不能用向上排空气法收集,只能用向下排空气法收集.
故答案为:
(1)固体和液体;不需加热;固体和固体;需要加热
(2)NH4Cl+Ca(OH)2═NH3↑+CaCl2+H2O;B;E;C和D;NH3密度比空气小而且易溶于水
(2)实验室制取氨气反应物为氯化铵(NH4Cl)晶体和熟石灰(Ca(OH)2)粉末,反应条件为加热,因此选择的发生装置为给固体加热”型;生成氨气、氯化钙和水,
因此反应原理为NH4Cl+Ca(OH)2
| ||
故答案为:
(1)固体和液体;不需加热;固体和固体;需要加热
(2)NH4Cl+Ca(OH)2═NH3↑+CaCl2+H2O;B;E;C和D;NH3密度比空气小而且易溶于水
点评:气体的实验室制法主要从药品、反应原理、发生装置、收集装置、检验、验满及实验操作注意事项等方面进行比较、归纳,总结实验室制取气体的一般思路和方法.

