【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究。
【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
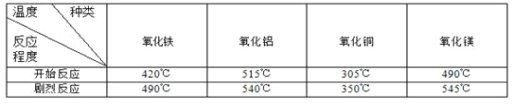
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是 。
【设计并完成实验】
Ⅰ. 将3.0g氯酸钾放在试管中加热
Ⅱ. 将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ. 将3.0g氯酸钾与Xg氧化铜均匀混合加热
【实验现象分析】
Ⅲ中X的值应为 ,实验Ⅰ和Ⅲ比较可证明 。 现象与实验Ⅲ相同.实验Ⅱ和Ⅲ对比的目的是 。将实验Ⅲ反应后的固体加水溶解、 、洗涤、干燥,然后进行称量的目的是 ,最后还要再将黑色粉末和 混合加热,
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的化学方程式为 。
【实验反思】MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计。)
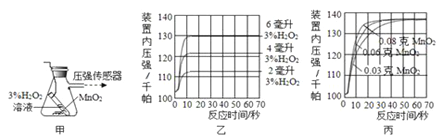
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出 。图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出 。
参考答案:
【答案】氧化铜 ; 1.0 ; 氧化铜能加快氯酸钾分解的速度;比较二氧化锰与氧化铜的催化效果;过滤; 验证氧化铜的质量在化学反应前后是否改变;氯酸钾;![]() ;0.1克MnO2与不同体积的3%H2O2溶液混合,过氧化氢的用量越多,速度差不多,但产生的氧气越多 ;不同质量的MnO2与相同体积的3%H2O2溶液混合,二氧化锰越多,产生的氧气一样多,但速度会加快。
;0.1克MnO2与不同体积的3%H2O2溶液混合,过氧化氢的用量越多,速度差不多,但产生的氧气越多 ;不同质量的MnO2与相同体积的3%H2O2溶液混合,二氧化锰越多,产生的氧气一样多,但速度会加快。
【解析】
试题分析:实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是氧化铜,因为其作用下,生成氧气所需的温度最低;【实验现象分析】Ⅲ中X的值应为1.0g。这样与Ⅱ所取得催化剂的质量相同,形成对比,实验Ⅰ和Ⅲ比较可证明氧化铜能加快氯酸钾分解的速度;现象与实验Ⅲ相同.实验Ⅱ和Ⅲ对比的目的是比较二氧化锰与氧化铜的催化效果。将实验Ⅲ反应后的固体加水溶解、 过滤、洗涤、干燥,然后进行称量的目的是验证氧化铜的质量在化学反应前后是否改变,最后还要再将黑色粉末和氯酸钾混合加热;验证其化学性质是否发生改变;【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的化学方程式为![]() 【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出0.1克MnO2与不同体积的3%H2O2溶液混合,过氧化氢的用量越多,速度差不多,但产生的氧气越多 ;图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出不同质量的MnO2与相同体积的3%H2O2溶液混合,二氧化锰越多,产生的氧气一样多,但速度会加快。。
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出0.1克MnO2与不同体积的3%H2O2溶液混合,过氧化氢的用量越多,速度差不多,但产生的氧气越多 ;图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出不同质量的MnO2与相同体积的3%H2O2溶液混合,二氧化锰越多,产生的氧气一样多,但速度会加快。。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(3分)钙元素与人类的生活有着密切联系。
(1)生活中常接触到“高钙牛奶”,其中的“钙”应理解为__________(填“元素”或“单质”)。
(2)幼儿和青少年缺钙会患__________。
A.贫血 B.佝偻病 C.夜盲症
(3)生石灰是常见的食品干燥剂,请写出它与水反应的化学方程式__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】 下列选项中物质的俗名、化学式及其类别均正确的是
俗名
化学式
类别
A
消石灰
CaO
氧化物
B
纯碱
Na2CO3
碱
C
酒精
C2H6O
有机物
D
水银
Ag
单质
-
科目: 来源: 题型:
查看答案和解析>>【题目】某天然矿泉水中元素及物质含量如下表所示,请用相关化学用语回答下列问题。
(1)右表中的一种阴离子 ;

(2)标出偏硅酸中硅元素的化合价 ;
(3)产自溶洞中的水中含有微量的二氧化碳,保持二氧化碳化学性质的最小粒子是 ;
(4)在自来水厂净水方法中,说法正确的是( )
①通过沉淀、过滤、吸附除去水中难溶性杂质,就可得到纯净水
②常用的方法有:沉淀、吸附、过滤、蒸馏,其中净化程度最高的是蒸馏
③通过过滤的方法将不溶于水的固体杂质与水分离开
④用氯气给水杀菌是化学变化,用活性炭净化水是物理变化.
(5)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式: ;
(6)有经验的鱼民在进行长途运输鲜鱼的过程中常常在水中加入少量的过氧化钙固体。已知过氧化氢的化学式可表示为H2O2,过氧化钾为K2O2,则过氧化钙的化学式为 ,若过氧化钾与水反应的方程式表示为2K2O2+2H2O=4KOH+O2↑,则过氧化钙与水的反应方程式为 ,请说出使用过氧化钙可以使鱼长期存活的理由: 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】地壳中含量最多的元素是
A.氧 B.硅 C.铝 D.铁
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学与生活息息相关,下列说法正确的是
A.人体缺钙会产生龋齿
B.超市里所有食品都不含食品添加剂
C.生活中常用的塑料、纤维、合金都是有机合成材料
D.为减少“白色污染”,可用降解塑料代替传统塑料
-
科目: 来源: 题型:
查看答案和解析>>【题目】鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小刚和小勇同学进行了如下实验。实验过程和测定的相关实验数据如下所示:请回答相关问题:

(1)逸航同学根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
(2)鑫烁同学根据“反应过程中减少的质量”,也求得了蛋壳中碳酸钙的质量分数,请你写出鑫烁的计算过程和结果。
(3)逸航和鑫烁根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因 。
相关试题

