【题目】在实验室中,化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸成分反应,测得部分数据与图象如下,请根据有关信息回答问题。
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(1)a的数值为____________;
(2)b的数值为____________;
(3)计算该试剂中氢氧化钙的质量分数(计算结果保留一位小数)______________。

参考答案:
【答案】 125g 2.2g 74.7%
【解析】(1)根据数据分析可知,该反应过程是盐酸先与氢氧化钙反应,再与碳酸钙反应。所以a的数值为:(19.8g+30.2g)+25g×3=125g。(2)第5次加入盐酸生成气体的质量是:[(19.8g+30.2g)+25g×5]-172.8=2.2g,第六次加入盐酸生成气体的质量是:[(19.8g+30.2g)+25g×6]-197.8=2.2g,说明第5次中碳酸钙已经反应完,所以b的数值为2.2g。(3)设试剂中碳酸钙的质量是x,CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
100 44
x 2.2g
![]() =
=![]() ,解得x=5g,该试剂中氢氧化钙的质量为:19.8g-5g=14.8g
,解得x=5g,该试剂中氢氧化钙的质量为:19.8g-5g=14.8g
该试剂中氢氧化钙的质量分数为:![]() ×100%=74.7%
×100%=74.7%
-
科目: 来源: 题型:
查看答案和解析>>【题目】通过一学年的化学学习,同学们已经掌握了实验室制取气体的一些规律。请结合下图回答问题:
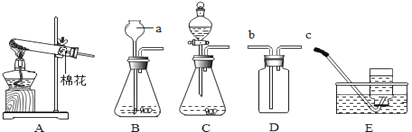
(1)写出图中仪器a的名称:a_________;
(2)小李同学选用装置A制取氧气。写出该反应的化学方程式_______________;用装置D收集氧气判断已集满气体的方法是____________;若用装置E收集的氧气不纯,其原因可能是___________(写出一种即可);
(3) 若用双氧水(加少量二氧化锰)制取氧气,要得到平稳的氧气流,发生装置可选用上图中的________(填字母编号)。
(4) 通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的有刺激性气味的气体,其水溶液称为氨水,小萍同学利用加热氯化铵和氢氧化钙的固体混合物的方法制取氨气,写出该反应的化学方程式________________________,若她选择的收集装置是D,则氨气应该从_______(填字母编号)通入,但使用该装置收集氨气所存在的明显的缺陷是___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~F为初中化学常见物质,这六种物质间存在右图所示的关系(“→”表示转化关系,“—”表示反应关系)。其中A、B两溶液发生中和反应,得到厨房内常用的一种调味品;C 在农业上可用来配制波尔多液,且C和D反应可制得B;A和D反应的产物与A和小苏打反应得到的产物完全相同。
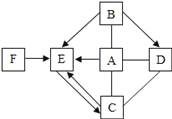
(1)A的化学式为___________。
(2)A、B充分反应后的溶液中溶质的组成可能有三种情况,欲通过一次实验证明溶质是哪一种情况,需要加入的试剂是_________________。
(3)C与D之间反应的化学方程式为_______________________。
(4)E物质的类别是___________(填酸、碱、盐、氧化物);若F是有机物,写出一个F生成E的化学方程式______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】黄铁矿一般不用于直接炼铁而用于制酸工业,如图是黄铁矿综合利用工艺流程图。试回答下列问题。
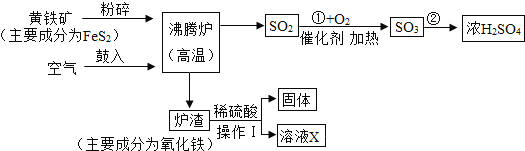
(1)工艺中操作 I的名称为 ____________________________________。
(2)写出反应①的化学方程式___________________________________。
(3)写出黄铁矿在沸腾炉中发生反应的化学方程式 ___________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】铁元素、铁原子的部分信息如下图所示。下列说法中错误的是


A. 铁离子的质子数为23
B. 第三层上的电子数y=14
C. 铁原子的核外电子数为26
D. 铁元素的相对原子质量为55.85
-
科目: 来源: 题型:
查看答案和解析>>【题目】某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分。根据该反应的微观示意图(如下图),分析下列说法正确的是
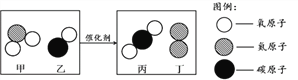
A. 四种物质均属于化合物
B. 物质丙由原子构成
C. 参加反应的甲和乙的分子个数比为1:2
D. 生成丙和丁两种物质的质量比为11:7
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是A、B、C三种物质的溶解度曲线,下列说法中错误的是
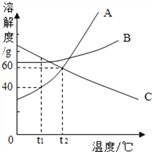
A. 升高温度可使接近饱和的C溶液变为饱和
B. 当A中含有少量B时,可以通过降温结晶的方法提纯A
C. t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
D. 将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
相关试题

