

【题目】某兴趣小组发现,上周做实验用的氢氧化钠固体忘记了盖瓶盖,他们欲对该固体的变质情况进行探究。
(提出问题)该瓶氢氧化钠固体是否变质,变质情况如何?
(查阅资料)①碳酸钠溶液的pH最大约为10.6,饱和的碳酸氢钠溶液约为8.0,氯化钙溶液呈中性。
②NaOH、Na2CO3分别在水和酒精中的溶解度如下表所示:
物质种类 | NaOH | Na2CO3 | |||
温度 | 20℃ | 40℃ | 20℃ | 40℃ | |
溶剂 | 水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 | |
(作出猜想)猜想Ⅰ:固体未变质;
猜想Ⅱ:固体部分变质;
猜想Ⅲ:固体全部变质。
(实验探究)(1)兴趣小组同学取少量样品于烧杯中,加适量水溶解,测得溶液的pH约为12。由此他们得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是______。
(2)组内其他同学取步骤(1)烧杯中少量溶液于试管中,加入过量的____溶液,振荡,有白色沉淀生成;不再产生沉淀时,取上层清液于另一支试管中,滴加____,溶液变红。
(实验结论)通过实验,兴趣小组证明猜想__正确。
(反思评价)根据查阅资料,有同学提出可以通过氢氧化钠和碳酸钠在酒精中溶解度不同来验证猜想Ⅲ正确。请你帮助他设计实验方案:_____。
(实验拓展)实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量。称取一定量样品,溶于水配成250.0mL溶液将pH=1的稀盐酸逐滴加入体积为25.0mL的该溶液中,所得曲线如图所示:
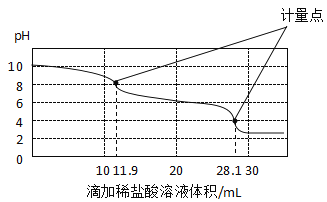
a.上一个计量点前发生反应的化学方程式为_____。
b.下一个计量点时溶液中大量存在的阴离子是_______。
【答案】氢氧化钠固体部分变质加水溶解后溶液的pH也可能为12 氯化钙(或氯化钡或硝酸钙或硝酸钡) 酚酞 Ⅱ 取样称量质量,加入酒精中,充分溶解后过滤,干燥后再次称量,两次所称质量相等。证明固体全部变质(或猜想Ⅲ正确)。 ![]() Cl-
Cl-
【解析】
实验探究:(1)氢氧化钠容易与空气中的二氧化碳反应生成碳酸钠和水,如果氢氧化钠部分变质,加水溶解后,pH也可能为12,不能得出猜想Ⅰ正确;
(2)氢氧化钠容易与空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,故可加入过量的氯化钙溶液,振荡,有白色沉淀生成,可以证明碳酸钠的存在,并将碳酸钠除尽,不再产生沉淀时,取上层清液于另一支试管中,滴加无色酚酞试液,溶液变红,说明含氢氧化钠。
实验结论:故通过以上实验可以得出氢氧化钠部分变质,故猜想Ⅱ成立;
反思评价:由表中数据可知,碳酸钠不溶于酒精,故为了证明猜想Ⅲ成立,可取样品,称量质量,溶于酒精,然后过滤、干燥,称量滤渣质量,如果溶解前后,滤渣的质量不变,说明只含碳酸钠,则猜想Ⅲ成立,故可设计实验:取样称量质量,加入酒精中,充分溶解后过滤,干燥后再次称量,两次所称质量相等。证明固体全部变质(或猜想Ⅲ正确);
实验拓展:a、向Na2CO3和NaHCO3混合物中滴加稀盐酸,一开始,稀盐酸量不足,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,该反应的化学方程式为:![]() ;
;
b、碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳和水,pH=4,说明稀盐酸过量,故下一个计量点时溶液中的溶质是NaCl、HCl,故大量存在的阴离子是:Cl-。


科目:初中化学 来源: 题型:
【题目】向一定质量的Zn(NO3)2和AgNO3混合溶液中加入ag铜粉,充分反应后过滤,得到某温度下的不饱和溶液和滤渣。下列有关说法错误的是
A.滤渣的质量一定大于ag
B.所得溶液中可能含有AgNO3
C.整个过程中Zn(NO3)2的质量不变
D.滤渣中一定含有单质Cu和单质Ag
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】明代宋应星著的《天工开物》中有关于“火法”冶炼金属锌的工艺记载:“炉甘石(注:主要成分是碳酸锌)十斤,装载入一泥罐內,然后逐层用煤炭饼(注:反应后生成一氧化碳)垫盛,其底铺薪,发火煅红,冷淀,毁罐取出,即倭铅也”。下列说法错误的是
A.煤炭中起作用的主要成分是C
B.冶炼Zn的化学方程式为: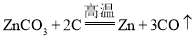
C.该冶炼锌的反应属于置换反应
D.倭铅是指金属锌和铅的混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)用途广泛,可用作净水剂,医学上可用作补血剂,还可用于制颜料。
(1)绿矾是一种絮凝剂,利用其溶于水后生成的胶状物对杂质的吸附作用,使杂质沉降来达到净水的目的。
(2)缺铁会引起贫血,铁是一种人体必需的微量元素。
(3)《本草纲目》中记载,绿矾“煅过变赤,则为绛矾”。绛矾是古代壁画、彩塑中使用的一种红色颜料。
(4)铁的氧化物中已知三氧化二铁为红色。四氧化三铁和氧化亚铁为黑色。
(5)氢氧化钠溶液可以吸收二氧化硫和三氧化硫;高锰酸钾溶液可以检验二氧化硫。
某化学兴趣小组同学对绿矾高温分解的产物很感兴趣,进行了如下探究。
(查阅资料)①绿矾高温分解的产物是一种固态金属氧化物和几种气态非金属氧化物。
②在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低。
③无水硫酸铜遇水变蓝。④硫有两种常见的氧化物,部分性质如下表:
硫的氧化物 | 熔点 | 沸点 | 能否使高锰酸钾溶液褪色 |
SO2 | -75.5℃ | -10℃ | 能 |
SO3 | 16.8℃ | 44.8℃ | 不能 |
(提出问题)《本草纲目》中记载绿矾“煅过变赤”,经实验验证绿矾高温分解确实产生红色固体,说明绿矾高温分解产生的一种固态金属氧化物是____________,那么产生的几种气态非金属氧化物是什么呢?
(进行猜想)猜想1:H2O和_____________;
猜想2:H2O和SO3;
猜想3:H2O、SO2和SO3
甲同学认为无需通过进一步实验即可判定猜想2错误,理由是__________________________。
(设计实验)乙同学用以下装置检验绿矾高温分解产生的气态非金属氧化物:
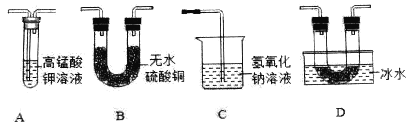
需将绿矾高温分解产生的气体依次通过_____________(填字母,且每套装置限用一次)。
(分析现象)进行上述实验,观察到A中试管内溶液_________,B中U形管内固体__________,D中U形管内出现无色晶体,说明猜想3正确。绿矾高温分解的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线。
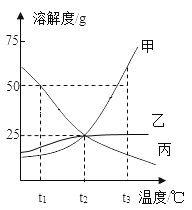
(1)t1℃时,三种物质的溶解度由大到小的关系为____。
(2)t2℃时,甲、乙、丙三种物质的饱和溶液降温至t1℃时为不饱和溶液的是__。
(3)现有含少量甲的乙固体,若要通过结晶法进行提纯乙(甲与乙不发生反应),现有下列实验步骤可供选择:
①取一定量的水将固体溶解 ②充分冷却后过滤 ③趁热过滤 ④加热蒸发至大部分晶体析出 ⑤加热蒸发至溶液接近饱和 ⑥停止加热用余热将溶液蒸干 ⑦用少量水洗涤晶体并烘干。
合理的操作顺序为_______(按顺序填编号)。
(4)t3℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定质量的水(析出的晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小的关系为______。
(5)t2°C时,配制甲、乙、丙三种物质的饱和溶液,一定相等的是___(填字母)。
A 溶质质量 B 溶剂质量
C 溶质质量分数 D 溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙醇俗称酒精,可以用作酒精灯、内燃机等的燃料,用灯帽盖灭酒精灯的灭火原理是____;乙醇完全燃烧的化学方程式_________;现有乙醇和乙醛(CH3CHO)的混合物共13.4g,完全燃烧后生成26.4gCO2,则生成水的质量为_________g.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,如图所示,下列说法正确的是
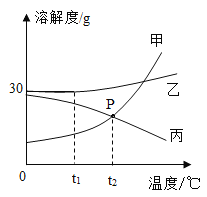
A.三种物质的溶解度都随温度的升高而增大
B.P点表示t2℃时甲、丙两物质的溶解度相等
C.t1°C时,乙物质的饱和溶液溶质质量分数为30%
D.甲中含有少量乙,可采用蒸发结晶的方法提纯甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室部分仪器或装置如下图所示,请回答下列问题。
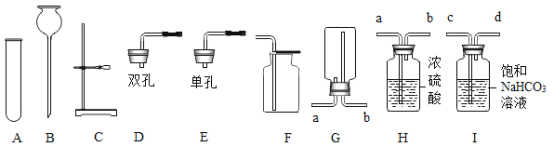
(1)写出仪器的名称:B_________。
(2)实验室制取二氧化碳气体,搭建发生装置可选择图中的______(填仪器字母),用该装置制取氧气的化学方程式为__________________。
(3)已知NaHCO3可与HCl反应,采用上述方法制取的二氧化碳中常含有氯化氢气体和水蒸气。为获得纯净、干燥的二氧化碳气体,可选用如图所示的H装置和1装置进行干燥和除杂,选择F装置收集,导管口连接的正确顺序是:气体→(_______)→(_______)→(_______)→(_______)→F;收集二氧化碳后验满的方法是:_____________。
(4)若用图G装置收集H2,则H2导入端为____(填“a”或“b”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫化氢(H2S)是一种密度比空气密度大的气体,实验室通常用固体硫化亚铁(FeS)和稀硫酸混合,常温下通过发生复分解反应制得硫化氢气体。试回答:
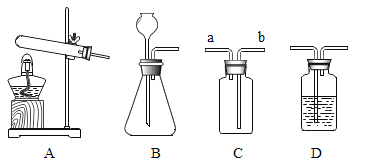
(1)实验室制取硫化氢气体的化学方程式为______________________。
(2)根据装置图回答下列问题。
①制得硫化氢气体的发生装置可以选用___________(填序号)。该装置在实验室还可以用来制取氧气,写出用该装置制取氧气的化学方程式_____________________。
②若用C装置收集硫化氢气体,进气口应为__________(填“a”或“b”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com