【题目】(7分)硫酸铜溶液对过氧化氢(H2O2)的分解有催化作用。取8.5%的过氧化氢溶液80g倒入小烧杯中,向其中加入未知浓度的硫酸铜溶液10.0g,使过氧化氢完全分解。计算:
(1)产生氧气的质量是多少?
(2)向反应后所得溶液中加入足量NaOH溶液,得到蓝色沉淀,过滤后随即进行称量(其他操作全正确),称得沉淀的质量为0.98g,请计算未知浓度的硫酸铜溶液的质量分数。
参考答案:
【答案】(1)3.2g
(2)小于16%
【解析】
试题分析:(1)过氧化氢分解生成水和氧气,利用化学方程式,根据过氧化氢与氧气的质量比即可计算出生成的氧气的质量;
过氧化氢溶液中溶质的质量=80g×8.5%=6.8g
解:设生成的氧气的质量为x;
2H2O2![]() 2H2O + O2↑
2H2O + O2↑
68 32
6.8g x
68/32 =6.8g/x
X=3.2g
(2)氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,根据沉淀氢氧化铜的质量即可计算出硫酸铜的质量;
设硫酸铜的质量为y;
2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO4
160 98
Y 0.98g
160/y = 98/0.98g
Y=1.6g
硫酸铜溶液的质量分数=1.6g/10g ×100%=16%
由于得到的沉淀没有进行干燥,故所得的沉淀的质量偏大,即实际硫酸铜的溶质质量分数小于16%。
答:略
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列能证明分子可分的事实是
A.氮气和氧气常温混合 B.氯酸钾加热后熔化
C.白糖分散于水中形成糖水 D.氢气在空气中燃烧
-
科目: 来源: 题型:
查看答案和解析>>【题目】有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如下图所示。由此推断白色固体中
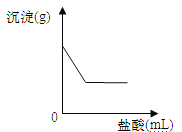
A.可能存在Na2SO4 B.可能存在NaOH
C.可能存在BaCl2 D.肯定只存在Na2CO3
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图,甲、乙两个装置均可通过胶头滴管向锥形瓶中滴加某种液体,达到使气球鼓起的目的,锥形瓶和胶头滴管放入物质正确的一组是
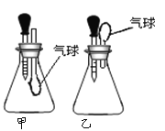
序号
A
B
C
D
装置名称
甲
乙
甲
乙
甲
乙
甲
乙
锥形瓶内物质
HCl气体
固体
NaCl
固体NaOH
NH3
Cu
CO2
锌粒
胶头滴管中物质
NaOH溶液
H2O
盐酸
H2O
H2O
稀盐酸
NaOH溶液
稀硫酸
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的化学式书写正确的是
A.溴化钠 BrNa B.氧化钠 Na2O
C.碳酸钠 NaCO3 D.氢氧化钙 CaOH2
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学实验室的铅蓄电池中装有硫酸.如果不慎将硫酸洒到大理石地面上,会发出嘶嘶声并有气体产生.这种气体是
A.CO2 B.N2 C.H2 D.O2
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明同学对所学部分化学知识整理如下,其中有错误的是
A.干冰不是冰 B.纯碱不是碱 C.水银不是银 D.食盐不是盐
相关试题

