【题目】在校园科技节上,为测出鸡蛋壳(主要成分是碳酸钙)中钙元素的质量分数,
某同学称取已洗净、晾干、研成粉末的鸡蛋壳10克置于烧杯中,将烧杯放在电子天平上,往烧杯中加入100g的稀盐酸,每0.5分钟记录一次电子天平的示数,据此计算出产生气体的质量,具体数据如表:
时间(分钟) | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余物质质量(克) | 110 | 108.2 | 107 | 106.4 | 106.04 | 106.04 | 106.04 |
(1)若产生的气体全部是鸡蛋壳中的碳酸钙与盐酸反应生成的CO2,根据实验结果计算出该鸡蛋壳中钙元素的质量分数。(假定鸡蛋壳中其它成分不含钙元素,写出具体计算过程)________
(2)下列哪些情况会导致实验中钙元素质量分数测量结果偏大?_______
A.鸡蛋壳未晾干 B.鸡蛋壳未充分研碎
C.鸡蛋壳中含有碳酸镁(可与盐酸反应生成MgCl2、H2O和CO2)
参考答案:
【答案】 36% C
【解析】(1)根据质量守恒定律和碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,可知,反应中的质量减少量为生成的二氧化碳的质量.根据二氧化碳的质量对应出钙元素的质量,最后求算出钙元素在混合物中的质量分数;
(2)钙元素在混合物中的质量分数计算是![]() ,根据这个计算式子分析可能引起偏高的操作。
,根据这个计算式子分析可能引起偏高的操作。
解:(1)根据质量守恒定律可得,生成的二氧化碳的质量110g﹣106.4g=3.6g
设钙元素的质量为x。
根据CaCO3+2HCl=CaCl2+H2O+CO2↑
可得Ca~~CO2↑
40 44
x 3.96g
![]()
x=3.6g
则鸡蛋壳中钙元素的质量分数为![]() =36%。
=36%。
(2)由于钙元素在混合物中的质量分数计算是![]() ,当结果偏大时,要么是钙元素的质量偏大,要么鸡蛋壳的质量偏小。鸡蛋壳未晾干,会导致总质量相对于干燥鸡蛋壳偏大,所以引起的钙元素的质量分数偏小。而鸡蛋壳没有完全反应,则对应的二氧化碳偏少,则对应的钙元素质量也偏小,所以质量分数偏小。
,当结果偏大时,要么是钙元素的质量偏大,要么鸡蛋壳的质量偏小。鸡蛋壳未晾干,会导致总质量相对于干燥鸡蛋壳偏大,所以引起的钙元素的质量分数偏小。而鸡蛋壳没有完全反应,则对应的二氧化碳偏少,则对应的钙元素质量也偏小,所以质量分数偏小。
而含有杂质碳酸镁时,消耗等质量的碳酸盐时,碳酸镁生成的二氧化碳多,而这个二氧化碳当成碳酸钙生成的,则对应的钙元素的质量就偏大,最终的钙元素的质量分数偏大。
故选:C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请根据下图实验内容回答下列问题。
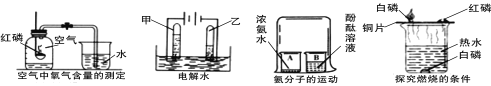
A B C D
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的五分之一,可能的原因是_____(填一条即可),该实验不能用蜡烛代替红磷,理由是___________________。
(2)B实验正极产生的气体与负极产生的气体的体积比约为_____________。
(3)C实验观察到的现象是___________________________________________________。
(4)D实验资料信息:白磷和红磷的着火点分别是40℃、240℃。铜片上的红磷不燃烧,是因为___。水中的白磷不燃烧,是因为____________。如果要让水中的白磷在水下燃烧,应采取的措施是____________。通过以上实验事实证明,燃烧一般需要同时具备下列条件:①物质具有可燃性;②可燃物与氧气接触;③_______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2016届辽宁省鞍山市九年级二模】下列应用与中和反应原理无关的是( )
A.用浓硫酸干燥氧气 B.服用含氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤 D.用氢氧化钠溶液洗涤石油产品中残留的硫酸
-
科目: 来源: 题型:
查看答案和解析>>【题目】蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
【作出猜想】小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
【实验验证】
方案一:小明将蔗糖在氧气中燃烧,检验到生成产物中有水和二氧化碳,得出结论“蔗糖是由碳、氢、氧三种元素组成的”。
小刚认为该方案不合理,只能说明蔗糖中一定含有碳、氢元素,不能确定是否含有氧元素,理由是_______________________。
方案二:小刚用下图所示装置进行实验。实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给蔗糖加强热。
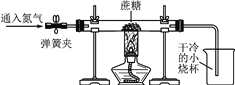
(1)观察到________________________出现,说明蔗糖中含有氢元素和氧元素。
(2)观察到硬质玻璃管中残留有黑色固体,他猜想该黑色固体是单质碳,并继续利用图示装置,另选试剂进行了验证单质碳的实验,实验过程和现象如下:
实验过程
实验现象
________________,点燃酒精灯
①硬质玻璃管中的黑色固体剧烈燃烧,发出白光;
②_____________
写出上述实验过程中一个反应的化学方程式:________________________。
【实验结论】蔗糖是由碳、氢、氧三种元素组成的。
【拓展交流】
(1)方案二中,先通入一会儿氮气的原因是___________________________________。
(2)查阅资料得知蔗糖的化学式为C12H22O11。小红发现:蔗糖分子中氢原子的数目是氧原子数目的2倍,但是,蔗糖中氧元素质量却是氢元素质量的8倍,导致出现这种情况的原因是________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】阿斯匹林(分子式为C9H8O4)是一种常用解热镇痛药,用于治疗感冒、发烧、头痛等疾病。某阿斯匹林肠溶片说明书的部分内容如图所示。

(1)阿斯匹林的相对分子质量是___________,其中氢、氧元素的质量比是___________;
(2)阿斯匹林中碳元素的质量分数_______;25mg阿斯匹林中含碳元素的质量_________;
(3)治疗不稳定性心绞痛时,病人每天服用阿斯匹林肠溶片的最大量是_________片。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图表示某些物质间转化关系(各反应物均无剩余)。A为黑色粉末,且A在该化学反应前后的化学性质和质量均不改变,F为能导致“温室效应”的无色气体;A、B、C、F均为氧化物;D、E、H均为单质;D和H为无色气体、E为黑色固体。请回答下列问题:
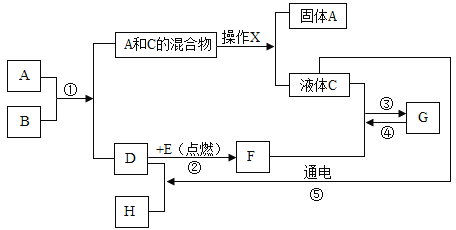
(1)写出有关物质的化学式:B______________________、F______________________;
(2)反应①中A物质的作用是__________________________________________________;
(3)反应①的化学方程式:___________________________________________________;
(4)反应③的化学方程式:___________________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】2014年春季我国北方多地持续雾霾天气,部分城市污染指数突破测量上限,PM2.5监测点“爆表”,空气堪比毒气。下列做法正确的是
A.大量燃放烟花爆竹
B.外出最好开私家车
C.大气污染物排放量大的单位自觉减排
D.大量使用煤作燃料
相关试题

