【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共6g放入大试管中加热,并在同时测定试管中剩余固体物质的质量(如下表),
请分析表中数据,完成下列问题:
反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
剩余固体质量/g | 5.20 | 4.60 | 4.20 | 4.10 | 4.08 |
(1)完全反应时,生成氧气的质量为_____g;
(2)原混合物中氯酸钾的质量分数是__________?(计算结果精确到0.1%)
参考答案:
【答案】 1.92g 81.7%
【解析】(1)氯酸钾发生分解反应生成氯化钾和氧气,二氧化锰作催化剂,反应前后二氧化锰的质量不变,根据质量守恒定律,生成氧气的质量为:6g-4.08g=1.92g。(2)设原混合物中氯酸钾的质量为x。
2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
245 96
x 1.92g
![]() =
=![]() ,解得x=4.9g
,解得x=4.9g
原混合物中氯酸钾的质量分数是: ![]() ×100%=81.7%
×100%=81.7%
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题:

(1)t 3 ℃ 时,将 30g 甲物质加入到 50g 水中,充分溶解后所得溶液的质量为______g。
(2)当甲中含有少量乙时,提纯甲的方法是_________。
(3) t 3 ℃ 时等质量的甲、乙、丙三种物质的饱和溶液降温至 t 1 ℃,所得溶液中溶质的质量分数由大到小的顺序为__________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下是初中化学的一些基本实验,请根据实验内容回答下列问题.
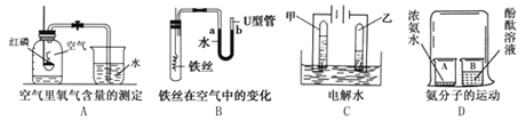
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的,可能的原因是 (填一条即可)。
(2)放置一周后,B实验观察到的现象是 。
(3)C实验产生氧气与氢气的体积比约为 。
(4)D实验观察到的现象是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示。
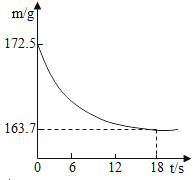
求:(1)生成CO2的质量。
(2)该纯碱样品中Na2CO3的质量分数。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
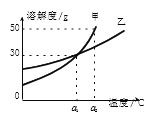
A. a1℃时甲和乙的饱和溶液,升温到 a2℃时仍是饱和溶液
B. 甲和乙的溶解度相等
C. a2℃时,在 100 g 水中加入 60 g 甲,形成 160 g 溶液
D. a1℃时,甲和乙各 30 g 分别加入 100 g 水中, 均形成饱和溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂,利用人呼出的二氧化碳与Na2O2反应放出O2,供给人的正常生命活动,该反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。某同学利用该反应原理制取氧气,设计了如图一所示的实验装置。
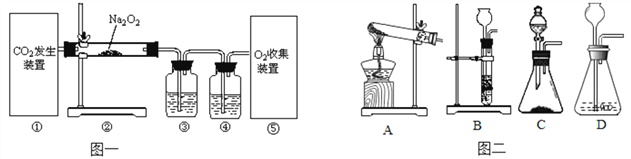
⑴装置①中CO2的制取方法有多种,若用加热NaHCO3固体制取CO2,应该选用的发生装置为________(选填图二中字母),图二C、D中用作反应容器的仪器名称为:______________。
⑵为收集纯净干燥的O2,装置③中盛放的试剂为饱和的氢氧化钠溶液,作用是_____________;装置④中盛放的试剂为___________;⑤中收集方法可选用______。(填选项)
A.排水集气法 B.向下排空气法 C.向上排空气法
⑶任意写出一种实验室制取氧气或二氧化碳气体的反应方程式:________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学用语与含义相符的是( )
A.4个氢原子:2H2 B.铝元素的化合价为+3价:Al3+
C.2个碳酸根离子:2CO32﹣ D.2个氮分子:2N
相关试题

