【题目】海水“晒盐”得到的粗盐,含有氯化镁、氯化钙、硫酸钠等可溶性杂质,必须对其进行分离和提纯,才能用于工业生产和人们的日常生活.某实验小组设计如下流程除去粗盐中的可溶性杂质,得到氯化钠晶体.请回答下列问题.
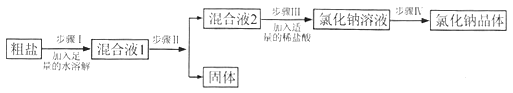
(1)步骤II加入的物质有:①过量的碳酸钠溶液、②过量的氢氧化钠溶液、③过量的氯化钡溶液,正确的加入顺序有三种,请你把它写出来(用物质前的序号表示),第一种:_____;第二种:___;第三种:________.
(2)步骤 IV的实验操作是___________.
(3)工业上电解饱和氯化钠溶液可制得烧碱,同时还有氯气和氢气生成.
该反应的化学方程式为_____________________________________.
参考答案:
【答案】 ③ ② ① 蒸发 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
【解析】(1)要先除SO42﹣离子,然后再除Ca2+离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加NaOH除去Mg2+离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,只要将三种离子除完了,然后过滤即可,最后加盐酸除去过量的氢氧根离子碳酸根离子,所以正确的操作顺序为:③②①;
(2)从氯化钠溶液中得到氯化钠晶体,可以采用蒸发操作;
(3)根据题意:电解氯化钠溶液可以得到氢氧化钠溶液、氢气和氯气,所以电解氯化钠的方程式为:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
-
科目: 来源: 题型:
查看答案和解析>>【题目】元素周期表是学习和研究化学的重要工具.请分析图中信息回答相关问题.
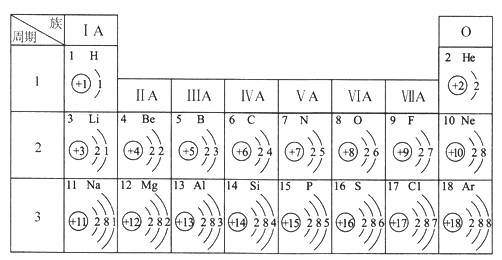
(1)硫元素的质子数是_____,它属于_____(填“金属”或“非金属”)元素,在化学反应中容易_______(填“得到”或“失去”)电子.
(2)原子序数为l、7、8的三种元素形成的碱的化学式为_________.
(3)在同一族中,各元素的原子最外层电子数________( He除外).
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据如图回答问题.
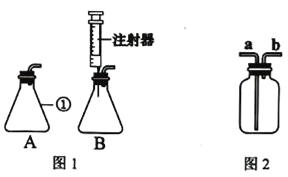
(1)图1中A、B都是制取二氧化碳的装置,其中标号①仪器的名称是__________.实验室制取二氧化碳的化学方程式是___________________.
(2)用图2装置收集二氧化碳气体,气体应从____管进去(填“a”或“b”),原因是___________.
(3)相对于A装置,B装置的优点是________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组为了区分氢氧化钠溶液和氢氧化钙溶液,设计了如下图所示的四组实验方案,请按要求回答问题.
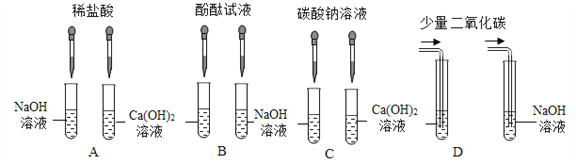
(1)上述实验方案中能达到实验目的是_______(填字母序号).
(2)C组实验中发生反应的化学方程式为___________________________.
【继续探究】实验结束后,小组的同学将A、B、C、D四组实验八支试管中的物质倒入同一个烧杯中,最终得到无色透明的溶液.
【分析讨论】
①烧杯中能跟稀盐酸发生化学反应的物质有_______种(酚酞除外).
②最终得到的溶液中:一定含有的溶质是_____________(填化学式,下同),一定不含有的溶质是________,可能含有的溶质是_______.
【实验验证】为了验证最终得到的溶液中可能含有的溶质是否存在,小组的同学取少量烧杯中的溶液于试管中,向其中逐滴加入碳酸钠溶液直至过量,观察到________,证明含有该溶质.
【拓展延伸】小组的同学把D组实验方案中的二氧化碳换成二氧化硫,达到同样实验效果.二氧化硫跟氢氧化钙反应的化学方程式为______________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~G是均含有一种相同元素的物质,其中A、B、C、D是不同类别的物质且相对分子质量(化学式量)依次减小,G与碱反应有气体生成.它们之间有如右图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“﹣”表示相连两种物质能发生化学反应,部分反应物、生成物及反应条件已略去).
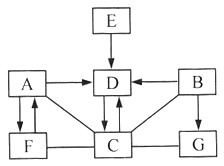
(l)从物质的分类分析,物质A属于______(填“酸”、“碱”、“盐”或“氧化物”).
(2)D、E是由相同的元素组成的物质,E的化学式是_________.
(3)写出下列反应的化学方程式:
D→C:__________________;B→G:______________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某小组同学对实验过程中产生的氯化钡和盐酸的混合废液进行如下处理:取140.05g氯化钡和盐酸的混合废液于烧杯中,向其中逐滴加入碳酸钠溶液.加入碳酸钠溶液质量与生成沉淀质量的关系如图所示.求:当恰好完全反应时.所得溶液的溶质质量分数是多少?(写出计算过程)

-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)如图1是a、b、c三种物质的溶解度曲线,回答下列问题:
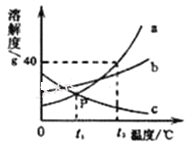
①t2℃时,a、b、c三种物质的溶解度由大到小的顺序为_______________.
②P点的含义是_____________________.
③t2℃时,将40ga物质加入50g水中,充分溶解后得到溶液的质量为_____g.
④将a、b、c三种物质的饱和溶液从t2℃降温到t1℃时,溶液中溶质的质量分数不变的是______.
(2)A﹣G是初中化学常见物质,A、C在常温下是气体且元素组成相同,B是铁锈的主要成分,E的相对分子质量为100,它们的相互转化关系如图2(部分反应物、生成物及反应条件已略去),请回答下列问题:

①写出物质E的化学式_____________.
②写出有关反应的化学方程式:
(Ⅰ)A+B→_____________________;
(Ⅱ)G+Na2CO3溶液→__________________________.
③写出F的一种用途_______________.
相关试题

