【题目】某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],煮沸时会有水垢生成。一个化学实验小组欲探究该水垢的主要成分。
【猜想】
Ⅰ CaO Ⅱ Ca(OH)2 Ⅲ CaCO3 Ⅳ Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是___(写出化学方程式)。
【实验探究】
实验 | 实验操作 | 现象 | 解释或结论 |
实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | 猜想___不成立 |
实验二 | 取适量的水垢,加入足量的___,将产生的气泡通入澄清石灰水 | 变浑浊 | 猜测Ⅲ成立 |
实验三 | 继续向实验二中变浑浊的石灰水中通入CO2 | 变澄清 |
|
【原理与解释】
(1)请用化学方程式表示实验二中有关反应的化学反应原理:___,___。
请写出实验三变澄清可能发生的化学方程式___ ,小组同学查阅资料发现在碳酸盐地区,饮用水的硬度较大,其中的原因与实验三的原理相同。
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用___来检测饮用水是硬水还是软水。
参考答案:
【答案】 CaO +H2O = Ca(OH)2 Ⅱ和 Ⅳ 稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2 ↑ Ca(OH)2+CO2=CaCO3↓+H2O CaCO3 +H2O+CO2=Ca(HCO3)2 肥皂水
【解析】根据所学知识和题中信息知,【猜想】Ⅰ CaO Ⅱ Ca(OH)2 Ⅲ CaCO3 Ⅳ
Ca(OH)2和CaCO3小强同学认为该水垢中不会存在CaO,理由是CaO +H2O = Ca(OH)2。
实验 | 实验操作 | 现象 | 解释或结论 |
实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | 猜想Ⅱ和 Ⅳ 不成立 |
实验二 | 取适量的水垢,加入足量的稀盐酸,将产生的气泡通入澄清石灰水 | 变浑浊 | 猜测Ⅲ成立 |
实验三 | 继续向实验二中变浑浊的石灰水中通入CO2 | 变澄清 |
|
【原理与解释】(1)用化学方程式表示实验二中有关反应的化学反应原理:CaCO3+2HCl=CaCl2+H2O+CO2 ↑,Ca(OH)2+CO2=CaCO3↓+H2O。实验三变澄清可能发生的化学方程式是CaCO3 +H2O+CO2=Ca(HCO3)2 。【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水,硬水泡沫少,软水泡沫多。
点睛∶本题主要考查通过实验探究水垢的主要成分。
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属钛的熔点高、密度小、抗腐蚀性能好,所以在航天、医疗和化学工业中用途广泛。已知钛原子的质子数为22,中子数为26,则该元素原子的电子数为( )
A. 48 B. 26 C. 22 D. 4
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是
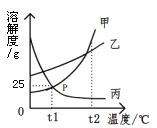
A. P点表示甲、丙两种物质的饱和溶液质量相等
B. t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
C. t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1∶4
D. 将三种物质的溶液从t2℃降至t1℃,溶质质量分数最小的一定是丙物质
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制取常见气体所需装置如下图所示,请回答有关问题。
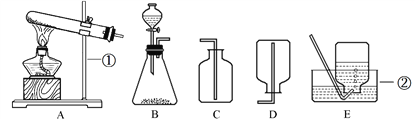
(1)写出图中标号仪器的名称: ①___,②___。
(2)实验室用A装置制氧气的化学方程式是___,收集装置是___(填字母)。
(3)实验室制取二氧化碳的化学方程式是___,装置的组合是___。
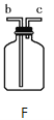
(4)实验室收集SO2可以选用C,据此可知:SO2具有的性质是__ ,由于SO2 ____,最好用下图F装置收集,应该是___管进气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】日常生活中应用缓慢氧化的例子有很多,下列反应中不包含缓慢氧化的是 ( )
A. 食物腐败 B. 酒的酿造
C. 酒精的燃烧 D. 动植物的呼吸
-
科目: 来源: 题型:
查看答案和解析>>【题目】括号内是区别下列各组常见物质的方法,其中错误的是
A.白酒和食醋(闻气味)
B.氧气与二氧化碳(加澄清石灰水,振荡)
C.蒸馏水与盐水(观察是否透明)
D.水和过氧化氢溶液(加MnO2,振荡)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关氧气的“自述”错误的是 ( )
A. 我不易溶于水
B. 我具有可燃性
C. 我的化学性质比较活泼
D. 我能供给呼吸
相关试题

