【题目】化学是一门以实验为基础的学科。根据下图回答问题:

(1)仪器①的名称是______________。
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为___________________,要收集一瓶较纯净的气体,选用的发生和收集装置是______(填字母序号,下同)。
(3)实验室制取二氧化碳,发生装置要能达到“控制反应速度”,需要选用的仪器和用品有_________;反应的化学方程式为__________;选用的收集装置是C,则二氧化碳从____(填导管的序号)进入。
(4)装置H中,向干燥石蕊试纸的a端滴入蒸馏水,观察到的实验现象为_______,该实验得出的结论为___________。
(5)小明同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(各部分连接紧密后,如下图所示)。该实验设计的优点有:能控制反应速率和____________。(写一点即可)

参考答案:
【答案】 锥形瓶 2KClO3![]() 2KCl + 3O2↑ AD BEG CaCO3 +2HCl==CaCl2 + CO2↑+H2O m 试纸a端变成红色 二氧化碳与水反应生成了碳酸 控制反应的停止和发生
2KCl + 3O2↑ AD BEG CaCO3 +2HCl==CaCl2 + CO2↑+H2O m 试纸a端变成红色 二氧化碳与水反应生成了碳酸 控制反应的停止和发生
【解析】本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的性质等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)据图可以看出,①是锥形瓶;
(2)实验室用氯酸钾和二氧化锰的固体混合物加热生成氯化钾和氧气,该反应的化学方程式为2KClO3![]() 2KCl + 3O2↑;要收集一瓶较纯净的氧气应选用排水法,所以收集一瓶较纯净的气体,选用的发生和收集装置是AD;
2KCl + 3O2↑;要收集一瓶较纯净的氧气应选用排水法,所以收集一瓶较纯净的气体,选用的发生和收集装置是AD;
(3)注射器可控制液体滴加速度,能控制反应的速度。要装配一套“控制反应速度”的气体发生装置,可用BEG;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式是:CaCO3 +2HCl==CaCl2 + CO2↑+H2O;二氧化碳的密度比空气大,可用排空气法收集,采用C装置是应从m端通入CO2;
(4)二氧化碳本身不呈酸性,二氧化碳与水反应生成了碳酸,碳酸呈酸性,所以试纸a端变成了红色;
(5)通过挤捏或放开塑料管,可以控制液体与固体的接触或分离,可以控制液体与固体的接触或分离的速度。该实验设计的优点有:能控制反应速率和控制反应的停止和发生。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如下图,向一定量AgNO3溶液中加入铜和锌的混合粉末,充分反应后进行操作a得溶液甲和固体乙。

(1)进行的实验操作a的名称是_________,若乙中含有锌、铜、银三种固体,则溶液甲中所含的金属离子符号为_____,此时向固体乙中加入稀盐酸,发生反应的化学方程式为________________;
(2)若溶液甲显蓝色,是因为____________(用化学反应方程式表示),此时固体乙中一定含有的物质是_________(填化学符号)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】高纯氧化锌广泛应用于电子工业,某研究小组设计如图流程制备高纯氧化锌。
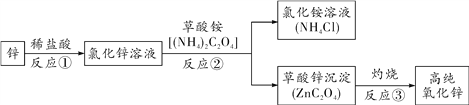
(1)反应①的化学方程式为________________________。
(2)反应②的基本反应类型是________________。
(3)反应②后进行的分离操作名称是________,若得到的NH4Cl溶液有浑浊,由于操作造成的原因可能是____________________(写出一种即可)。
(4)反应③属于分解反应,除得到氧化锌外还生成2种常见气体,其化学式为________、________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】老师在《探究燃烧的条件》教学中改进了教材中的实验,如下图所示,在铜片上罩上烧杯,请根据图示和资料信息回答有关问题:资料信息:白磷和红磷的着火点分别是40℃、240℃。
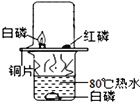
(1)铜片上的红磷不燃烧,是因为____________;
(2)罩上烧杯的作用_______________;
(3)如果让水中的白磷在水下燃烧,应采取的措施是___________;
(4)通过以上实验事实证明,燃烧必须同时具备下列条件:
①可燃物;②氧气(或空气); ③_______________;
(5)写出白磷燃烧的化学方程式为_________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图中的①②是钙元素、硒元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图:
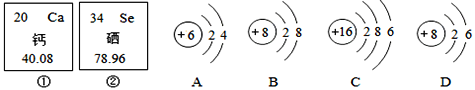
请回答:
(1) 钙元素的原子序数为________,硒元素的相对原子质量为_______;
(2) B所表示的粒子符号为___________;
(3) A、B、C、D四种粒子中属于同种元素的是_____(填序号,下同),化学性质相似的是_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A、B为两种黑色粉末状固体,E是能与血红蛋白结合的有毒气体,D为红色单质。A、B、C、D、E、F六种物质之间的转化关系如下图所示,请回答:
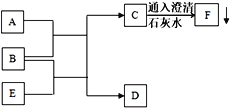
⑴ B、E两种物质的化学式分别是:B_________,E ________;
⑵ A和B反应的化学方程式____________;
⑶ C→F的化学方程式 ________________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学用语与意义对应正确的是
A. H2(两个氢分子) B. NH4SO4(硫酸铵)
C. n
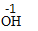 (n个氢氧根离子) D.
(n个氢氧根离子) D. 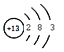 铝原子的结构示意图)
铝原子的结构示意图)
相关试题

