【题目】实验室欲配制84g质量分数为10%的碳酸氢钠溶液用于实验,请计算:
(1)需要碳酸氢钠的质量为 g.
(2)已知碳酸氢钠与稀盐酸发生如下反应:NaHCO3+HCl═NaCl+CO3↑.向84g 10%的碳酸氢钠溶液 中加入一定量的稀盐酸,恰好完全反应,反应后剩余溶液质量为117g(假设生产的气体全部逸出).求:
①生成氯化钠的质量;
②所得溶液中溶质质量分数.
参考答案:
【答案】5.85g;5%
【解析】
试题分析:
(1)需要碳酸氢钠的质量为:84g×10%=8.4g,故填:8.4.
(2)设生成氯化钠的质量为x,
NaHCO3+HCl═NaCl+H2O+CO2↑,
84 58.5
8.4g x
![]() ,
,
x=5.85g,
所得溶液中溶质质量分数为:![]() ×100%=5%
×100%=5%
答:生成了5.85g氯化钠,氯化钠溶液中氯化钠的质量分数是5%
-
科目: 来源: 题型:
查看答案和解析>>【题目】某学习同学在做“氢气在空气中燃烧”实验时,对生成物的成分产生了质疑:水和过氧化氢具有相同的组成元素,那么氢气在空气中燃烧除生成水外,是否有过氧化氢生成呢?带着疑问,该小组同学利用如图所示实验装置进行了以下探究.
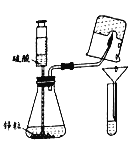
【提出猜想】氢气在空气中燃烧除生成水,还有过氧化氢生成.
【查阅资料】
(1)在一定条件下(低温环境下),氢气在空气中燃烧除生成水外,还有过氧化氢生成.
(2)过氧化氢溶液能使无色的淀粉碘化钾溶液变蓝色.
【实验探究】
主要步骤
主要现象
实验结论
①将注射器内的稀硫酸接入到盛有锌粒的锥形瓶中
在锌粒表面有 产生
反应的化学方程式为
②点燃经验纯后的氢气,用底部结有并冰的小烧杯罩在火焰上方,用漏斗和试管收集所得液体.向试管
中加入
氢气燃烧产生淡蓝色火焰,试管中液体由无色变 色
氢气在空气中燃烧有过氧化氢生成
【评价反思】实验中将氢气燃烧的火焰对着冰,冰的作用是 (填序号).
①用冰有利于吸收氢气燃烧产生的气体
②用冰创设低温环境,使部分氢气燃烧产生一定量的过氧化氢
③有利于生成的过氧化氢和较低的温度下溶入冰融化成的水中,便于收集
【拓展分析】除氢气和氧气反应会生成两种氧化物外,金属钠也具有类似的化学性质:金属钠露置在空气中与氧气反应,生成氧化钠;钠在空气中燃烧,生成过氧化钠(Na2O2).请写出钠在空气中燃烧的化学方程式: .此反应的基本类型是 反应.
-
科目: 来源: 题型:
查看答案和解析>>【题目】把金属X放入AgNO3溶液中,X表面有银白色固体析出;若放入FeSO4溶液中,无明显现象。则X、Ag、Fe三种金属活动性由强到弱的顺序正确的是
A.Fe、X、Ag B.X、Fe、Ag C.Fe、Ag、X D.Ag、X、Fe
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化肥属于磷肥的是
A.NH4NO3 B.Ca(H2PO4)2 C.CO(NH2) D.K2CO3
-
科目: 来源: 题型:
查看答案和解析>>【题目】新修订的《环境空气质量标准》增加了PM2.5监测指标,PM2.5是指大气中直径小于或等于2.5微米的可吸入颗粒物。下列做法不会改变PM2.5检测结果的是
A.海水晒盐 B.燃放鞭炮
C.露天焚烧垃圾 D.工厂排放烟尘
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质露置于空气中,质量会减小的是
A.浓硫酸 B.浓盐酸 C.氢氧化钠 D.氯化钠
-
科目: 来源: 题型:
查看答案和解析>>【题目】一壶水烧开了,壶盖被顶开,这是因为
A.水分子间隔变大 B.水分子体积变大
C.水分子数目增多 D.水分子质量变大
相关试题

