【题目】小明同学利用不同装置测定空气中氧气的含量。
(1)小明先用图1中装置测定空气中氧气的含量。红磷燃烧的现象是__________,放热,
反应的化学方程式是___________________________________。小明同学得出的结论:空气中氧气的体积约占1/5。能得出此结论的实验现象为___________________________________。

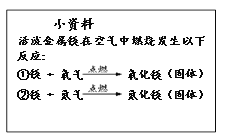
(2)完成实验后,小明想能否使用其它物质代替红磷进行上述实验,并且查阅了相关资料,如右所示。下列物质中,不能用于代替红磷进行该实验的有________(填字母序号)。
A. 木炭 B. 铁丝 C. 镁条 D.硫
(3)小明又设计了图2装置测定空气中氧气的含量 [查阅资料]白磷的着火点40℃。
[实验准备]锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。
[实验探究]装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。

[现象分析]①将锥形瓶底部放入热水中,白磷被引燃;
②在整个实验过程中,可观察到气球的变化是____________;
③待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象一是:注射器中的水自动喷射出来,原因是_________________;现象二是:当注射器中的水还剩约________mL时停止流下。
参考答案:
【答案】 产生大量白烟 4P+5O2![]() 2P2O5 烧杯中的水倒吸入集气瓶中,约占瓶中空气体积的1/5 ABCD 先膨胀,后缩小 白磷燃烧消耗瓶中的氧气,使瓶中气压减小 4
2P2O5 烧杯中的水倒吸入集气瓶中,约占瓶中空气体积的1/5 ABCD 先膨胀,后缩小 白磷燃烧消耗瓶中的氧气,使瓶中气压减小 4
【解析】测定空气中氧气的含量。(1) 用图1中装置测定空气中氧气的含量。红磷燃烧的现象是产生大量白烟,放热,反应的化学方程式是∶4P+5O2![]() 2P2O5。得出的结论:空气中氧气的体积约占1/5。能得出此结论的实验现象为∶烧杯中的水倒吸入集气瓶中,约占瓶中空气体积的1/5。(2)不能用于代替红磷进行该实验的有∶木炭生成二氧化碳气体;铁丝在氧气中不燃烧;镁条不仅与氧气反应,还有氮气,二氧化碳反应;硫生成二氧化硫气体。(3) 图2装置测定空气中氧气的含量。[查阅资料]白磷的着火点40℃。[实验准备] 该装置气密性良好。[实验探究] [现象分析]①将锥形瓶底部放入热水中,白磷被引燃;②在整个实验过程中,可观察到气球的变化是先膨胀,后缩小,燃烧放热膨胀,消耗了氧气,冷却后缩小。③注射器中的水自动喷射出来,原因是白磷燃烧消耗瓶中的氧气,使瓶中气压减小;现象二是:当注射器中的水还剩约4 mL时停止流下,230mL×
2P2O5。得出的结论:空气中氧气的体积约占1/5。能得出此结论的实验现象为∶烧杯中的水倒吸入集气瓶中,约占瓶中空气体积的1/5。(2)不能用于代替红磷进行该实验的有∶木炭生成二氧化碳气体;铁丝在氧气中不燃烧;镁条不仅与氧气反应,还有氮气,二氧化碳反应;硫生成二氧化硫气体。(3) 图2装置测定空气中氧气的含量。[查阅资料]白磷的着火点40℃。[实验准备] 该装置气密性良好。[实验探究] [现象分析]①将锥形瓶底部放入热水中,白磷被引燃;②在整个实验过程中,可观察到气球的变化是先膨胀,后缩小,燃烧放热膨胀,消耗了氧气,冷却后缩小。③注射器中的水自动喷射出来,原因是白磷燃烧消耗瓶中的氧气,使瓶中气压减小;现象二是:当注射器中的水还剩约4 mL时停止流下,230mL×![]() =46mL, 50mL-46mL=4 mL。
=46mL, 50mL-46mL=4 mL。
点睛∶本实验成功的关键①制取气密性良好②反应物过量,生成物只能是固体③冷却后测量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图所示实验装置回答问题:
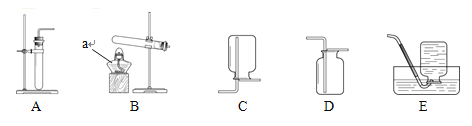
(1)图中仪器a的名称为 _____。
(2)实验室用过氧化氢制取氧气,应选用的发生装置是 _____(填字母序号),该反应的化学方程式为 _____________。
(3)若用B装置制备氧气,发生反应的化学方程式为 _____________。
(4)若要收集较纯净的氧气,应选用的收集装置是 _____(填字母序号)。
(5)若用排空气法收集氧气时,检验氧气是否收集满的方法是 ______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】十八世纪末,人们就开始了对水的组成的研究。
(1)英国科学家普利斯特里把“易燃空气”(氢气)和空气混合后盛在干燥、洁净的玻 璃瓶中,当用电火花点火时发出震耳的爆鸣声,且玻璃瓶内壁上出现了液滴。不久,卡 文迪许用纯氧气代替空气进行上述实验,确认所得液滴是水,该反应的化学方程式是_________________。
(2)基于卡文迪许实验,可得出的关于水的组成的结论是:水是由_________________组成的。
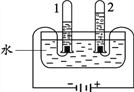
(3)后来,科学家进一步利用电解水实验(如右图所示)证明水的组成,该反应的化学方程式是_____________________, 实验中得到氧气的试管是________ (填“1”或“2”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学设计了如下2个实验验证质量守恒定律。
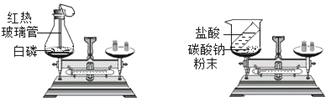
实验1 实验2
(1)上述实验方案中,合理的是________(填“实验1”或“实验2”)。
(2)实验2中,天平的指针________(填字母序号)。
A. 向左偏转 B. 不偏转 C. 向右偏转
(3)如右图所示,点燃蜡烛后,电子称示数逐渐减小。蜡烛减小的质量________(填“大于”“等于”或“小于”)燃烧后生成物的总质量。

-
科目: 来源: 题型:
查看答案和解析>>【题目】合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如下:
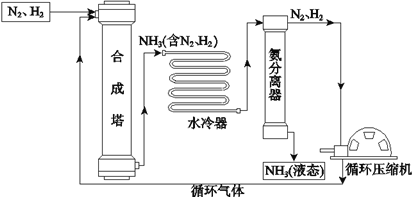
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是____________。
(2)上述反应中,一定发生改变的是_____(填字母序号)。
A.元素种类 B. 分子种类 C. 原子种类
(3)生产过程中可循环使用的物质是_____。
(4)根据表中的数据回答问题。
物质
H2
N2
NH3
沸点/℃(1.01×105 Pa)
–252
–195.8
–33.35
在1.01×105 Pa时,要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在________℃≤ T <________℃。
-
科目: 来源: 题型:
查看答案和解析>>【题目】柴油机尾气中的主要污染物是氮氧化物,某种尾气处理技术利用氨气与氮氧化物发生化学反应①和②,降低污染物排放,反应的微观示意图如下:
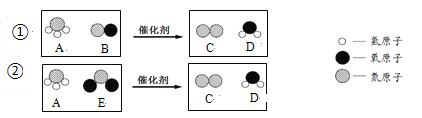
(1)一个A分子是由_____个原子构成的。
(2)上述反应所涉及的物质中,属于氧化物的是_____(填字母序号)。
(3)反应①的化学方程式为_____________________。
(4)反应②涉及的含氮元素物质中,氮元素化合价最低的是_____(填字母序号)。
-
科目: 来源: 题型:
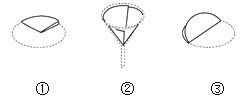
查看答案和解析>>【题目】(1)制作过滤器的过程如下图所示,其正确操作顺序为______(填序号)。
(2)在过滤操作中,玻璃棒的作用是_____________________。
(3)过滤时漏斗下端管口应____________________________ 。
(4)举出一个生活中应用过滤原理的实例:____________________________。
相关试题

