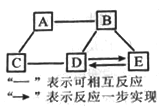
【题目】A~E均为初中化学常见的物质,它们之间的关系如图所示(部分物质已经略去)。已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%, 其水溶液呈蓝色,常用来配制农药波尔多液;D属于碱;E属于盐。则C的化学式为__________;A与B反应的化学方程式为__________;E转化为D的化学方程式为__________。
参考答案:
【答案】 CuSO4 Fe+2HCl=FeCl2+H2↑ Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
【解析】A是目前世界上年产量最高的金属,则A是铁;B是胃酸的主要成分,则B是盐酸;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液,则C是硫酸铜;D属于碱,E属于盐,且E、D能与HCl反应,D能与CuSO4反应,并且常见,则D可能是NaOH,E可能是Na2CO3。C的化学式为CuSO4;A与B的反应是铁与盐酸反应,反应的化学方程式为Fe+2HCl=FeCl2+H2↑;E转化为D是碳酸钠转化为氢氧化钠,反应的化学方程式为Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图装置可以做 CO还原Fe2O3的实验并检验该反应的气体生成物, 已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。

(1)写出B装置玻璃管内反应的化学方程式___________。
(2)从环保角度考虑,请写出一种尾气处理方法。___________
(3)若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因。___________
-
科目: 来源: 题型:
查看答案和解析>>【题目】碱式碳酸铜[Cu2(OH)2CO3]受热分解生成氧化铜、水和二氧化碳,反应的化学方程式为__________;充分加热24g含氧化铜的碱式碳酸铜固体,若反应前后固体中铜元素的质量分数之比为3∶4,则该反应生成水和二氧化碳的质量之和为__________ g。
-
科目: 来源: 题型:
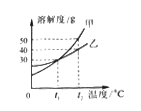
查看答案和解析>>【题目】下图是甲、乙两种固体的溶解度曲线。甲和乙的溶解度相等时的温度为__________℃;t2℃时,分别用甲、乙的固体配制相同质量甲、乙的饱和溶液,所需要水的质量关系为:甲______乙(填“大于” “小于”或“等于”);t2℃时,将75g甲的饱和溶液与50g水混合后所得溶液中溶质的质量分数为__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】酸、碱、盐在生产和生活中有广泛的应用。
(1)焙制糕点所用发酵粉中含有碳酸氢钠,其俗名为__________( 填字母代号)。
a.纯碱 b.烧碱 c.苏打 d.小苏打
(2)下图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。

①根据图示判断,该实验是将______ ( 填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
②滴入溶液体积为V2mL时,溶液中的溶质为__________。
(3)为除去粗盐水中的可溶性杂质MgSO4、CaCl2,某化学小组设计了以下方案:
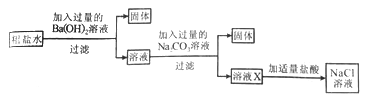
①过滤用到的玻璃仪器有烧杯、玻璃棒和__________。
②写出加入Ba(OH)2溶液时反应的化学方程式___________ ( 提示:微溶物不形成沉淀)
③溶液X中含有哪些杂质? __________请设计实验加以证明。(简要写出实验步骤和现象) ___________
(4)为测定某石灰石样品中碳酸钙的质量分数,称取10g石灰石(杂质不参加反应)放入烧杯中,加入100g稀盐酸,二者恰好完全反应,反应后烧杯中利余物质的总质量为106.7 g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数为___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关叙述、对应的方程式,所属基本反应类型都正确的是
A. 拉瓦锡研究空气成分 HgO
 Hg + O2↑ 分解反应
Hg + O2↑ 分解反应B. 生石灰作干燥剂 CaO + H2O == Ca(OH)2 化合反应
C. 三氧化硫与氢氧化钠溶液反应 SO3 + NaOH == Na2SO3 + H2O 复分解反应
D. 葡萄糖在人体内氧化 C6H12O6 + 6O2
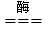 6CO2 + 6H2O 氧化反应
6CO2 + 6H2O 氧化反应 -
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是
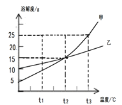
A. 乙中含有少量甲,可用冷却热饱和溶液的方法提纯甲
B. t3℃时,甲的溶液溶质质量分数一定大于乙的溶液溶质质量分数
C. t3℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t2℃,析出晶体的质量甲一定大于乙
D. t1℃时,乙的不饱和溶液只有通过蒸发溶剂的方法才能转变成饱和溶液
相关试题

