【题目】某兴趣小组同学利用图1装置制取气体并探究气体的某些性质.
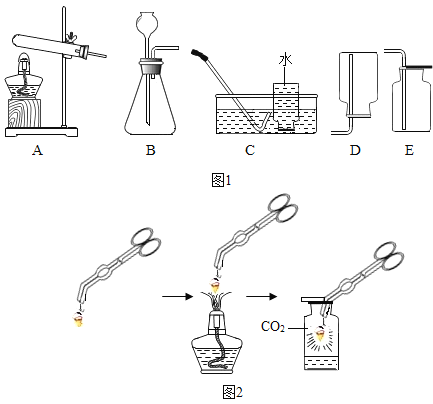
(1)制取气体
①若选择A与C组合制取氧气,反应的化学方程式为__.
②用石灰石和稀盐酸制取CO2的化学方程式为__,选用的发生与收集装置是__(填标号).连接好装置,将药品加入装置前应进行的操作是__.
(2)探究气体的性质
某同学在空气中点燃镁条,想利用CO2来熄灭燃烧的镁条,结果发现镁条在充满CO2的集气瓶中没有熄灭反而剧烈燃烧,集气瓶内壁出现黑色固体,瓶底出现白色固体,实验过程如图2所示.请回答:
①夹持镁条的仪器名称是__;
②生成的黑色固体是__(写化学式);
③查阅资料:MgO、Mg(OH)2、MgCO3均为难溶于水的白色固体.同学讨论后认为白色固体不可能是Mg(OH)2,理由是__.
④为进一步确定白色固体的成分,进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取白色固体于试管中,加入足量稀盐酸 | __ | 白色固体不是MgCO3,而是MgO |
⑤镁在CO2中燃烧的化学方程式为__;通过上述探究,你对燃烧或灭火的新认识是__.
【答案】2KClO3![]() 2KCl+3O2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ BE 检查装置的气密性 坩埚钳 C 反应物中没有氢元素 白色固体逐渐消失,没有气泡冒出 2Mg+CO2
2KCl+3O2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ BE 检查装置的气密性 坩埚钳 C 反应物中没有氢元素 白色固体逐渐消失,没有气泡冒出 2Mg+CO2![]() 2MgO+C 燃烧不一定有氧气参加(合理即可);
2MgO+C 燃烧不一定有氧气参加(合理即可);
【解析】
(1)A装置试管口没有放棉花,不能用于高锰酸钾制氧气,可用于氯酸钾制氧气,氯酸钾制氧气需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气化学方程式为2KClO3![]() 2KCl+3O2↑;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;实验装置选BE,连接好装置,将药品加入装置前应进行的操作是:检查装置的气密性;故答案为:①2KClO3
2KCl+3O2↑;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;实验装置选BE,连接好装置,将药品加入装置前应进行的操作是:检查装置的气密性;故答案为:①2KClO3![]() 2KCl+3O2↑;②CaCO3+2HCl=CaCl2+H2O+CO2↑;BE;检查装置的气密性。
2KCl+3O2↑;②CaCO3+2HCl=CaCl2+H2O+CO2↑;BE;检查装置的气密性。
(2)如图2所示,夹持镁条的仪器名称是坩埚钳,生成的黑色固体是碳,同学讨论后认为白色固体不可能是Mg(OH)2,理由是:反应物中没有氢元素;实验如下:取白色固体于试管中,加入足量稀盐酸;当观察到白色固体逐渐消失,没有气泡冒出;因此白色固体不是MgCO3,而是MgO;镁在CO2中燃烧生成氧化镁和碳,化学方程式为2Mg+CO2![]() 2MgO+C;我对燃烧或灭火的新认识是:燃烧不一定有氧气参加、二氧化碳支持某些金属的燃烧等;故答案为:①坩埚钳;②C;③反应物中没有氢元素;④白色固体逐渐消失,没有气泡冒出;⑤2Mg+CO2
2MgO+C;我对燃烧或灭火的新认识是:燃烧不一定有氧气参加、二氧化碳支持某些金属的燃烧等;故答案为:①坩埚钳;②C;③反应物中没有氢元素;④白色固体逐渐消失,没有气泡冒出;⑤2Mg+CO2![]() 2MgO+C;燃烧不一定有氧气参加(合理即可)。
2MgO+C;燃烧不一定有氧气参加(合理即可)。

