【题目】化学用语是学习化学的重要工具。
(1)用化学符号填空:
①氨气分子_ _;②碳酸钙中阴离子 ;③ 过氧化氢中氧元素的化合价 ;④侯氏联合制碱法中的“碱”是__ _;⑤最简单的有机物是 ;
⑥食品袋中的“双吸剂”
(2) 完成下列变化的化学方程式,并按要求填空。
①湿法冶铜: ; 反应类型;
②高炉炼铁的原理: ;
③实验室用氯酸钾制取氧气的反应: 。
参考答案:
【答案】(1)①NH3②CO32-③-1④Na2CO3⑤CH4⑥Fe(2)①Fe + CuSO4 == FeSO4 + Cu;置换反应;②3CO+ Fe2O3![]() 2Fe + 3CO2③2KClO3
2Fe + 3CO2③2KClO3![]() 2KCl + 3O2↑
2KCl + 3O2↑
【解析】
试题分析:(1)①由分子的表示方法可知,为NH3;②碳酸钙中的阴离子为碳酸根离子,由离子的表示方法可知,为CO32-;③H2O2中氢元素的化合价为+1,由化合物中各元素的化合价代数和为0,设氧元素的化合价为x,那么+1×2+x×2=0,x=-1;④是纯碱-碳酸钠,化学式为Na2CO3 ;⑤最简单的有机物为甲烷,CH4 ;⑥铁-Fe生锈是和氧气、水蒸气反应,可以作为吸收氧气和水的双吸剂;(2)①即用铁和铜盐溶液反应,可以是Fe + CuSO4 == FeSO4 + Cu;为单质和化合物生成另一种单质和化合物,属于置换反应;②为用一氧化碳还原氧化铁3CO+ Fe2O3![]() 2Fe + 3CO2;③2KClO3
2Fe + 3CO2;③2KClO3![]() 2KCl + 3O2↑。
2KCl + 3O2↑。
-
科目: 来源: 题型:
查看答案和解析>>【题目】人体内缺少下列某种元素会造成食欲不振,生长迟缓,发育不良,该元素是
A.碘 B.铁 C.钙 D.锌
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业。有一种碳酸盐矿石其主要成分为碳酸钡和碳酸钙,以此矿石为原料生产碳酸钡的流程如下图所示。
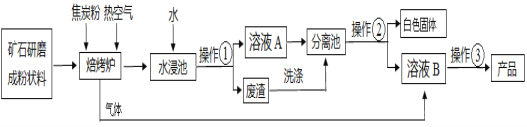
【已知】:碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应。但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度。
温度/℃
0
40
80
Ca(OH)2溶解度/g
0.187
0.141
0.094
Ba(OH)2溶解度/g
1.67
8.22
101.4
(1)写出焙烧炉中含钡元素物质发生反应的化学方程式: ;
(2)除了水之外,进入分离池中的物质是 和 ,请你推测分离池中操作②的方法是 (选填“A”或“B”)。
A.降温,过滤; B.加热,过滤
(3)写出由溶液B制取产品的化学方程式: ;
(4)以下相关说法正确的是 。
A.对矿石进行预处理“研磨成粉状”有利于充分反应
B.焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态
C.焙烧炉内只涉及分解反应
D.废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料
-
科目: 来源: 题型:
查看答案和解析>>【题目】重庆山峡博物馆最近启用新购置的“真空充氮杀虫灭菌消毒机”来处理和保护文物,将文物放入该机器内(氮气浓度:99.99%),密封三天,好氧菌和丝状霉菌都被杀灭,下列有关氮气在该机器内的工作原理说法不正确的是( )
A. 氮气难溶于水
B. 高浓度的氮气能抑制菌类的生长
C. 氮气化学性质不活泼
D. 氮气不能供给呼吸
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各组物质在pH=3的溶液中能大量共存,且形成无色溶液的是
A.KCl、NaCl、Na2CO3 B.AgNO3、NaNO3、HCl
C.CuSO4、H2SO4、MgCl2 D.KNO3、Ca(NO3)2、NH4Cl
-
科目: 来源: 题型:
查看答案和解析>>【题目】厨房里发生的下列变化为物理变化的是( )
A.天然气燃烧 B.铁锅生锈 C.开水沸腾 D.蔬菜腐烂
-
科目: 来源: 题型:
查看答案和解析>>【题目】氢化钙(CaH2)固体是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物。
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气。
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,图1是模拟制取装置:


(1)装置B的作用是 ;装置D的作用是 ;
(2)利用图1实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞, (请按正确的顺序填入下列步骤的序号)。
①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此断,上述实验确有CaH2生成.
①写出CaH2与水反应的化学方程式 ;
②该同学的判断不正确,原因是 。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,方法为 ;
②装入药品,按图2(固定装置省略)所示连接仪器。
③调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0 mL。
④将Y型管中水与氢化钙样品混合,操作为 。
⑤反应结束,冷却至室温,再次 ,读取液面所在刻度数据为110.0 mL。
回答下列问题:
(5)如何判断样品与水完全反应: 。
(6)反应生成氢气的体积为 mL。
(7)已知该实验条件下,氢气的密度为0.09 mg/mL。样品中氢化钙的纯度为 。(结果精确到0.1%)(2分)
(8)结果讨论:(填“偏大” 、“偏小” 、“准确”)
①Y型管中残留有氢气,对测定结果的影响是 。
②未冷却至室温即读数,对测定结果的影响是 。
相关试题

