【题目】如图为实验室模拟炼铁及部分气体的性质实验装置图,请回答下列问题:
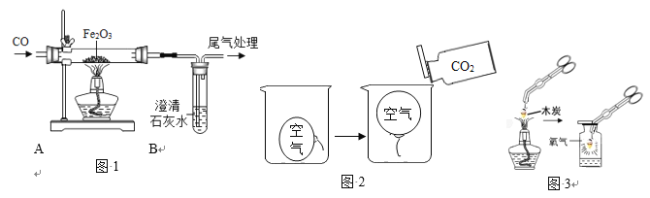
(1)图 1 为 CO 还原氧化铁的实验。
①开始时,需先通一段时间的 CO,后点燃酒精喷灯,其原因是___________。
②实验过程中,装置 B 中澄清石灰水变浑浊,则发生化学反应的方程式为_______________。
(2)如图 2 所示,根据气球浮起的现象可以说明CO2的性质是____________。
(3)如图 3 所示,木炭在空气和氧气中反应的现象不同,说明燃烧的剧烈程度与_________有关。
【答案】防止 CO 与空气混合加热,引起爆炸 CO2 + Ca(OH)2= CaCO3 ↓+H2O 密度比空气大 氧气的浓度
【解析】
(1)①开始时,需先通一段时间的CO,把管内的空气排出,然后点燃酒精喷灯加热,其原因是防止 CO 与空气混合加热,引起爆炸。
②实验过程中,装置 B 中澄清石灰水变浑浊,是因为二氧化碳气体与氢氧化钙反应生成难溶的碳酸钙沉淀和水,反应的方程式为CO2 + Ca(OH)2= CaCO3 ↓+H2O。
(2)烧杯中气球内装的是空气,倒入二氧化碳时,气球浮起来,说明CO2的密度比空气的大。
(3)空气中氧气的浓度较低,木炭在空气燃烧发出红光,放出热量,而集气瓶中的氧气浓度较高,木炭在氧气剧烈燃烧,发出白光,放出热量,这说明燃烧的剧烈程度与氧气的浓度有关。

