13.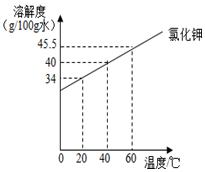 根据下表实验,回答相关问题
根据下表实验,回答相关问题
①实验步骤Ⅱ中加入Xg氯化钾,X=9g.
②实验步骤Ⅲ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
③冷却至20℃,烧杯中的现象是有固体析出.
④有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等浓度的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
 根据下表实验,回答相关问题
根据下表实验,回答相关问题| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 在盛有100g水的烧杯中,加入25g氯化钾,搅拌,恢复到20℃. | 全部溶解 |
| Ⅱ | 再加Xg氯化钾,搅拌,恢复到20℃,恰好饱和. | 全部溶解 |
| Ⅲ | 再加6g氯化钾,搅拌,恢复到20℃ | 固体不溶 |
| Ⅳ | 加热 | 全部溶解 |
| Ⅴ | 冷却至20℃ | 有固体析出 |
②实验步骤Ⅲ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
③冷却至20℃,烧杯中的现象是有固体析出.
④有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等浓度的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
分析 ①根据20℃氯化钾的溶解度考虑;②饱和溶液再加入溶质,不再溶解,固体不溶解,仍然是饱和溶液考虑;③冷却至20℃,烧杯中的现象是有固体析出;④根据溶质质量分数相等的溶液中加入硝酸银后生成沉淀质量相等考虑.
解答 解:①20℃氯化钾的溶解度考虑是34g,100g水中最多溶解34g,已经加入了25g,所以还需加入34g-25g=9g;
②饱和溶液再加入溶质,不再溶解,固体不溶解,说明是饱和溶液;
③冷却至20℃,此时已经加入了40g氯化钾,最多溶解34g,所以烧杯中的现象是有固体析出;
④溶质质量分数相等的溶液中加入硝酸银后生成沉淀质量相等,根据上面的分析可知,Ⅱ、Ⅲ、Ⅴ都是饱和溶液,溶质质量分数相等.
故答案为:①9;②饱和;③有固体析出;④3.
点评 解答本题关键是熟悉饱和溶液与不饱和溶液的转化方法.

