【题目】(9分)根据下列实验装置图,按要求回答下列问题:
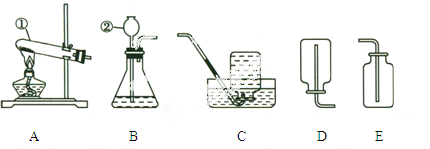
(1)写出标有序号的仪器名称:①______________;②______________。
(2)实验室制取CO2的化学反应方程式为__________________________;制取并收集该气体应选择的装置是______________(填序号);若想控制反应速率,可以将仪器②用______________代替;检验该气体的方法是_____________________________(写化学方程式)
(3)若用高锰酸钾制取氧气,化学方程式为: _____ ,选择的发生装置为 ____(填代号).实验结束后,通过溶解、 、洗涤、干燥等操作步骤,可以从生成物中分离出二氧化锰.
参考答案:
【答案】(1)试管;长颈漏斗;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;BE;分液漏斗或注射器;CO2+Ca(OH)2=CaCO3↓+H2O;
(3)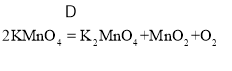 ;A;过滤.
;A;过滤.
【解析】(1)a是试管,b是长颈漏斗;
(2)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;该反应属于固液常温型,二氧化碳能够溶于水,密度比空气大,用向上排空气法收集,故用BE;分液漏斗可控制反应速率;二氧化碳气体能使澄清石灰水变浑浊,所以检验二氧化碳气体,是把气体通入澄清的石灰水中,若变浑浊,则为二氧化碳,其化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
(3)若用高锰酸钾制取氧气,反应的化学方程式为:
该反应需要加热,应用A装置作为发生装置;实验结束后,通过溶解、过滤、洗涤、干燥等操作步骤,可以从生成物中分离出二氧化锰.故填: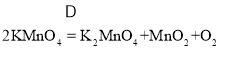
试题分析:(1)根据仪器的用途书写名称;(2)根据实验室选择气体发生装置的依据是反应物的状态和反应条件,气体收集装置选择的依据为气体的密度和溶解性;实验室用大理石和稀盐酸反应制取二氧化碳,根据反应原理书写方程式;根据分液漏斗可以控制滴加液体的速率分析;根据二氧化碳的检验方法和操作分析;(3)根据高锰酸钾制取氧气属于固-固加热型分析;根据二氧化锰和锰酸钾的溶解性以及分离固体混合物的操作进行分析.
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分。
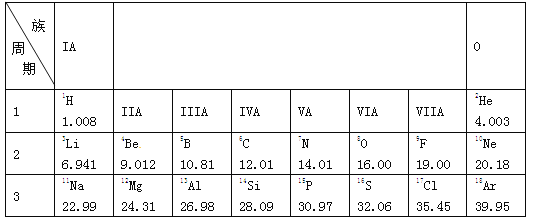
(1)查出碳的相对原子质量:__________,写出16号元素的元素符号:__________
(2)表中不同种元素最本质的区别是__________(填字母)
A. 质子数不同 B. 中子数不同
C. 相对原子质量不同 D .电子数不同
(3)利用元素周期表,人们对元素的认识进入全新的飞跃时期。近日,俄罗斯科学家宣布他们将人工合成第118号元素,则此元素的核电荷数为__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)去年冬天至今年春天,我国西南地区遭遇大范围持续干旱。全国人民团结一致,共同抗旱。

(1)有些村庄打深井取用地下水。检验地下水是硬水还是软水,可用的物质是 ,
(2)有些村民取浑浊的坑水作生活用水。有同学利用所学的知识将浑浊的坑水用右图所示的简易净水器进行净化,其中小卵石、石英沙的作用是 。
(3)如果地下水硬度大,或者坑水中病原微生物过多,都可以采取______ 方法,来降低硬度和杀灭病原微生物。
(4)身处旱区之外的我们能做些什么? (举一做法)
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)某实验小组利用图中所示仪器配制一定溶质质量分数的氯化钠溶液。
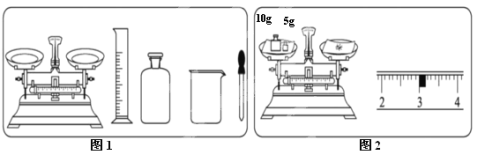
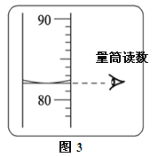
(1) 图1中缺少一种必须用到的玻璃仪器,仪器名称是:______________;用途是:___________________;
(2) 量取蒸馏水的体积读数如图3所示,则量取的水的体积为:___________。
(3) 该小组原计划配制的溶液中溶质与溶剂之比为______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】青铜是人类最早使用的铜、锡合金,下列说法中不正确的是( )
A.青铜属于纯净物 B.青铜属于金属材料
C.青铜的硬度比铜大 D.青铜耐腐蚀,易铸造成型
-
科目: 来源: 题型:
查看答案和解析>>【题目】(6分)由于碳元素的存在,让我们的世界绚丽多彩.在日常生活中,我们每一个人都应该传播“低碳”理念,倡导“低碳”生活,请按下列要求填空.
(1)天然气主要成分燃烧的化学方程式 ________________ .
(2)家用饮水机是利用活性炭的 作用除去饮用水中的部分杂质.
(3)人类向空气中排放大量的二氧化碳气体会导致大气产生 效应.
(4)有二氧化碳生成的置换反应 ___________________
(5)有二氧化碳参加的化合反应__________________________________________
(6)人体可直接利用的糖类﹣﹣葡萄糖,其化学式为C6H12O6,其相对分子质量为
-
科目: 来源: 题型:
查看答案和解析>>【题目】(3分)高氯酸(HClO4)和亚氯酸钠(NaClO2)在工业上有广泛的用途,其制备工艺流程如下:
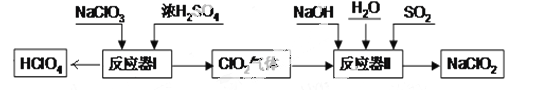
请回答下列问题:
(1)HClO4中Cl元素的化合价是 。
(2)反应器I中的生成物有HClO4、ClO2、NaHSO4、H2O,其中属于氧化物的是
(3)反应器II中发生反应的化学方程式为2ClO2+SO2+4NaOH=2NaClO2+X+2H2O,则X的化学式是 。
相关试题

