【题目】将15.8 g高锰酸钾放在试管里加热制取氧气,加热到不再产生气体为止。请回答:
(1)反应后剩余固体物质的质量________高锰酸钾的质量。(填“大于”“小于”“等于”)。推断的依据是__________________。
(2)剩余固体物质中含有的物质是________,各是________克?
参考答案:
【答案】⑴小于⑵质量守恒定律⑶锰酸钾和二氧化锰⑷锰酸钾是9.85g,二氧化锰是4.35g。
【解析】(1)反应后剩余固体物质的质量小于高锰酸钾的质量,生成了气体氧气;推断的依据是质量守恒定律,任何一个化学反应都必然遵循质量守恒定律。
(2)高锰酸钾加热完全反应后生成固体是锰酸钾和二氧化锰,反应后剩余固体物质中含有锰酸钾和二氧化锰。
解:设剩余的固体中含K2MnO4的质量为x,含MnO2的质量为y
2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
316 197 87
15.8 x y
![]() =
=![]() , x=9.85 g。
, x=9.85 g。
![]() =
=![]() , y=4.35 g。
, y=4.35 g。
答:剩余固体物质中含有K2MnO49.85克,含MnO24.35克。
点睛∶任何一个化学反应都必然遵循质量守恒定律。高锰酸钾加热完全反应后生成固体是锰酸钾和二氧化锰。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用下图装置探究可燃物燃烧的条件。

(1)铜片上白磷燃烧的化学方程式是______。
(2)观察到铜片上白磷燃烧、红磷不燃烧,可知可燃物燃烧的条件之一是______。
(3)水中白磷不燃烧的原因是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图表示某些物质间的转化关系(反应条件均略去)。其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属。B、D、X、E均为无色气体。请回答:

(1)X是_______ (填化学式)。
(2)B物质固态时的名称是______,该物质在实际生活中的一种用途是____________。
(3)写出下列反应的化学方程式。
①F+X→B+G:________________________________________。
②C→D+E:__________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在生活和实验室,我们可以利用过氧化氢制取氧气。
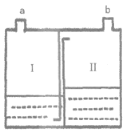
下图为家庭制氧机内桶构造示意图,桶上设有制氧剂投药口和出气口。
已知:
i. 制氧剂的主要成分是过碳酸钠和催化剂;
ii. 本产品用于人体保健吸氧,产生的氧气需通入水中净化。制氧时,从投药口中投入药品后,立即将其关闭。过碳酸钠加入水中后,分解产生过氧化氢;过氧化氢再在催化剂的作用下产生氧气。
(1)过氧化氢发生反应的文字表达为____________________________________。
(2)氧气的出口为__________(填“a”或“b”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】熊去氧胆酸(C24H40O4)被用来治疗胆结石。下列有关熊去氧胆酸的说法正确的是( )
A. 熊去氧胆酸中氢、氧元素的质量比为10:1
B. 392g熊去氧胆酸中含有40g的氢元素
C. 熊去氧胆酸中氧元素的质量分数最小
D. 熊去氧胆酸是由68个原子构成的
-
科目: 来源: 题型:
查看答案和解析>>【题目】在某密困容器中,有关物质变化过程的微观示意图如图所示,其中“
 ”代表氢原子,“
”代表氢原子,“ ”代表氧原子,下列有关说法中不正确的是( )
”代表氧原子,下列有关说法中不正确的是( )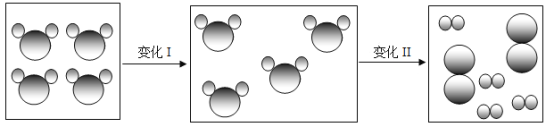
A. 变化1中发生了物理变化
B. 变化Ⅱ中发生了分解反应
C. 该密闭容器中,变化前后所有的物质均为氧化物
D. 在变化Ⅱ中,分子先分成原子,原子又重新结合成新的分子
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学实验中通过观察实验现象,不能达到实验目的( )
A. 证明蜡烛中含有氧元素
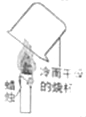
B. 探究同种溶质在不同溶剂中的溶解性
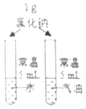
C. 验证氢氧化钠溶于水放热

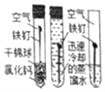
D. 探究钢铁锈蚀的原因
相关试题

