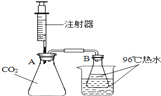
【题目】某研究性学习小组利用下图装置研究CO2与NaOH的反应。
已知:水的沸点与气体压强有关,气体压强小,沸点低;气体压强大,沸点高。
实验装置 | 实验步骤 |
| Ⅰ. A中充满CO2,B和烧杯中均盛有96℃以上但未沸腾的热水(假设实验过程无热量损耗)。 Ⅱ. 用注射器向A中注入一定量浓NaOH溶液,振荡后观察到B中热水沸腾。 Ⅲ.另取相同装置,用注射器向A中注入20mL水,振荡后观察到B中的热水没有沸腾。 |
(1)检查装置气密性:向上缓慢拉动注射器活塞至一定高度,松手后,观察到活塞_________,说明装置的气密性良好。
(2)步骤Ⅱ中注入浓NaOH溶液的体积应为_________mL。
(3)步骤Ⅲ的目的是排除_________的干扰。
(4)通过对比_________现象,可知CO2与NaOH确实发生了反应,其反应的化学方程式为_________。
参考答案:
【答案】 回到原处 20 水 Ⅱ中水沸腾,Ⅲ中水不沸腾 2NaOH + CO2 === Na2CO3+ H2O
【解析】(1)如果装置的气密性良好,向上缓慢拉动注射器活塞至一定高度,装置中的压强会变小,松手后,在外界大气压的作用下,活塞回到原处;
(2)步骤Ⅱ、Ⅲ要形成对照,所以注入浓NaOH溶液的体积应与注入水的体积相同,为20mL。
(3)步骤Ⅲ注入20mL水的目的是排除二氧化碳溶于造成的干扰;
(4)通过对比Ⅱ中水沸腾,Ⅲ中水不沸腾现象,可得CO2与NaOH确实发生了反应,二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:2NaOH + CO2 = Na2CO3+ H2O。
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳酸饮料是指在一定条件下充入二氧化碳气体的饮料,如可乐、雪碧、汽水等。生产碳酸饮料的主要流程如下:
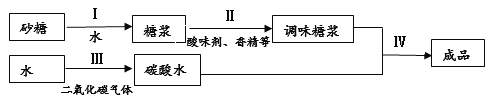
(1)步骤Ⅰ的操作是_________。
(2)步骤Ⅲ中发生反应的化学方程式为_________。
(3)成品饮料中所含的溶质有_________(至少写出2种)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】从CCTV-1每日发布的我国主要城市空气质量日报和预报中可看到,北京市属于空气污染较严重的城市之一,减少下列哪种气体的排放,可减少对空气污染
①二氧化硫②二氧化碳③氮气④二氧化氮
A.①② B. ③④ C.②③ D.①④
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质中含有氧气的是
A.空气 B.过氧化氢 C.高锰酸钾 D.二氧化锰
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2016年湖南省长沙市】空气是人类生产活动的重要资源,空气中能支持燃烧和供给呼吸的气体是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关氧气的说法正确的是
A.氧气可以支持燃烧,说明氧气具有可燃性
B.带火星的木条一定能在含有氧气的集气瓶中复燃
C.鱼、虾等能在水中生存,说明氧气易溶于水
D.液氧属于纯净物
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制取气体所需装置如下图所示。
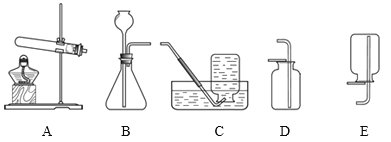
(1)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_________,其反应的化学方程式为_________。
(2)用高锰酸钾制取氧气时,所选用的收集装置是C或_________。将带火星的木条接近集气瓶口,看到木条_________,证明氧气已收集满。
相关试题