【题目】根据质量守恒定律回答下列问题:
(1)加热24.5gKClO和2gMnO的混合物,充分反应后,剩余固体的质量为16.9g,则产生氧气的质量为_______g。
(2)浓硝酸分解反应的化学方程式为:4HNO![]() 2HO+4NO↑+X↑。回答下列问题:
2HO+4NO↑+X↑。回答下列问题:
推断X的化学式是______,推断X化学式的依据是___________________________,此反应的基本反应类型属于______。
参考答案:
【答案】 9.6 O 化学反应前后原子种类数目不变 分解反应
【解析】本题考查了质量守恒定律的运用。
(1)根据质量守恒定律可知,产生氧气的质量=24.5g+2g-16.9=9.6g;
(2)根据质量守恒定律可知化学反应前后原子种类数目不变,由反应4HNO![]() 2HO+4NO↑+X↑,反应前4HNO3中含H、N、O原子个数分别为4、4、12,而反应后2H2O、4NO2中共含有H、N、O原子个数分别为4、4、10,根据反应前后原子种类、个数不变,可判断X分子由2个O原子构成,物质X的化学式为O2,此反应是由一种物质生成三种物质,属于分解反应。
2HO+4NO↑+X↑,反应前4HNO3中含H、N、O原子个数分别为4、4、12,而反应后2H2O、4NO2中共含有H、N、O原子个数分别为4、4、10,根据反应前后原子种类、个数不变,可判断X分子由2个O原子构成,物质X的化学式为O2,此反应是由一种物质生成三种物质,属于分解反应。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学用语回答下列问题:
(1)地壳中含量最多的元素是___________________________________;
(2)氧气分子_________________________________________________;
(3)两个氮原子_______________________________________________;
(4)2个镁离子_______________________________________________;
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图所示装置可用于野外获取淡水,工作原理如图所示.
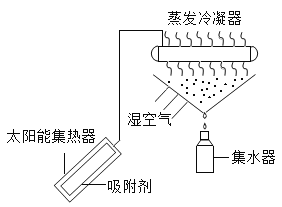
(1)蒸发冷凝器中发生的是________(填“物理”或“化学”)变化。
(2)吸附剂中主要物质为SiO和CaCl,SiO中硅元素的化合价为_________,CaCl中钙、氯元素的质量比为_________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】结合下列有关实验,回答问题。
(1)硫在氧气中燃烧的实验:在集气瓶中预先放少量水,目的是_______________________,
反应的化学方程式为_______________________。
(2)木炭在氧气中燃烧的实验:
用坩埚钳夹持点燃后的木炭,伸入氧气瓶的操作,是由瓶口向下缓慢伸入,这样的操作的目的是_____________。
(3)下列两个实验都用到红磷,实验时取用红磷的量不会影响实验结论的是_____________。
A.测定空气中氧气的含量 B.验证质量守恒定律
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下是实验室制取气体的常用仪器,回答下列问题。

(1)仪器E的名称为_______________;
(2)在实验室里,用高锰酸钾为药品来制取氧气,并用排水法收集。
①该反应的化学方程式为______________________________;
②组装制取装置时,需选择上图中的a、b、e、f、h、l、m、n和______________;
③当看到____________现象,证明氧气已经收集满了;
④实验完毕后,发现水槽中的水沿导管倒流了,你应采取的紧急措施是____________。
(3)用排水法收集一瓶氧气让蜡烛在其中燃烧,然后倒入澄清石灰水振荡,通过观察现象即可得出蜡烛组成中一定含有____________元素。
(4)某同学要用过氧化氢溶液和二氧化锰混合制取氧气:
①使用仪器c的作用是____________________________;
②反应的化学方程式为____________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】结合下图所示实验,请回答下列问题.
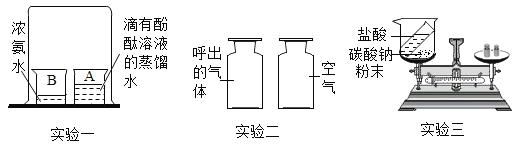
实验一的目的是利用浓氨水的碱性和挥发性,验证了分子是______;
实验二中,证明呼出的气体比空气中氧气含量少的操作是向两瓶中分别______;
实验三中,通过测定盐酸和碳酸钠粉末反应前后的质量来验证质量守恒定律,前后两次称量结果不一致,原因是没有称量______的质量.
-
科目: 来源: 题型:
查看答案和解析>>【题目】图a是两种元素的信息,图b是氟元素原子结构示意图。下列说法正确的是
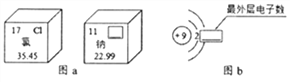
A. 图a方框右上角横线上应填写NA
B. 氯元素属于金属元素
C. 图b方框横线上的数字是9
D. 氯元素与钠元素形成的化合物的化学式是NaCl
相关试题

