【题目】(15分)某校80周年校庆举行社团开放日,化学社的同学在老师的指导下,设计了如下实验装置进行气体制取和性质实验的探究:
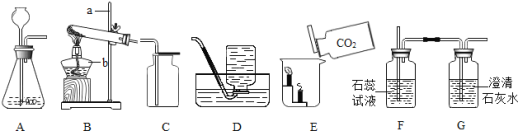
(1)请写出仪器名称a b
(2)实验室制取氧气时,可选用的发生装置是 (填写装置的字母代号,下同),实验室制取二氧化碳气体时发生的化学反应方程式为 ,收集二氧化碳的装置是 。
(3)如图E所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的化学性质是 。
(4)若装置A中反应剧烈,从实验安全角度考虑,不宣采取的措施有 (填序号)
① 用容积较小的锥形瓶
② 将长颈漏斗换成针筒减慢液体的滴加速度
③ 加热反应物
④ 降低液体反应物的浓度
(5)同学用图中A、F、G装置组合制取二氧化碳气体并验证相关性质.F装置中反应现象是 ,发生的化学反应方程式为 ,G装置中发生的化学反应方程式为 .
参考答案:
【答案】(1)a铁架台; b酒精灯;(2)A或B; ![]() ,C;(3)不燃烧、不支持燃烧;(4)①③;(5)紫色石蕊试液变成红色;
,C;(3)不燃烧、不支持燃烧;(4)①③;(5)紫色石蕊试液变成红色;![]() ;
; ![]() ;
;
【解析】
试题分析:(1)a是铁架台,b是酒精灯;(2)实验室制取氧气可以用过氧化氢在常温下分解,则可以选择装置A做反应容器,也可以用加热高锰酸钾或者氯酸钾与二氧化锰的混合物,则可以选择装置B做反应容器;二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集;(3)蜡烛熄灭说明二氧化碳不燃烧不支持燃烧;(4)① 用容积较小的锥形瓶,则气体在有限的空间内聚集更易发生爆炸;② 液体加入的速度越快则反应速率越快,故将长颈漏斗换成针筒减慢液体的滴加速度可以减慢化学反应速率;③ 温度越高则反应速率越快,加热反应物可以加快化学反应速率;④ 液体的浓度越大则反应越快,降低液体反应物的浓度可以减慢化学反应速率;(5)二氧化碳和水反应生成碳酸,而碳酸显酸性,可以使紫色的石蕊溶液变红;二氧化碳和石灰水中的氢氧化钙反应生成不溶性的碳酸钙和水,据此书写化学方程式;
-
科目: 来源: 题型:
查看答案和解析>>【题目】我市中考实行网上阅卷,答题时必需用2B铅笔填涂答题卡,2B铅笔的主要成分是
A.石墨 B.金刚石 C.木炭 D.C60
-
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)如图是A、B、C三种固体物质(固体组成与溶质相同)的溶解度曲线。在t1℃时,将质量为ag的A、B、C三种物质分别加入100g水中,根据图示回答下列问题:
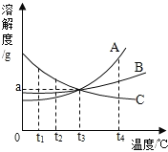
(1)三种物质中,随温度升高溶解度减小的物质是_______;
(2)
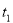 ℃时,所得三种物质的溶液中为不饱和溶液的是_______;
℃时,所得三种物质的溶液中为不饱和溶液的是_______;(3)若使这三种溶液溶质的质量分数相等,则温度应由
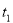 ℃升至 ℃;
℃升至 ℃;(4)若将温度由
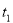 ℃升至
℃升至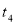 ℃时,三种溶液中溶质质量分数的大小关系为 。
℃时,三种溶液中溶质质量分数的大小关系为 。 -
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)2013年3月22日是今年的世界水日.今年世界水日的主题是“21 世纪的水”,意在要求人们立即采取节水和开发水资源行动,以保障 21 世纪人类用水.
(1)下列正确的是
A.自然界中的水大多数为纯净物
B.水中
 的增多会引起水体的富营养化
的增多会引起水体的富营养化C.只有用蒸馏的方法才能降低水的硬度
D.“绿色食品”、“白色污染”、“赤潮”说的都不是颜色问题
(2)如图是自来水厂净水过程示意图:
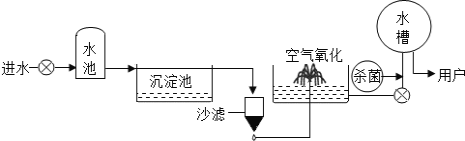
①沉淀池中加入的絮凝剂可能是 ; 自来水厂净水过程中加入活性炭除去杂质,是利用了活性炭的 性;
②小玲参加了一次户外训练活动郊游打来河水,用肥皂洗衣服时发现泡沫很少,且有浮渣,衣服洗不干净.据此推测当地的河水可能为 (填“硬水”或“软水”),生活中可用 的方法来净化它.
③自来水的生产过程包括以下流程,其中发生化学变化的是 ;
A.自然沉降 B.消毒杀菌 C.沙滤
④请你举出一种生活中节约用水的措施 .
(3)高铁酸钾(
 )是一种新型、高效的多功能水处理剂.高铁酸钾受热时发生的反应为
)是一种新型、高效的多功能水处理剂.高铁酸钾受热时发生的反应为

 ,则R是 (填化学式)
,则R是 (填化学式) -
科目: 来源: 题型:
查看答案和解析>>【题目】今有四种粒子的结构示意图,下列说法不正确的是
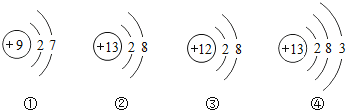
A.它们表示四种元素
B.④表示的元素在化合物通常显+3价
C.②③所表示的离子的符号为
 、
、
D.①表示的粒子在化学反应中易得电子
-
科目: 来源: 题型:
查看答案和解析>>【题目】日常生活中除去油污的方法很多,下列现象不属于乳化的是
A.修车工用汽油洗去手上的油污 B.洗发精洗去头发上的油脂
C.洗面奶洗去皮肤上的油脂 D.洗洁精洗去餐具上的油污
-
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)目前市场上的补钙药剂很多,下图是某品牌补钙药品的部分说明书.

为测定其含量是否达标,某兴趣小组的同学取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应):
加入稀盐酸的质量/g
0
20
40
60
80
100
烧杯中剩余物质质量/g
10
29.12
48.24
67.36
86.48
106.48
请你根据题给信息和表中数据,回答下列问题:
(1)实验过程中将钙片研碎的目的是: .
(2)完全反应后,产生二氧化碳的质量为 g.
(3)试通过计算说明,该品牌钙片含量是否达标.(写出计算过程)
(4)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为 g.
相关试题

