【题目】将氢氧化钠和氯化钠的混合物19.3g,放入80.7g水中使其完全溶解,再加入100g溶质质量分数为7.3%的稀盐酸,恰好完全反应。试计算:
(1)将上述浓度的稀盐酸100克稀释为溶质质量分数为4%的稀盐酸,需要加入水的质量;
(2)原混合物中氢氧化钠的质量;
(3)反应后所得溶液中溶质的质量。
参考答案:
【答案】(1)82.5克 (2)8克 (3)23克
【解析】
试题分析:(l)稀盐酸中溶质的质量为:l00g×7.3%=7.3g;
(2)设氢氧化钠的质量为x,生成氯化钠的质量为y.
NaOH + HCl = NaCl +H2O
40 36.5 58.5
X 7.3g y
![]()
解得:x=8g y=11.7g
(3)所得溶液中溶质的质量为:11.7克+19.3克-8克=23克
答:(1)l00g 7.3%的稀盐酸中溶质的质量是7.3g;
(2)原混合物中氢氧化钠的质量是8g;
(3)反应后所得溶液中溶质的质量是23克
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图中能正确反映其对应关系的是 ( )
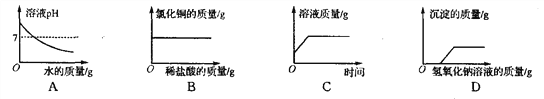
A. 向氢氧化钠溶液中不断加水,溶液pH与加入水的质量的关系
B. 向盛有氧化铜的烧杯中加入稀盐酸至过量,生成氯化铜质量与加入稀盐酸质量的关系
C. 一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
D. 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液,生成沉淀与加入氢氧化钠溶液的质量关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去),其中A为金属氧化物,E、F为金属单质,且F为紫红色,化学反应②和③的基本反应类型相同。
请按要求填空:
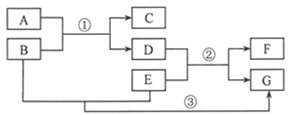
(1)物质C的化学式为 。
(2)写出反应②的一个化学方程式 。
(3)反应③的基本反应类型是 。
(4)E、F和氢由强到弱的金属活动性顺序为 (填元素符号)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是A、B、C三种物质的溶解度曲线,下列说法错误的是
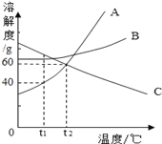
A.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
B.当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A
C.升高温度可使接近饱和的C溶液变为饱和溶液
D.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质属于氧化物的是
A.KMnO4 B.CO2 C.O2 D.H2SO4
-
科目: 来源: 题型:
查看答案和解析>>【题目】用分子、原子的观点分析下列生活中的现象,其解释不合理的是
A.50mL水与50mL酒精混合后,总体积小于100mL---------分子之间有间隔
B.八月桂花飘香---------分子在不断运动
C.1滴水中约含1.67×1021个水分子---------分子很小
D.水结成冰---------分子停止运动
-
科目: 来源: 题型:
查看答案和解析>>【题目】(15分)碳酸钠、碳酸氢钠是中学常见的化合物。
探究一:碳酸钠、碳酸氢钠与酸反应
如图所示,将两气球内的NaHCO3和Na2CO3同时倒入试管中。已知盐酸足量,且装置气密性良好。
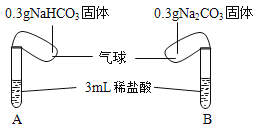
回答下列问题:
(1)碳酸钠俗名是 。
(2)实验过程中观察到的现象是: 。
(3)NaHCO3和Na2CO3都能与盐酸反应产生二氧化碳、水和氯化钠。任写出其中一个反应的化学方程式 。
(4)已知NaHCO3、Na2CO3的相对分子质量分别为84、106,通过计算:实验结束后, (填“A”或“B”)试管的气球更大。
探究二:碳酸氢钠、碳酸钠固体与酸反应的热效应
【发现问题】在探究一实验过程中用手触摸试管,发现盛NaHCO3的试管温度降低,而盛Na2CO3的试管温度升高。
【猜想与推测】甲同学由此推测:NaHCO3和盐酸反应为吸热反应,Na2CO3和盐酸反应为放热反应。
【实验与数据】乙同学认为甲同学推测不妥,通过以下多次实验后取平均值数据记录如下:
步骤①
步骤②
步骤③
步骤④
步骤⑤
测量10mL水温/℃
加入物质0.5 g
溶解后测量溶液温度t1/℃
静置一段时间后测量溶液温度t2/℃
加入20%盐酸10 mL反应后测量溶液温度t3/℃
20
NaHCO3
18.5
20.0
20.8
20
Na2CO3
23.3
20.0
23.7
【分析与结论】
(1)由步骤①~③比较得到的结论是 。
(2)由步骤④~⑤比较得到的结论是: 。
(3)结合上面探究活动,你认为甲同学推测的不妥之处是 。
相关试题

