【题目】工业烟气脱硫是将烟气中含有的二氧化硫除去。采用“双碱法”脱硫的工业流程如下。下列说法错误的是
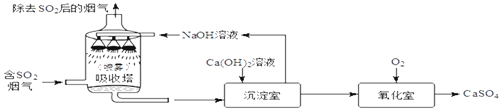
A. 流程中有三种元素化合价发生改变
B. 理论上如果生成13.6gCaSO4,那么实际吸收的SO2质量应该是6.4g
C. NaOH溶液喷成雾状的目的是增大接触面积,充分吸收SO2
D. 吸收塔中发生反应的基本类型是复分解反应
参考答案:
【答案】AD
【解析】A.单质中元素的化合价为零,化合物中元素的化合价代数和为零。二氧化硫中硫元素显+4价,硫酸钙中硫元素显+6价;氧气中氧的化合价为零,化合物中氧的化合价为-2价;流程中只有氧、硫两种元素化合价发生改变,错误;B. 据质量守恒定律可知反应前后元素的种类、质量不变,生成CaSO4与吸收的SO2中,硫元素的质量相等;要生成13.6gCaSO4,设实际吸收的质量应该是x;CaSO4 ~ SO2
136 64
13.6g x 136/13.6g=64/x x=6.4g 正确;C. NaOH溶液喷成雾状的目的是增大氢氧化钠和二氧化硫的接触面积, 使SO2吸收更彻底、更充分,正确;D.两种化合物相互结合生成两种新的化合物的反应,叫复分解反应,吸收塔中二氧化硫和氢氧化钠发生反应,生成亚硫酸钠和水,化学方程式为2NaOH+SO2===Na2SO3+H2O,不是复分解反应;错误。故选AD。
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类社会的发展离不开能源。当今社会,人类利用的能源主要来自化石燃料。
(1)化石燃料蕴藏的能量来源于生物体吸收的_____________; “可燃冰”又称天然气水合物,它是在海底的高压、低温条件下形成的,1体积“可燃冰”可储藏100~200体积的甲烷。下列关于“可燃冰”的叙述中,不正确的是_____________。
A.“可燃冰”不是冰 B.“可燃冰”有可能成为人类未来的重要能源
C.“可燃冰”的可燃成分是甲烷 D.“可燃冰”的实质是水变成的固态油
(2)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属_____________变化。石油中主要含有碳、氢元素,还含有硫、氮等元素,燃烧时会产生的污染物有_____________(写一种)。
(3)在实验室里,可用稀高锰酸钾溶液检验二氧化硫,现象是________________________;反应的化学方程式为:5SO2+2KMnO4+xH2O═K2SO4+2MnSO4+2H2SO4。其中x的值为_____________,恰好完全反应后,溶液中大量存在的阴离子是_____________(填符号)。
(4)开发和利用清洁高效而又用之不竭的新能源,是21世纪人类面临的重要课题。2006年1月起,我国部分地区推广使用乙醇汽油。乙醇可利用农作物发酵制得,农作物在催化剂作用下转化为葡萄糖(C6H12O6),然后葡萄糖在酒化酶的作用下分解为乙醇和二氧化碳,写出葡萄糖分解为乙醇的化学方程式_________。
(5)科学家用转基因的方法培育出一种“食电”细菌,它“吃进”电能,把二氧化碳和水转化为甲烷等物质,能量转化率高达80%,下列说法中正确的是_____________。
A.细菌“食电”过程能释放出氧气 B.上述反应属于化合反应
C.这种方法能缓解白色污染 D.“食电”细菌不属于生物
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁的生产流程示意图:

已知:①SiO2不溶于酸 ②Fe2(SO4)3 + Fe == 3FeSO4
回答下列问题:
(1)酸浸、过滤后滤液A中的金属阳离子是_______________。
(2)步骤Ⅱ中加入足量的铁粉目的是除去过量的酸,还可能有的作用是________________________。
(3)煅烧FeCO3生成产品I的化学反应方程式为______________________。
(4)已知几种盐的溶解度随温度变化的曲线如下图所示,产品Ⅱ的化学式为_____________,为了获得产品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,还需要进行的操作是蒸发浓缩、__________、洗涤、干燥。
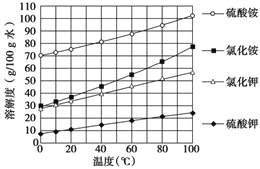
(5)检验产品Ⅱ晶体中是否含有少量的氯化物杂质需用到的试剂是________________________。
(6)步骤Ⅲ中可选用__________________(填序号)试剂调节溶液的pH。
A.稀硝酸 B.双氧水 C.氨水
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表是我国颁布的生活饮用水水质标准的部分内容。
项目
标准
感官指标
无异味、异臭等
化学指标
pH 6.5~8.5,铜<1.0mgL-1,氟化物<1.0mgL-1,游离氯≥0.3mgL-1等
⑴感官指标表现的是自来水的______性质(填“物理”或“化学”);若化学指标中的 pH=8时,表明自来水呈________ (填“酸性”、“碱性”或“中性”)。
⑵天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是__________。
⑶硬水给生活和生产带来很多麻烦,生活中可用______来区分硬水和软水,常用______的方法来降低水的硬度。
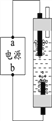
⑷液氯可以作为饮用水消毒剂。下图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气 和氯气,该反应的化学方程式为________;从能量变化角度看,该反应中将________能转化为化学能。
⑸饮用水消毒剂除了液氯以外,还有氯胺(NH2Cl)、臭氧(O3)等。O3中氧元素的化合价是_____。NH2Cl中氯元素与氢元素的质量比是_________。
⑹ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒。制取ClO2的反应过程示意图如下:
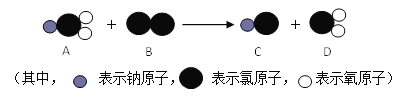
该反应的化学方程式是_________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】加热氯酸钾和二氧化锰的混合物可制备氧气,该反应的化学方程式为____________________,但实验中发现有刺激性气味的气体产生。
(提出问题)刺激性气味的气体是什么呢?
(猜想假设)猜想一:臭氧(化学式为O3) 猜想二:HCl 猜想三:Cl2
同学们认为不需要实验验证就可以判断猜想_______________是错误的,理由为_______________。
(查阅资料)(1)C12+H2O===HC1O+HCl。
(2)臭氧在MnO2存在的情况下极易分解成氧气。
(3)氯气可使湿润的淀粉碘化钾试纸变蓝。
(实验探究)
查阅资料后大家认为猜想一是错误的,理由为____________________________。他们进一步又做了如下实验:取氯酸钾和二氧化锰的混合物放人试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管口(如图),看到的现象是_____________,再将湿润的淀粉碘化钾试纸悬于试管口,试纸变_______________色,最终证明猜想三正确。
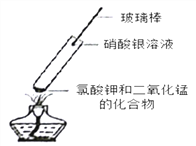
(反思拓展)
(1)欲证明二氧化锰是氯酸钾分解的催化剂,需证明二氧化锰的________、________在反应前后不变。
(2)自来水厂常用氯气来杀菌消毒,氯气和水反应后会产生H+、Clˉ和ClOˉ,而野外常用漂白粉[主要成分化学式为Ca(ClO)2]。你认为在水中起杀菌消毒作用的离子是_____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】图 1 所示装置可用于测定空气中氧气的含量,其中与集气瓶相连的压强传感器等电子设备能将集气瓶内气体压强精确地记录下来。图 2、图 3 是用该装置测得的红磷和木炭分别在集气 瓶中燃烧的压强-时间关系图(该装置气密性良好,p0 是集气瓶内初始压强,p 和 p′分别是反应结束后恢复到室温时集气瓶内的压强)。下列说法不正确的是( )
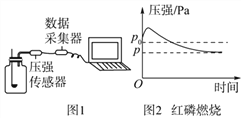

A. 燃烧匙内所装红磷或木炭的多少对实验结果无影响
B. 反应开始时集气瓶中压强瞬间变大是由燃烧放热造成的
C. p≈0.79p0,p′≈p0 是由反应前后气体体积变化造成的
D. 只可根据图 2 推出空气中氧气的含量
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是几种盐的溶解度曲线,根据曲线判断下列说法正确的是( )
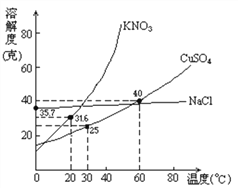
A. 20℃时,硝酸钾饱和溶液的质量分数是 31.6%
B. 40℃时,35g 氯化钠溶于 100g 水中,降温至 0℃时,可析出氯化钠晶体
C. 30℃时,将 35g 硝酸钾和 35g 氯化钠同时溶于 100g 水中,蒸发时先析出的是氯化钠
D. 60℃时,200g 水中溶解 80g 无水硫酸铜达饱和,降温至 30℃,可析出 30g 硫酸铜晶体
相关试题

